Clear Sky Science · zh
肿瘤周围脂肪组织通过3‑羟基犬尿喹啉酸介导抑制铁蛋白自噬而促进抗铁死亡
肿瘤周围的脂肪:隐蔽的保护者
许多癌症与柔软的脂肪紧密相邻。远非旁观者,这些邻近的脂肪能悄然帮助肿瘤抵抗化疗和现代免疫疗法。本研究揭示了肿瘤周围脂肪阻断癌细胞内一种由铁驱动的细胞死亡方式的意外机制,并表明破坏这一屏障可提高现有治疗的效果,尤其是在沿脂肪表面扩散的腹膜转移性癌症中。
位置如何赋予肿瘤优势
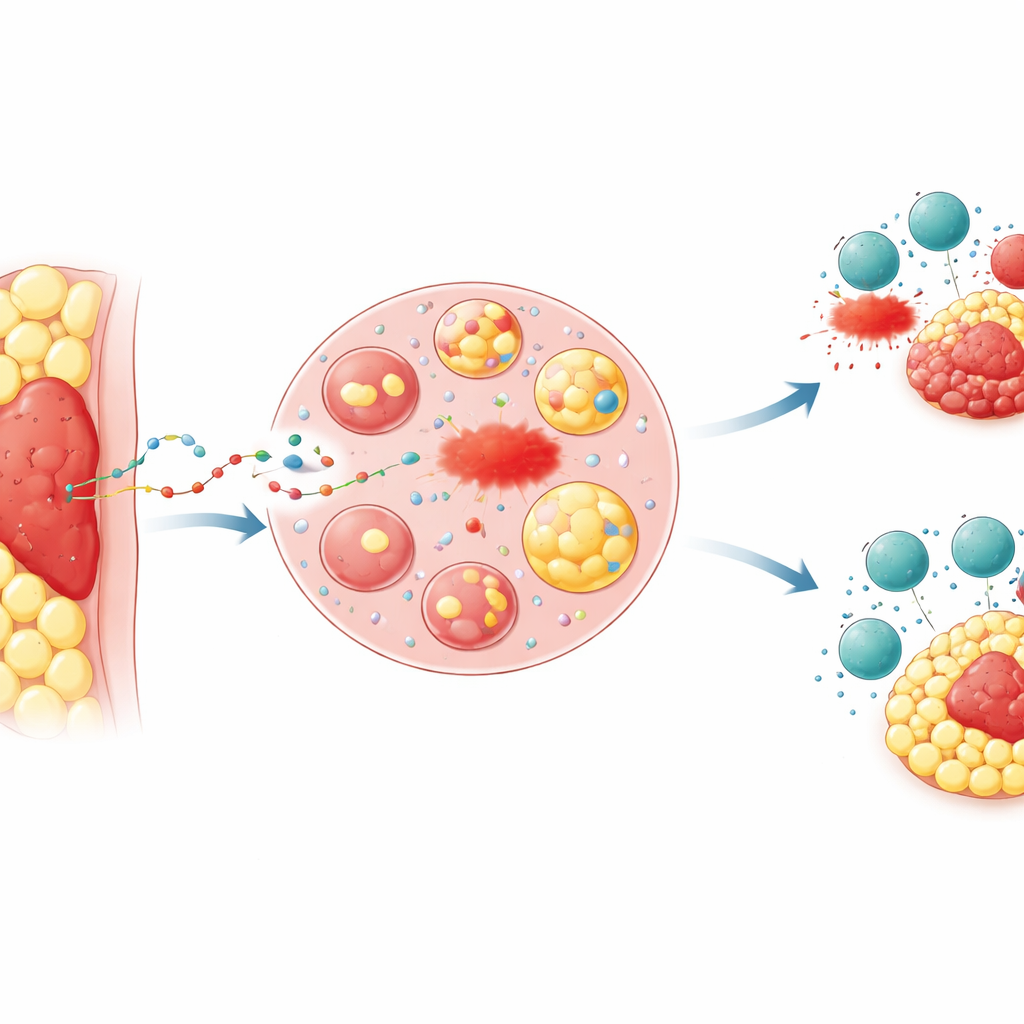
临床医生长期观察到,埋伏于脂肪中的肿瘤——例如侵入腹膜的晚期结直肠癌和胃癌——往往对治疗反应较差,预后更差。研究者将注意力集中在“肿瘤周围脂肪组织”——紧邻肿瘤的那一圈脂肪。在小鼠模型中,他们将相同的癌细胞种植在皮下(脂肪较少处)或直接植入脂肪垫。位于脂肪中的肿瘤生长更快,对诱导一种称为铁死亡的细胞死亡的药物更耐受,并且对杀伤性T细胞或抗‑PD‑1免疫治疗的敏感性降低。作为铁死亡发生标志的脂质损伤化学标记在脂肪包埋的肿瘤中显著减低,这与晚期结直肠和胃癌患者组织样本中观察到的模式一致。
癌细胞内的铁“保险箱”
铁死亡依赖游离铁;当足够的铁存在时,它会促使细胞膜发生失控的氧化,从而导致细胞死亡。癌细胞可以通过将铁储存在称为铁蛋白的蛋白壳中来缓冲这种威胁。研究团队探究邻近脂肪是否以某种方式重编了肿瘤的铁代谢。他们在来自人和鼠脂肪组织的培养液中培养癌细胞,发现这种“调节”培养基显著提高了细胞对铁死亡的抵抗力。蛋白质组分析显示两种主要铁蛋白亚基显著上调,而其它已知的铁死亡调控因子变化不大。与此同时,细胞内的游离铁池实际上下降。当研究者敲低铁蛋白时,脂肪来源培养基的保护效应消失,且脂肪丰富处位点的肿瘤变小并对铁驱动的损伤更敏感。
从脂肪到肿瘤的代谢信使
为找出脂肪分泌的物质,团队转向代谢组学——对小分子的全面筛查。有一种分子——犬尿喹啉酸(色氨酸的代谢产物)在脂肪调节培养基和生长于脂肪中的肿瘤中持续升高。包围这些肿瘤的液体中犬尿喹啉酸高而色氨酸低,表明局部环境被重编程。周围脂肪组织表达将色氨酸转化为犬尿喹啉酸的酶IDO1和TDO2水平较高,单细胞核RNA测序显示脂肪细胞及其前体细胞是主要来源。当癌细胞暴露于犬尿喹啉酸时,它们提高了铁蛋白水平、降低了游离铁并抵抗铁死亡。在脂肪中阻断IDO1和TDO2会消除这种铁蛋白升高,除非外源补充犬尿喹啉酸。
阻断铁释放阀门的单一分子
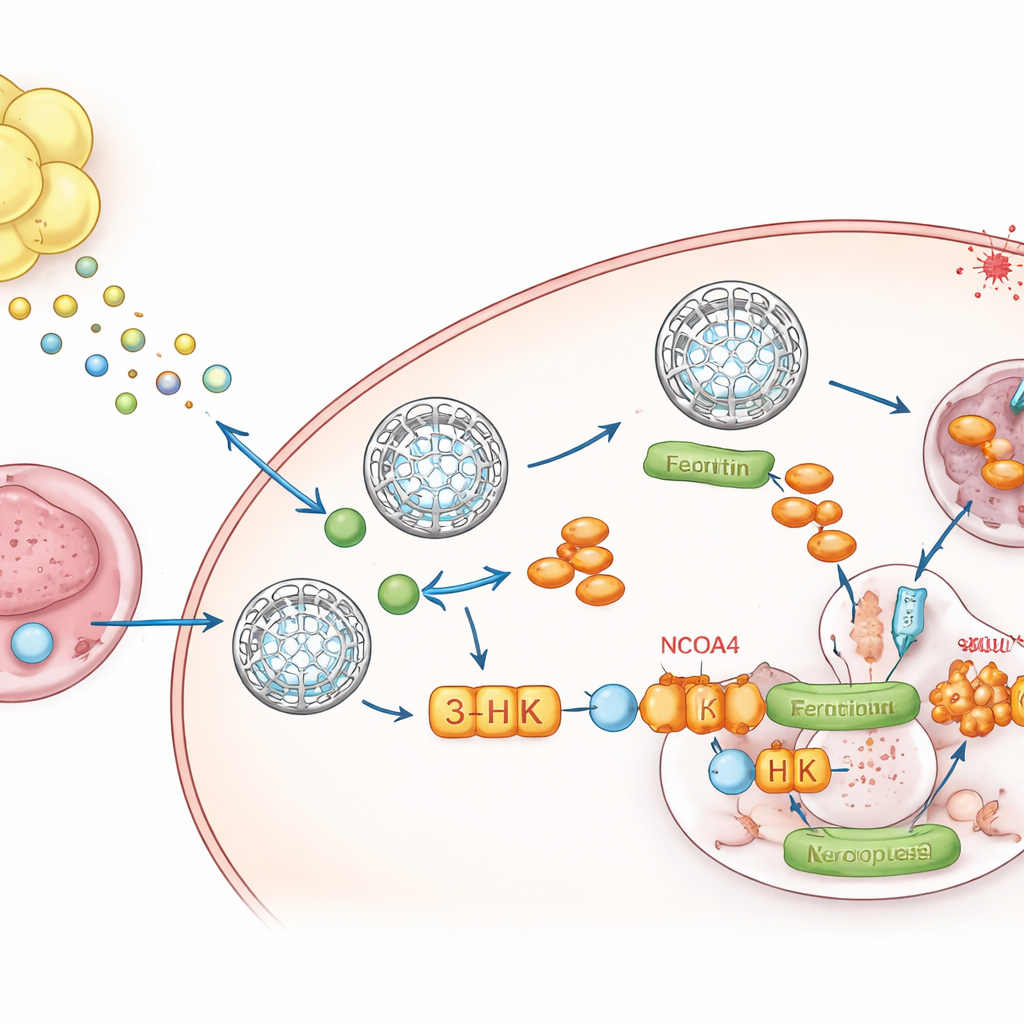
犬尿喹啉酸并非独自发挥作用。在肿瘤细胞内,它沿途被转化为多种代谢物。通过选择性阻断各个步骤,作者发现一种中间产物3‑羟基犬尿喹啉酸(3‑HK)是关键。即使在低剂量下,3‑HK也能稳定铁蛋白、减少铁释放,并强力保护细胞免受铁死亡。机制上,3‑HK直接结合一种名为NCOA4的蛋白,NCOA4通常将铁蛋白运送到细胞“回收中心”,在那里铁蛋白被降解、铁被释放。结构与生物物理实验表明3‑HK钩住NCOA4并阻止其与铁蛋白对接,有效地将这些铁“保险箱”锁定在原位,剥夺铁死亡所需的金属。当去除NCOA4时,3‑HK无法再提升铁蛋白或保护细胞免受铁死亡。
将屏障转化为治疗靶点
由于癌细胞的铁死亡可增强抗肿瘤免疫,脂肪驱动的3‑HK–铁蛋白通路为为何富含脂肪的转移病灶(如结直肠或胃癌的腹膜种植)常常对免疫治疗耐受提供了解释。在多种小鼠模型中,同时抑制IDO1和TDO2降低了肿瘤‑脂肪生态位中的犬尿喹啉酸与3‑HK,减少了铁蛋白积累,使肿瘤对铁死亡诱导剂更加脆弱。最显著的是,将IDO1/TDO2抑制剂与抗‑PD‑1抗体联合使用能显著增强肿瘤控制,包括在腹膜转移模型中;而当化学方式阻断铁死亡时,这种益处消失。患者数据支持这些发现:腹膜转移灶显示铁蛋白更高且脂质损伤更低,与原发肿瘤相比,预测高3‑HK丰度的基因特征与病情更晚期和更差的生存相关。
这对未来癌症治疗的意义
这项工作揭示了脂肪与肿瘤之间此前未被注意到的对话:周围脂肪制造犬尿喹啉酸并输送给癌细胞,从而提高3‑HK水平,锁定铁在铁蛋白内并阻断铁死亡。这样,脂肪不仅帮助肿瘤抵御以铁死亡为靶的药物,还削弱了免疫系统和免疫检查点抑制剂消灭肿瘤的能力。通过中断这一犬尿喹啉酸–3‑HK–铁蛋白轴,例如联合使用IDO1/TDO2抑制剂,临床上或可剥除这一保护屏障,使嵌入脂肪的肿瘤对免疫治疗和其他治疗更为敏感。
引用: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
关键词: 肿瘤微环境, 铁死亡, 犬尿喹啉酸途径, 肿瘤周围脂肪组织, 癌症免疫治疗