Clear Sky Science · de
Peritumorales Fettgewebe fördert Ferroptoseresistenz durch 3‑Hydroxykynurenin‑vermittelte Unterdrückung der Ferritinophagie
Fett um Tumoren: Ein verborgener Schutz
Viele Krebserkrankungen wachsen in engem Kontakt mit weichem, polsterndem Fettgewebe. Dieses nahegelegene Fett ist keineswegs ein passiver Beobachter, sondern kann Tumoren heimlich helfen, sowohl Chemotherapien als auch moderne Immuntherapien zu überstehen. Diese Studie enthüllt einen überraschenden Mechanismus, durch den das umgebende Fett eine Art eisengetriebener Zellsterblichkeit in Krebszellen blockiert, und zeigt, wie die Unterbrechung dieses Schutzschilds bestehende Behandlungen wirkungsvoller machen könnte — insbesondere bei Bauchkrebsarten, die sich über fettige Oberflächen ausbreiten.
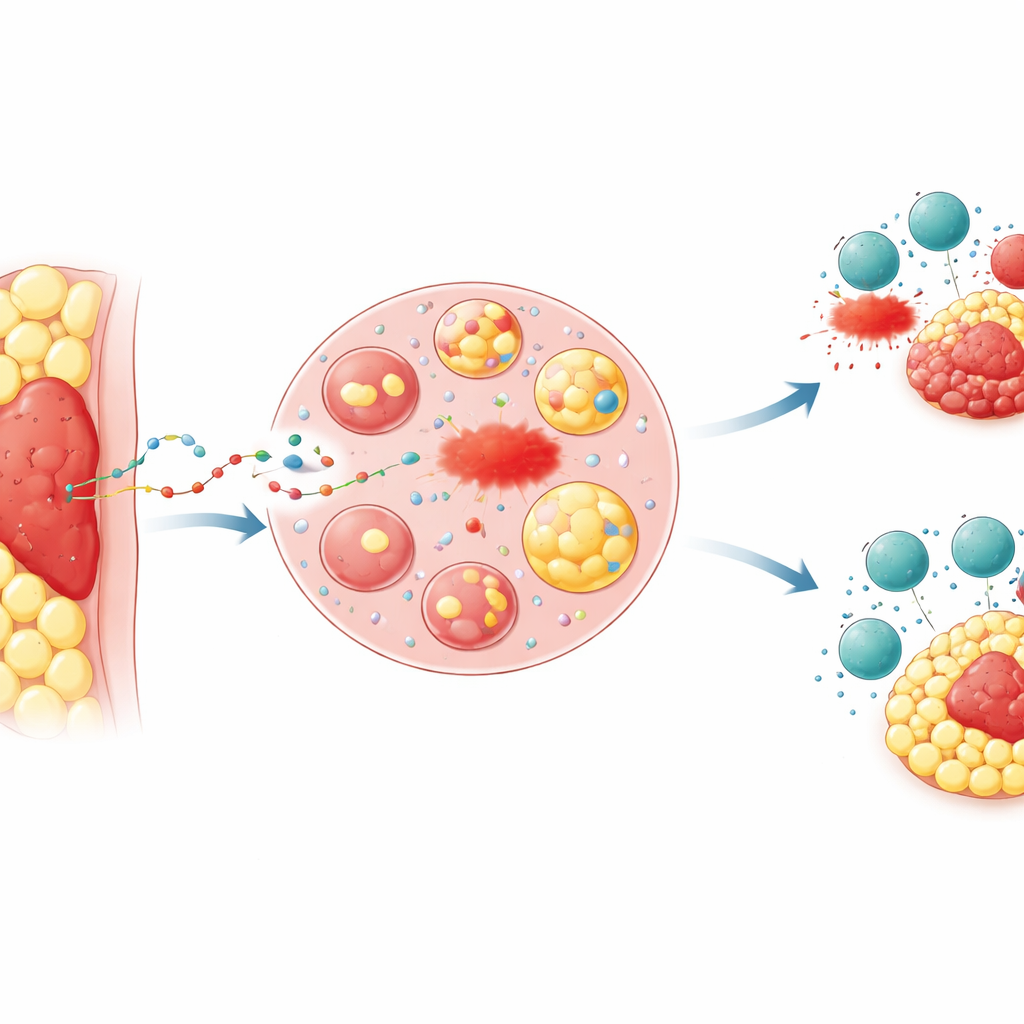
Wenn der Standort Tumoren einen Vorteil verschafft
Ärzte haben lange beobachtet, dass Tumoren, die im Fett eingebettet sind, wie fortgeschrittene Kolon‑ und Magenkrebserkrankungen, die das Bauchfell durchdringen, häufig schlecht auf Therapien ansprechen und mit schlechteren Prognosen einhergehen. Die Forscher konzentrierten sich auf das „peritumorale Fettgewebe“—den Fettkranz unmittelbar um einen Tumor. In Mausmodellen setzten sie dieselben Krebszellen entweder unter die Haut, wo wenig Fett vorhanden ist, oder direkt in ein Fettpolster. In Fett eingebettete Tumoren wuchsen schneller, ließen sich schwerer mit Wirkstoffen töten, die eine Form des Zelltods namens Ferroptose auslösen, und waren weniger empfindlich gegenüber der Attacke durch killer‑T‑Zellen oder gegenüber Anti‑PD‑1‑Immuntherapie. Chemische Marker von Lipidschäden, die anzeigen, dass Ferroptose stattfindet, waren in den in Fett eingebetteten Tumoren deutlich niedriger — ein Muster, das sich auch in Gewebeproben von Patientinnen und Patienten mit fortgeschrittenem kolorektalem und Magenkrebs zeigte.
Eiserne Tresore innerhalb von Krebszellen
Ferroptose hängt von freiem Eisen ab; wenn genügend Eisen verfügbar ist, treibt es die unkontrollierte Oxidation von Zellmembranen voran und tötet die Zelle. Krebszellen können dieser Bedrohung begegnen, indem sie Eisen in Proteinhüllen namens Ferritin speichern. Das Team fragte, ob das nahegelegene Fett die Eisenhandhabung der Tumoren irgendwie umlenkt. Sie kultivierten Krebszellen in Flüssigkeit aus menschlichem und Maus‑Fettgewebe und fanden, dass dieses „konditionierte“ Medium die Zellen deutlich resistenter gegen Ferroptose machte. Proteomische Analysen zeigten einen starken Anstieg beider Haupt‑Ferritin‑Untereinheiten, ohne größere Veränderungen bei anderen bekannten Ferroptose‑Regulatoren. Gleichzeitig fiel der Pool an freiem Eisen innerhalb der Zellen tatsächlich. Als die Forscher Ferritin herunterregulierten, verschwand der Schutz durch das fettabgeleitete Medium, und Tumoren an fettreichen Stellen wurden kleiner und empfindlicher gegenüber eisengetriebenen Schäden.
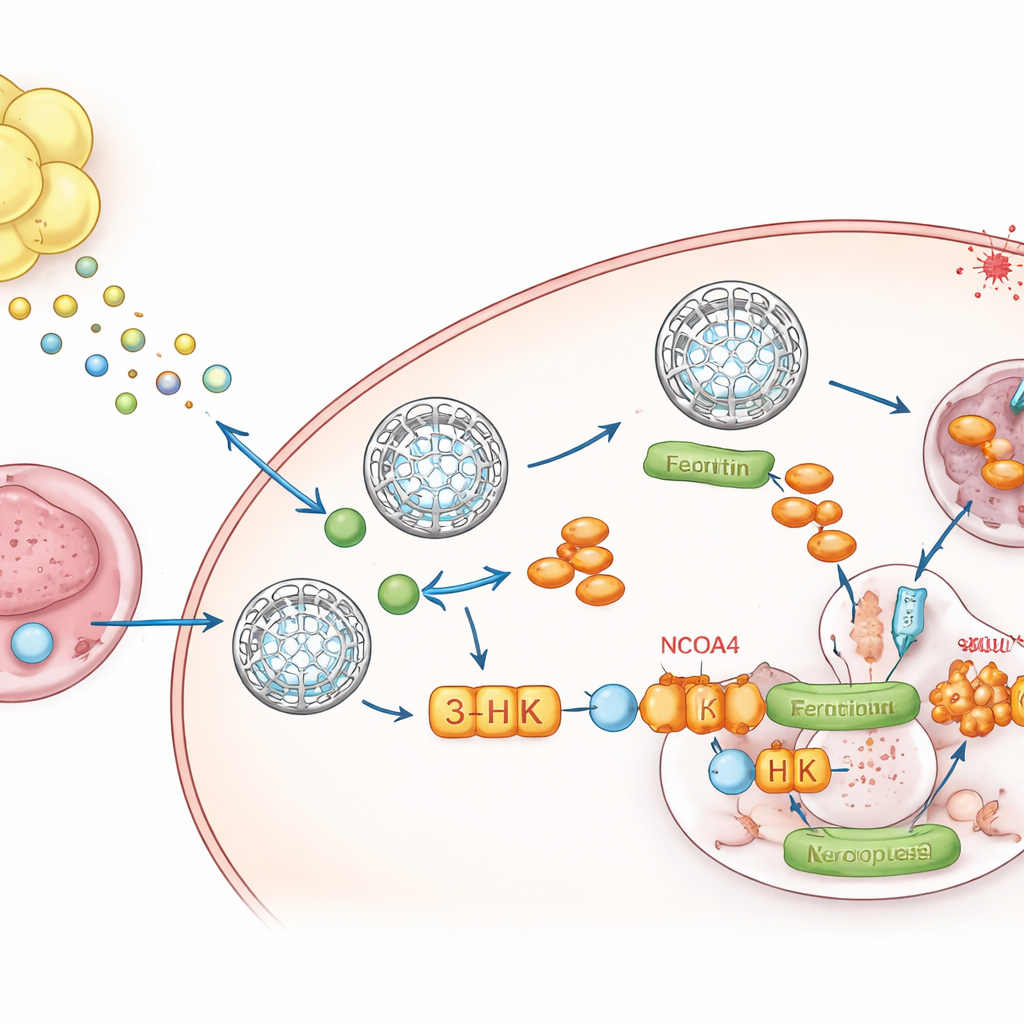
Ein metabolischer Bote von Fett zum Tumor
Um zu ermitteln, was das Fett aussendet, wandte sich das Team der Metabolomik zu, einer Analyse kleiner Moleküle. Eine Verbindung, Kynurenin, ein Abbauprodukt der Aminosäure Tryptophan, fiel als durchgängig erhöht in fettkonditioniertem Medium und in Tumoren, die im Fett wuchsen, auf. Die Flüssigkeit, die diese Tumoren umgab, enthielt viel Kynurenin und wenig Tryptophan, was zeigt, dass die lokale Umgebung umprogrammiert ist. Das umgebende Fett exprimierte hohe Mengen der Enzyme IDO1 und TDO2, die Kynurenin produzieren, und Einzelzellkern‑RNA‑Sequenzierung zeigte, dass Adipozyten und ihre Vorläuferzellen die Hauptquellen sind. Wurden Krebszellen Kynurenin ausgesetzt, erhöhten sie ihre Ferritinspiegel, verringerten freies Eisen und wurden gegen Ferroptose resistent. Das Blockieren von IDO1 und TDO2 im Fett beseitigte diesen Ferritinanstieg, sofern nicht Kynurenin wieder zugeführt wurde.
Ein einzelnes Molekül, das das Eisen‑Auslassventil blockiert
Kynurenin wirkt nicht allein. Innerhalb der Tumorzellen wird es entlang eines Stoffwechselwegs in mehrere Metaboliten umgewandelt. Durch selektives Blockieren einzelner Schritte entdeckten die Autoren, dass ein Zwischenprodukt, 3‑Hydroxykynurenin (3‑HK), der Schlüsselakteur ist. 3‑HK stabilisierte selbst in niedrigen Dosen Ferritin, reduzierte die Eisenfreisetzung und schützte Zellen stark vor Ferroptose. Mechanistisch band 3‑HK direkt an ein Protein namens NCOA4, das normalerweise Ferritin zu zellulären „Recyclingzentren“ begleitet, wo es abgebaut und Eisen freigesetzt wird. Strukturelle und biophysikalische Experimente zeigten, dass 3‑HK an NCOA4 andockt und dessen Verbindung mit Ferritin verhindert, wodurch diese Eisentreuhandbehälter effektiv fixiert werden und der Ferroptose das Metall entzogen wird, das sie zum Entflammen braucht. Wenn NCOA4 entfernt wurde, konnte 3‑HK Ferritin nicht mehr erhöhen oder Zellen gegen ferroptotischen Tod verteidigen.
Aus dem Schutzschild ein therapeutisches Ziel machen
Da ferroptotischer Zelltod von Krebszellen die antitumorale Immunität verstärken kann, liefert der durch Fett gesteuerte 3‑HK–Ferritin‑Weg eine Erklärung dafür, warum fettreiche Metastasen, wie peritoneale Implantate von Darm‑ oder Magenkrebsen, oft gegenüber Immuntherapien resistent sind. In mehreren Mausmodellen senkte die gleichzeitige Hemmung von IDO1 und TDO2 Kynurenin und 3‑HK in der Tumor‑Fett‑Nische, verringerte die Ferritinansammlung und machte Tumoren deutlich anfälliger für Ferroptose‑Induktoren. Am auffälligsten war, dass die Kombination von IDO1/TDO2‑Inhibitoren mit Anti‑PD‑1‑Antikörpern eine wesentlich stärkere Tumorkontrolle erzielte, auch in Modellen peritonealer Metastasen, und dieser Vorteil verlor sich, wenn Ferroptose chemisch blockiert wurde. Patientendaten stützten diese Befunde: Peritoneale Metastasen zeigten höheres Ferritin und geringere Lipidschäden als Primärtumoren, und Gen‑Signaturen, die reichlich 3‑HK vorhersagten, korrelierten mit fortgeschritteneren Erkrankungsstadien und schlechterem Überleben.
Was das für die zukünftige Krebsbehandlung bedeutet
Diese Arbeit offenbart einen zuvor verborgenen Dialog zwischen Fett und Tumor, in dem das umgebende Fett Kynurenin herstellt, es an Krebszellen abgibt und dadurch 3‑HK‑Spiegel erhöht, die Eisen im Ferritin einkapseln und Ferroptose blockieren. Damit hilft das Fett den Tumoren nicht nur, Ferroptose‑gerichtete Medikamente zu überstehen, sondern schwächt auch die Fähigkeit des Immunsystems und von Checkpoint‑Inhibitoren, sie zu zerstören. Durch die Unterbrechung dieser Kynurenin–3‑HK–Ferritin‑Achse, etwa mit kombinierten IDO1/TDO2‑Inhibitoren, könnten Klinikern dieser Schutzschild entzogen und fett‑eingebettete Tumoren deutlich empfänglicher für Immuntherapie und andere Behandlungen gemacht werden.
Zitation: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Schlüsselwörter: Tumormikroumgebung, Ferroptose, Kynurenin‑Stoffwechselweg, peritumorales Fettgewebe, Krebsimmuntherapie