Clear Sky Science · ja
腫瘍周囲脂肪組織は3-ヒドロキシキヌレニンを介したフェリチノフォジー抑制によりフェロトーシス耐性を促進する
腫瘍周囲の脂肪:隠れた保護者
多くのがんは柔らかくクッション性のある脂肪と密接に接して増殖します。単なる受動的な存在ではなく、周囲脂肪は化学療法や最新の免疫療法に対して腫瘍を密かに守ることがあります。本研究は、腫瘍を囲む脂肪が腫瘍細胞内の鉄依存型の細胞死を遮断する驚くべき仕組みを明らかにし、この防御を破壊することで既存治療、特に脂肪面に広がる腹腔内がんに対する治療効果が高まる可能性を示します。
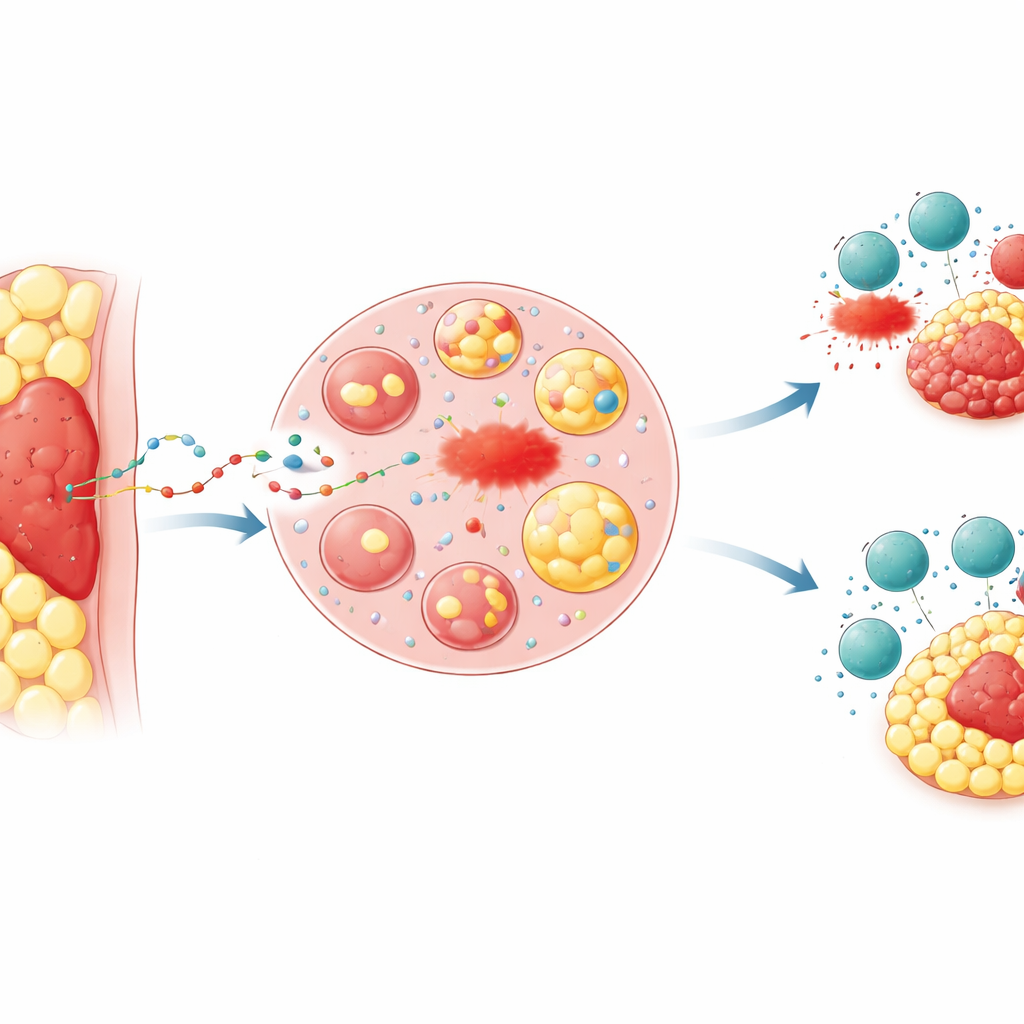
部位がもたらす腫瘍の優位性
臨床では、腹膜に浸潤する進行大腸がんや胃がんのように脂肪に埋もれた腫瘍は治療反応が悪く、予後不良になることが長く知られてきました。研究チームは腫瘍を直ちに取り巻く輪状の脂肪、すなわち「腫瘍周囲脂肪組織」に着目しました。マウスモデルでは、同一のがん細胞を皮下(脂肪の少ない部位)または脂肪パッド内に移植しました。脂肪に囲まれた腫瘍はより速く成長し、フェロトーシスを誘導する薬剤に対して死ににくく、キラーT細胞や抗PD-1免疫療法による攻撃にも感受性が低下しました。脂質損傷の化学的マーカー(フェロトーシスが進行している指標)は脂肪内腫瘍で著しく低く、進行した大腸・胃がん患者の組織サンプルに見られるパターンと一致しました。
がん細胞内の鉄の金庫
フェロトーシスは遊離鉄に依存します。十分な鉄が存在すると細胞膜の過酸化が暴走し、細胞死が引き起こされます。がん細胞はフェリチンと呼ばれるタンパク質の殻に鉄を貯蔵することでこの脅威を緩和できます。周囲の脂肪が腫瘍の鉄代謝をどのように書き換えるかを調べるため、研究者らはヒトおよびマウスの脂肪組織由来の培養液でがん細胞を培養しました。すると、この「コンディションドメディア」は細胞を著しくフェロトーシス耐性にしました。プロテオミクス解析では、既知のフェロトーシス調節因子に大きな変化はない一方で、主要なフェリチンサブユニットが強く増加していました。同時に細胞内の遊離鉄プールはむしろ減少しました。フェリチンをノックダウンすると脂肪由来メディアの保護効果は消失し、脂肪豊富な部位の腫瘍は小さくなり鉄による損傷に敏感になりました。
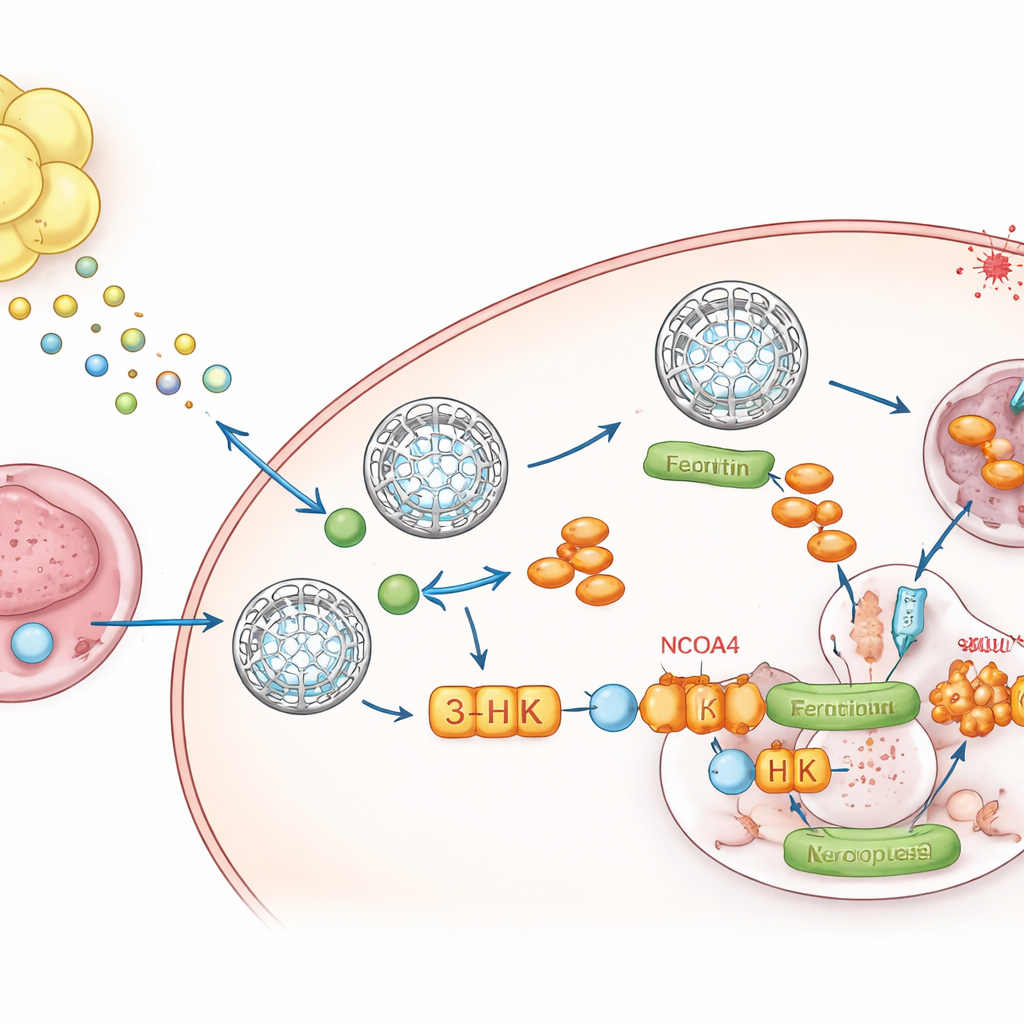
脂肪から腫瘍へ送られる代謝メッセンジャー
脂肪が何を送っているのかを特定するため、研究チームは低分子の網羅的解析(メタボロミクス)を行いました。トリプトファンの分解生成物であるキヌレニンが、脂肪で処理された培地や脂肪内で増殖する腫瘍に一貫して上昇している化合物として際立ちました。これらの腫瘍を取り巻く体液はキヌレニン高くトリプトファン低く、局所環境が書き換えられていることを示しています。周囲の脂肪組織はキヌレニンを産生する酵素IDO1およびTDO2を高発現しており、単一核RNAシーケンスは脂肪細胞とその前駆細胞が主要な供給源であることを示しました。がん細胞をキヌレニンに曝露するとフェリチンが増加し、遊離鉄が低下し、フェロトーシスに抵抗しました。脂肪でのIDO1/TDO2阻害はこのフェリチン増加を消失させ、キヌレニンを戻すと再び増加しました。
鉄の放出弁を塞ぐ単一分子
キヌレニン単独で作用するわけではありません。腫瘍細胞内でキヌレニンは複数の代謝物に変換されます。個々のステップを選択的に阻害することで、著者らは中間代謝物の一つ、3-ヒドロキシキヌレニン(3-HK)が主要因子であることを突き止めました。低用量でも3-HKはフェリチンを安定化させ、鉄の放出を抑え、細胞を強力にフェロトーシスから保護しました。分子機構として、3-HKは通常フェリチンを細胞内の“リサイクルセンター”へ運び分解して鉄を放出する役割を持つNCOA4というタンパク質に直接結合しました。構造生物学的および生物物理学的実験は、3-HKがNCOA4に結びつき、NCOA4がフェリチンにドッキングするのを妨げることで、これらの鉄の金庫を固定化し、フェロトーシスが必要とする金属を枯渇させることを示しました。NCOA4を除去すると3-HKはもはやフェリチンを増加させえず、フェロトーシスに対する防御も失われました。
防御を治療標的に変える
がん細胞のフェロトーシス死は抗腫瘍免疫を高めうるため、脂肪駆動の3-HK–フェリチン経路は、腹膜転移など脂肪に富む転移巣が免疫療法に抵抗する理由を説明します。複数のマウスモデルでIDO1とTDO2を同時に阻害すると腫瘍–脂肪ニッチのキヌレニンと3-HKが低下し、フェリチン蓄積が減少して腫瘍はフェロトーシス誘導剤に対してはるかに脆弱になりました。最も顕著だったのは、IDO1/TDO2阻害剤と抗PD-1抗体の併用が腫瘍抑制を大きく強化したことで、腹膜転移モデルでも同様の効果が得られ、なおかつこの利点はフェロトーシスを化学的に阻害すると失われました。患者データもこれらの所見を支持しました:腹膜転移は原発腫瘍より高いフェリチンと低い脂質損傷を示し、豊富な3-HKを予測する遺伝子署名はより進行した疾患と生存率の低下に相関していました。
今後のがん治療への示唆
本研究は脂肪と腫瘍の間に従来見落とされていた対話を明らかにします。周囲の脂肪組織がキヌレニンを産生してがん細胞に供給し、それが3-HKを上昇させてフェリチン内に鉄を閉じ込めフェロトーシスを阻害するのです。これにより脂肪はフェロトーシスを標的とする薬剤に対する耐性を助けるだけでなく、免疫系やチェックポイント阻害剤による破壊力も弱めます。キヌレニン–3-HK–フェリチン軸を、たとえばIDO1/TDO2の併用阻害で断つことにより、臨床医はこの保護シールドを取り除き、脂肪に埋もれたがんを免疫療法や他の治療に対してより反応性の高いものにできる可能性があります。
引用: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
キーワード: 腫瘍微小環境, フェロトーシス, キヌレニン経路, 腫瘍周囲脂肪組織, がん免疫療法