Clear Sky Science · tr
Tümör çevresi yağ dokusu, ferritinofajiyi 3‑hidroksikinurenin aracılı baskılayarak ferroptozise direnç kazandırır
Tümör Çevresindeki Yağ: Gizli Bir Koruyucu
Birçok kanser yumuşak, süngerimsi yağ dokusuyla yakın temas halinde büyür. Pasif bir gözlemci olmaktan uzak olan bu yakın yağ, tümörlerin hem kemoterapiye hem de modern immünoterapilere karşı gizlice hayatta kalmasına yardım edebilir. Bu çalışma, tümörleri çevreleyen yağın kanser hücreleri içinde demir kaynaklı bir hücre ölüm türünü nasıl engellediğine dair şaşırtıcı bir mekanizmayı açığa çıkarıyor ve bu kalkanın bozulmasının özellikle yağlı yüzeylere yayılan karın kanserlerinde mevcut tedavileri nasıl daha etkili kılabileceğini gösteriyor.
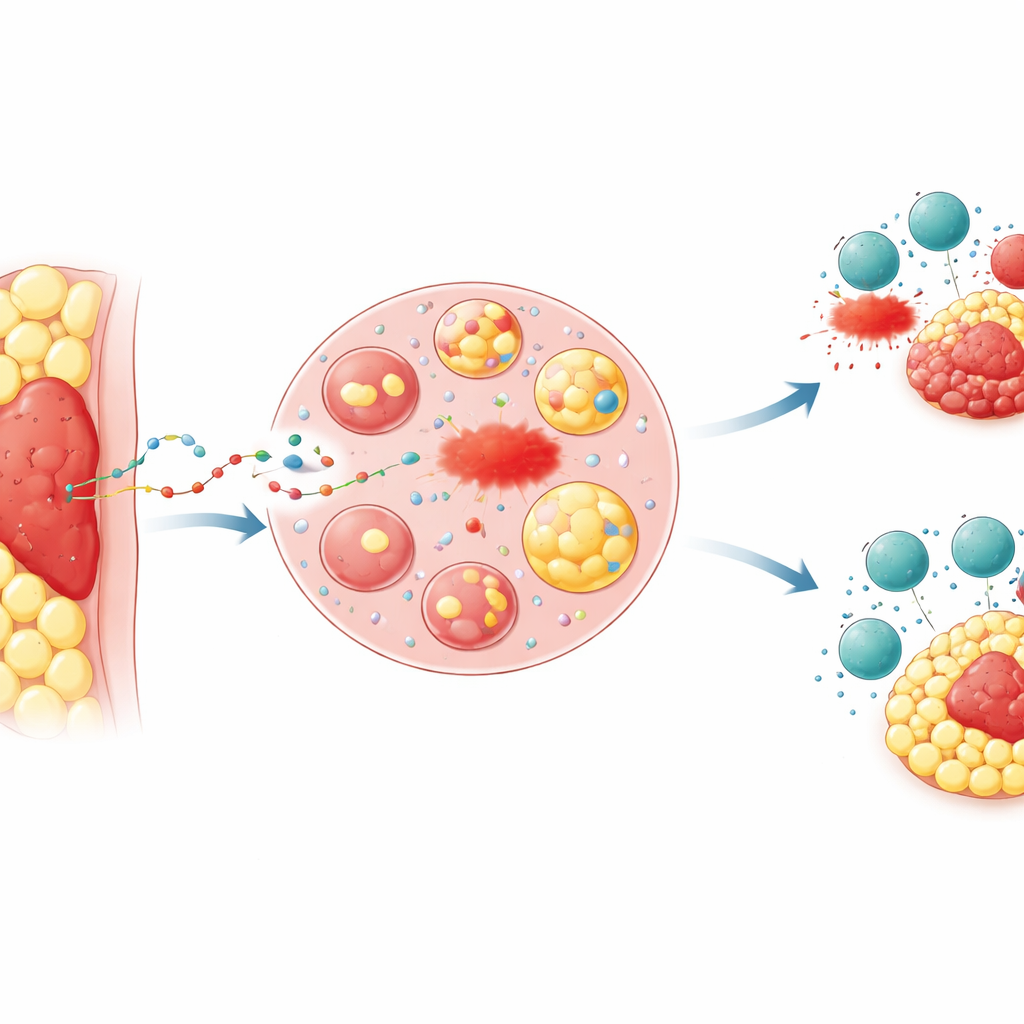
Konumun Tümörlere Sağladığı Avantaj
Hekimler uzun zamandır, karın zarı gibi yağ dokusu içinde gömülü tümörlerin —örneğin ilerlemiş kolon ve mide kanserlerinin— genellikle tedaviye kötü yanıt verdiğini ve daha kötü sonuçlara yol açtığını gözlemlemişlerdir. Araştırmacılar, tümörü çevreleyen hemen yanındaki yağ halkası olan “tümör çevresi adipöz doku”ya odaklandı. Fare modellerinde aynı kanser hücrelerini ya az yağ olan deri altına ya da doğrudan bir yağ yastığına naklettiler. Yağ içine gömülü tümörler daha hızlı büyüdü, ferroptozis adı verilen bir hücre ölümünü tetikleyen ilaçlarla öldürülmesi daha zor oldu ve öldürücü T hücreleri veya anti‑PD‑1 immünoterapisine daha az duyarlıydı. Ferroptozisin gerçekleştiğine işaret eden lipid hasarı kimyasal belirteçleri, yağ içinde büyüyen tümörlerde çok daha düşüktü; bu durum, ileri evre kolorektal ve gastrik kanserli hastalardan alınan doku örneklerindeki desenleri yansıtıyordu.
Kanser Hücreleri İçindeki Demir Kilit Kutuları
Ferroptozis, serbest demire bağlıdır; yeterli demir bulunduğunda hücre zarlarının kontrolsüz oksidasyonunu hızlandırarak hücreyi öldürür. Kanser hücreleri bu tehdidi ferritin adı verilen protein kabukların içinde demiri depolayarak tamponlayabilir. Araştırmacılar, yakın yağın tümör demir yönetimini bir şekilde yeniden programlayıp programlamadığını sordular. İnsan ve fare yağ dokusundan elde edilen sıvıda kanser hücrelerini yetiştirdiler ve bu “şartlandırılmış” ortamın hücreleri belirgin şekilde ferroptozise daha dirençli hale getirdiğini buldular. Proteomik profilleme, diğer bilinen ferroptozis düzenleyicilerinde büyük değişiklikler olmaksızın ana ferritin alt birimlerinin her ikisinde de güçlü bir artış ortaya koydu. Aynı zamanda hücre içindeki serbest demir havuzu aslında azaldı. Araştırmacılar ferritini susturduklarında, yağ kaynaklı ortamın koruyucu etkisi ortadan kalktı ve yağ bakımından zengin bölgelerdeki tümörler daha küçük oldu ve demir kaynaklı hasara karşı daha duyarlı hale geldi.
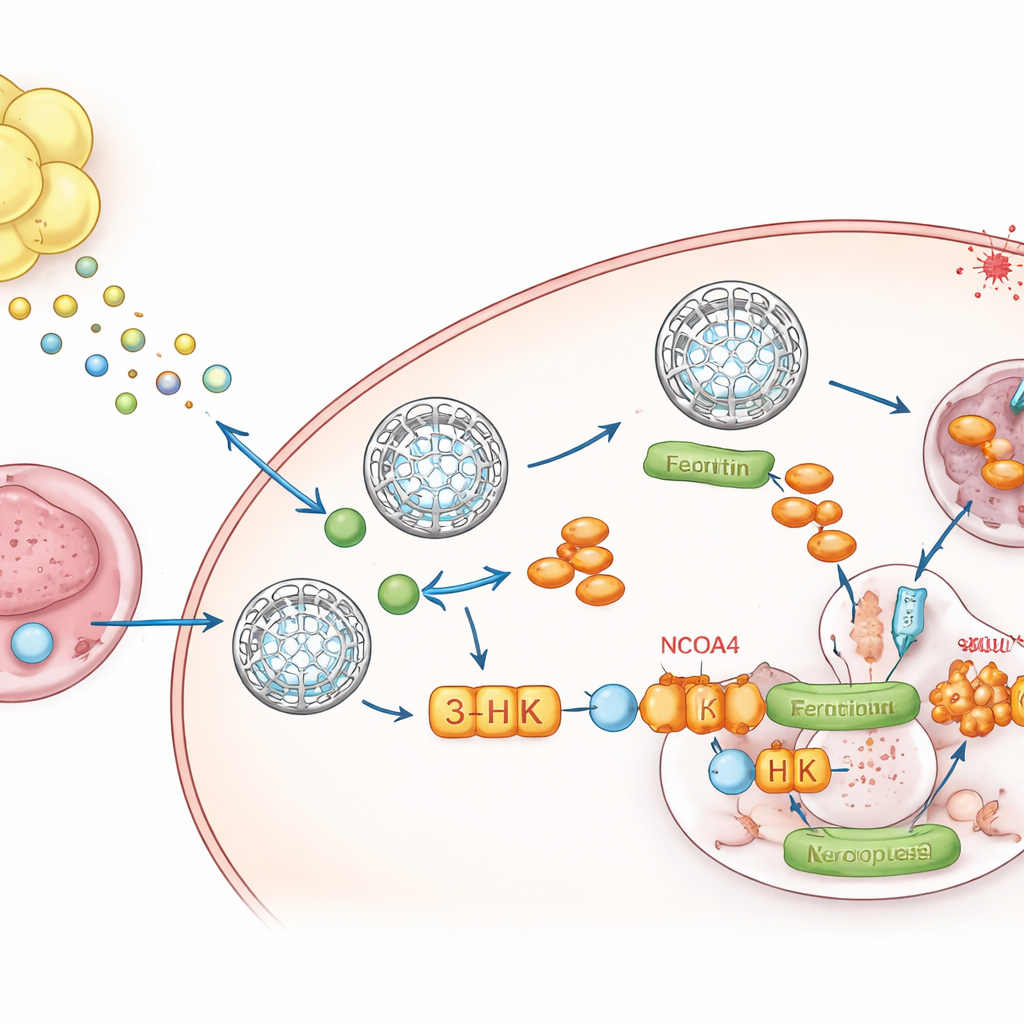
Yağdan Tümöre Metabolik Bir Haberci
Yağın ne gönderdiğini belirlemek için ekip küçük moleküllerin taraması olan metabolomik analizine yöneldi. Bir bileşik, aminoasit triptofanın yıkım ürünü olan kinurenin, yağ şartlandırılmış ortamlarda ve yağ içinde büyüyen tümörlerde sürekli olarak yükseldiği biçimde öne çıktı. Bu tümörleri yıkayan sıvı, yüksek kinurenin ve düşük triptofana sahipti; bu, yerel ortamın yeniden programlandığını gösteriyordu. Çevreleyen yağ, kinurenini üreten IDO1 ve TDO2 enzimlerini yüksek düzeyde ifade ediyordu ve tek çekirdek RNA dizilemesi, adipositler ve onların öncül hücrelerinin ana kaynaklar olduğunu gösterdi. Kanser hücreleri kinurenine maruz kaldığında ferritin seviyelerini artırdı, serbest demiri düşürdü ve ferroptozise direnç kazandı. Yağdaki IDO1 ve TDO2’yi bloke etmek, kinurenin eklenmediği sürece bu ferritin artışını ortadan kaldırdı.
Demir Salınım Vanasını Engelleyen Tek Bir Molekül
Kinurenin tek başına hareket etmez. Tümör hücreleri içinde bir yol boyunca birkaç metabolite dönüştürülür. Yazarlar bireysel adımları seçici olarak engelleyerek, bir ara ürün olan 3‑hidroksikinurenin (3‑HK) kilit oyuncu olduğunu keşfettiler. 3‑HK, düşük dozlarda bile ferritini stabilize etti, demir salınımını azalttı ve hücreleri ferroptozisten güçlü şekilde korudu. Mekanistik olarak, 3‑HK doğrudan NCOA4 adlı bir proteine bağlandı; NCOA4 normalde ferritini hücresel “geri dönüşüm merkezlerine” götürür, burada ferritin parçalanır ve demir serbest bırakılır. Yapısal ve biyofiziksel deneyler, 3‑HK’nin NCOA4’e tutunup onun ferritinle kenetlenmesini engellediğini, böylece bu demir kilit kutularını yerinde dondurduğunu ve ferroptozisin ateşlenmesi için gereken metali kıstığını gösterdi. NCOA4 kaldırıldığında, 3‑HK artık ferritini yükseltemedi veya hücreleri ferroptotik ölümden koruyamadı.
Kalkanı Terapötik Bir Hedefe Çevirmek
Kanser hücrelerinin ferroptotik ölümü antitümör bağışıklığı güçlendirebildiği için, yağ kaynaklı 3‑HK–ferritin yolu, peritoneal implantlar gibi yağ bakımından zengin metastazların neden sıklıkla immünoterapiye dirençli olduğuna dair bir açıklama sunar. Birden çok fare modelinde, IDO1 ve TDO2’nin eşzamanlı inhibisyonu tümör–yağ nişindeki kinurenin ve 3‑HK düzeylerini düşürdü, ferritin birikimini azalttı ve tümörleri ferroptozis indükleyicilere karşı çok daha kırılgan hale getirdi. En çarpıcı olanı, IDO1/TDO2 inhibitörlerini anti‑PD‑1 antikorlarıyla birleştirmenin tümör kontrolünü çok daha güçlü hale getirmesi, peritoneal metastaz modellerinde dahi belirgin fayda sağlamasıydı; bu yarar ferroptozis kimyasal olarak bloke edildiğinde kayboldu. Hasta verileri bu bulguları destekledi: peritoneal metastazlar primer tümörlere göre daha yüksek ferritin ve daha düşük lipid hasarı gösterdi ve bol 3‑HK’yi öngören gen imzaları daha ileri hastalık ve daha kötü sağkalım ile koreleydi.
Gelecekteki Kanser Bakımı İçin Anlamı
Bu çalışma, çevreleyen adipöz dokunun kinurenin ürettiği, bunu kanser hücrelerine verdiği ve böylece ferritin içinde demiri kilitleyen ve ferroptozisi engelleyen 3‑HK düzeylerini yükselttiği, yağ ile tümör arasında önce bilinmeyen bir iletişimi açığa çıkarıyor. Bu süreçle yağ, yalnızca ferroptozisi hedefleyen ilaçlara karşı tümörlerin dayanmasına yardımcı olmakla kalmaz, aynı zamanda bağışıklık sistemi ve kontrol noktası inhibitörlerinin onları yok etme yeteneğini de köreltir. Bu kinurenin–3‑HK–ferritin eksenini, örneğin kombine IDO1/TDO2 inhibitörleriyle kesintiye uğratarak, klinisyenler bu koruyucu kalkanı soyabilir ve yağ içine gömülü kanserleri immünoterapi ve diğer tedavilere karşı çok daha duyarlı hale getirebilirler.
Atıf: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Anahtar kelimeler: tümör mikroçevresi, ferroptozis, kinurenin yolu, tümör çevresi yağ dokusu, kanser immünoterapi