Clear Sky Science · nl
Peritumoraal vetweefsel bevordert ferroptose‑resistentie via 3‑hydroxykynurenine‑gemedieerde remming van ferritinophagie
Vetcellen rond tumoren: een verborgen beschermer
Veel kankers groeien in nauw contact met zacht, kussenvormig vet. Dit nabije vet is geen passieve toeschouwer; het kan tumorcellen heimelijk helpen te overleven onder chemotherapie en moderne immunotherapieën. Deze studie onthult een verrassende manier waarop het vet rond tumoren een vorm van ijzer‑gedreven celdood in kankercellen blokkeert, en laat zien hoe het doorbreken van dit schild bestaande behandelingen effectiever zou kunnen maken, met name bij buikholtekankers die zich over vettige oppervlakken verspreiden.
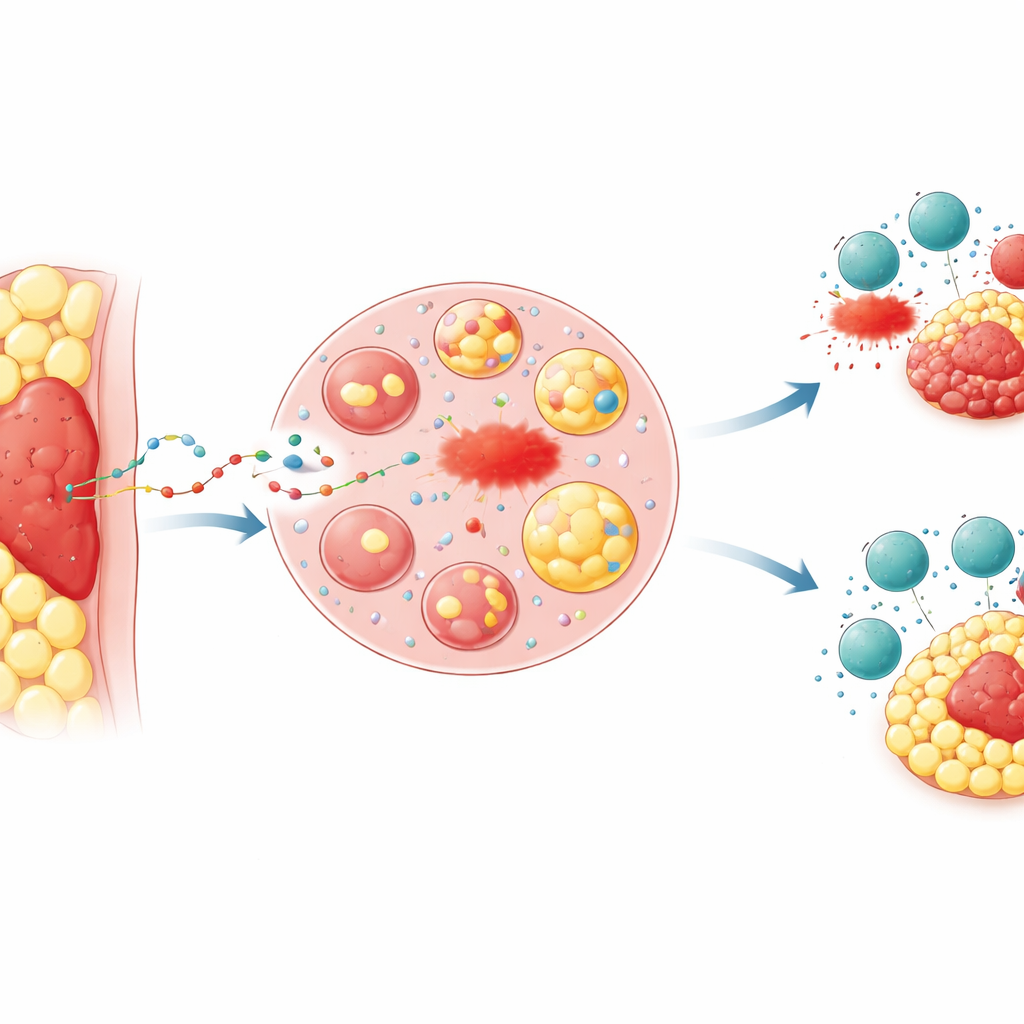
Wanneer locatie tumoren een voordeel geeft
Artsen merken al lang dat tumoren die in vet begraven liggen, zoals gevorderde colon‑ en maagkankers die het buikvlies binnenvallen, vaak slecht op behandeling reageren en tot slechtere uitkomsten leiden. De onderzoekers richtten zich op het “peritumoraal vetweefsel”—de ring van vet die direct een tumor omgeeft. In muismodellen implanteerden ze dezelfde kankercellen ofwel onder de huid, waar weinig vet aanwezig is, of direct in een vetkussen. Tumoren ingebed in vet groeiden sneller, waren moeilijker te doden met middelen die ferroptose opwekken, en waren minder gevoelig voor aanvallen door cytotoxische T‑cellen of voor anti‑PD‑1‑immunotherapie. Chemische merkers van lipidschade, die aangeven dat ferroptose optreedt, waren veel lager in vet‑ingesloten tumoren, wat overeenkomt met patronen gezien in weefselmonsters van patiënten met gevorderde colorectale en maagkanker.
IJzerkluisjes binnen kankercellen
Ferroptose hangt af van vrij ijzer; wanneer er genoeg ijzer beschikbaar is, bevordert het de runaway‑oxidatie van celmembranen en doodt het de cel. Kankercellen kunnen deze dreiging dempen door ijzer op te slaan in eiwitomhulsels die ferritine heten. Het team vroeg zich af of het nabije vet op de een of andere manier de ijzerhuishouding van tumoren herschakelt. Ze lieten kankercellen groeien in vloeistof afkomstig van menselijk en muisvetweefsel en ontdekten dat dit “geconditioneerde” medium de cellen duidelijk resistenter maakte tegen ferroptose. Proteomische profilering toonde een sterke toename van beide hoofdsubunits van ferritine, zonder grote veranderingen in andere bekende ferroptoseregulatoren. Tegelijkertijd daalde de hoeveelheid vrij ijzer in de cellen. Wanneer de onderzoekers ferritine uitschakelden, verdween het beschermende effect van het vetafgeleide medium, en werden tumoren in vetrijke locaties kleiner en gevoeliger voor ijzer‑gedreven schade.
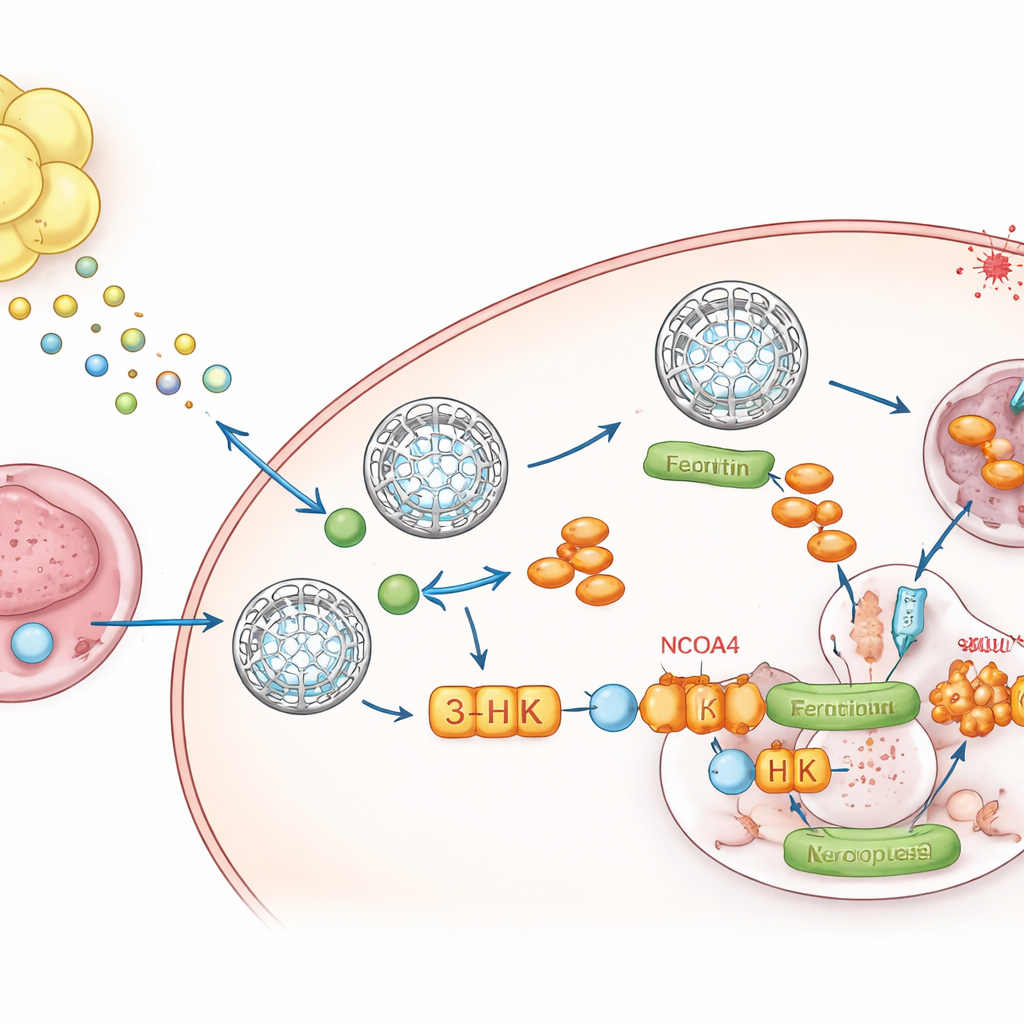
Een metabole boodschapper van vet naar tumor
Om te achterhalen wat het vet uitstuurde, gingen de onderzoekers naar metabolomics, een inventarisatie van kleine moleculen. Eén verbinding, kynurenine, een afbraakproduct van het aminozuur tryptofaan, viel op doordat deze consequent verhoogd was in vet‑geconditioneerd medium en in tumoren die in vet groeiden. De vloeistof die deze tumoren omspoelde bevatte veel kynurenine en weinig tryptofaan, wat aantoont dat de lokale omgeving herschikt is. Het omgevende vet drukte hoge niveaus uit van de enzymen IDO1 en TDO2 die kynurenine maken, en single‑nucleus RNA‑sequencing toonde dat adipocyten en hun voorlopercellen de belangrijkste bronnen waren. Wanneer kankercellen aan kynurenine werden blootgesteld, verhoogden ze ferritineniveaus, verlaagden ze vrij ijzer en weerstonden ze ferroptose. Het blokkeren van IDO1 en TDO2 in vet maakte deze ferritine‑toename ongedaan, tenzij kynurenine werd teruggegeven.
Een enkel molecuul dat het ijzer‑ontgassingsventiel blokkeert
Kynurenine werkt niet alleen. Binnen tumorcellen wordt het langs een route omgezet in verschillende metabolieten. Door selectief individuele stappen te blokkeren ontdekten de auteurs dat één tussenproduct, 3‑hydroxykynurenine (3‑HK), de sleutelspeler is. 3‑HK stabiliseerde ferritine, verminderde ijzerafgifte en beschermde cellen sterk tegen ferroptose, zelfs bij lage doses. Mechanistisch bond 3‑HK zich direct aan een eiwit genaamd NCOA4, dat normaal gezien ferritine escorteert naar cellulaire “recyclingcentra” waar het wordt afgebroken en ijzer wordt vrijgegeven. Structurele en biofysische experimenten toonden aan dat 3‑HK zich vastklampt aan NCOA4 en verhindert dat dit eiwit aan ferritine andockt, waardoor deze ijzerkluisjes effectief bevroren blijven en ferroptose de metalen brandstof ontbreekt die het nodig heeft om te ontbranden. Wanneer NCOA4 werd verwijderd, kon 3‑HK ferritine niet meer verhogen of cellen tegen ferroptotische dood verdedigen.
Het schild omzetten in een therapeutisch doelwit
Aangezien ferroptotische dood van kankercellen de antitumorale immuniteit kan versterken, biedt de door vet aangedreven 3‑HK–ferritine‑route een verklaring waarom vetrijke metastasen, zoals peritoneale implantaten van colon‑ of maagkanker, vaak resistent zijn tegen immunotherapie. In meerdere muismodellen verlaagde dubbele remming van IDO1 en TDO2 kynurenine en 3‑HK in de tumor‑vet‑nis, verminderde ferritine‑ophoping en maakte tumoren veel kwetsbaarder voor ferroptose‑inductoren. Het meest opvallend was dat het combineren van IDO1/TDO2‑remmers met anti‑PD‑1‑antistoffen tot veel betere tumorcontrole leidde, ook in peritoneale metastasemodellen, en dit voordeel verdween wanneer ferroptose chemisch werd geblokkeerd. Patiëntgegevens ondersteunden deze bevindingen: peritoneale metastasen vertoonden hogere ferritine en minder lipideschade dan primaire tumoren, en genexpressieprofielen die veel 3‑HK voorspelden correleerden met meer gevorderde ziekte en slechtere overleving.
Wat dit betekent voor toekomstige kankerzorg
Dit werk onthult een eerder verborgen wisselwerking tussen vet en tumor waarbij het omgevende adipose weefsel kynurenine vervaardigt, het aan kankercellen levert en daardoor 3‑HK‑niveaus verhoogt die ijzer binnen ferritine opsluiten en ferroptose blokkeren. Daarmee helpt vet niet alleen tumoren bestand te zijn tegen ferroptose‑gerichte middelen, maar dempt het ook het vermogen van het immuunsysteem en checkpointremmers om ze te vernietigen. Door deze kynurenine–3‑HK–ferritine‑as te onderbreken, bijvoorbeeld met gecombineerde IDO1/TDO2‑remmers, zouden clinici dit beschermende schild kunnen wegnemen en vet‑ingesloten kankers veel beter gevoelig kunnen maken voor immunotherapie en andere behandelingen.
Bronvermelding: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Trefwoorden: tumormicro‑omgeving, ferroptose, kynurenine‑route, peritumoraal vetweefsel, kankerimmunotherapie