Clear Sky Science · ru
Периопухолевая жировая ткань способствует устойчивости к ферроптозу за счёт подавления ферритинофагии медиатором 3‑гидроксикинуренином
Жир вокруг опухолей: скрытый защитник
Многие виды рака развиваются в тесном контакте с мягкой, упругой жировой тканью. Эта окружающая ткань далеко не безучастна: она может тайно помогать опухолям выживать при химиотерапии и современных иммунотерапевтических подходах. В работе выявлен неожиданный механизм, с помощью которого жир вокруг опухоли блокирует внутри раковых клеток тип клеточной гибели, зависящий от железа, и показано, как разрушение этой защиты может повысить эффективность существующих терапий, особенно при опухолях в брюшной полости, распространяющихся по жировым поверхностям.
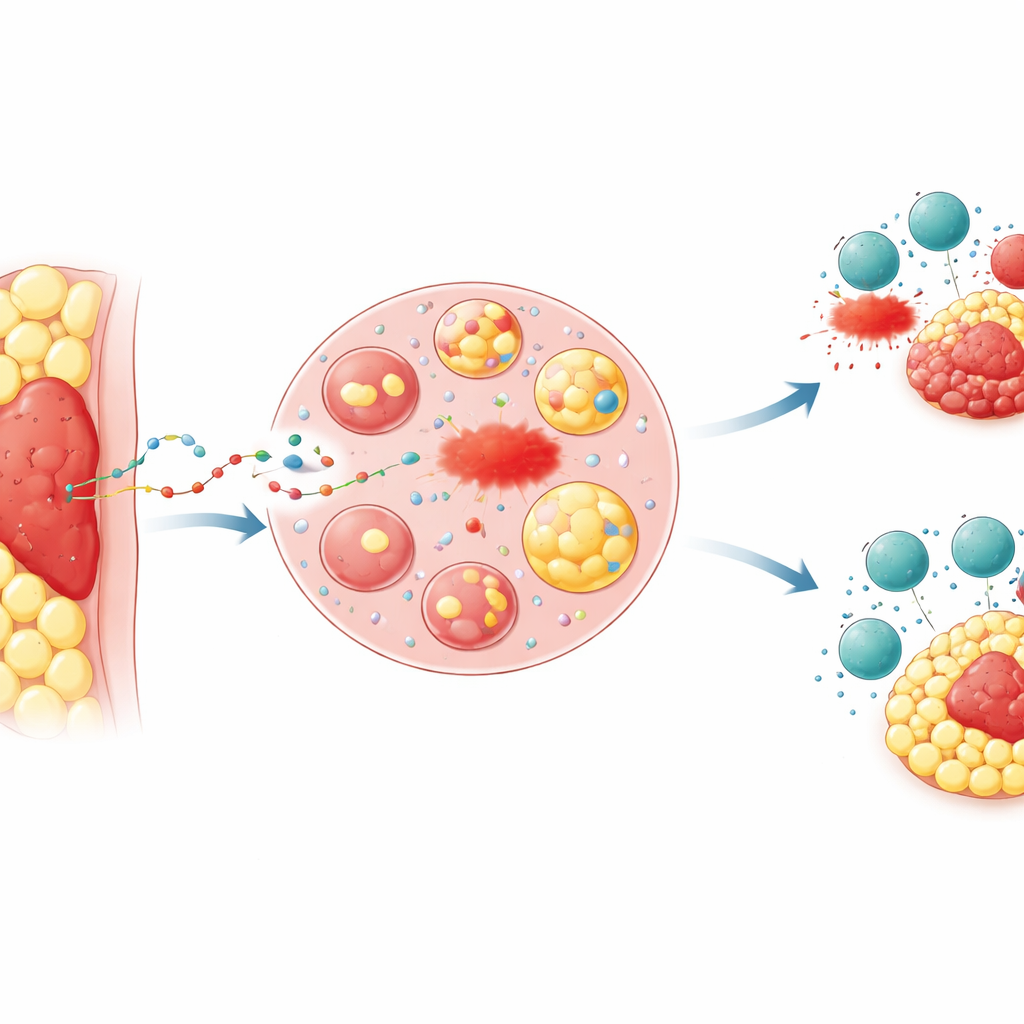
Когда местоположение даёт опухоли преимущество
Врачи давно замечают, что опухоли, погружённые в жир — например, распространённые колоректальные и желудочные раки, прорастающие брюшину — часто хуже реагируют на лечение и сопровождаются худшим прогнозом. Исследователи сосредоточились на «периопухолевой жировой ткани» — кольце жира непосредственно вокруг опухоли. В моделях на мышах те же раковые клетки имплантировали либо под кожу, где жира мало, либо прямо в жировой депо. Опухоли, укоренённые в жировой ткани, росли быстрее, были труднее уничтожаемы препаратами, индуцирующими ферроптоз, и хуже подвергались атаке со стороны киллерных Т‑клеток и терапии анти‑PD‑1. Химические маркеры повреждения липидов, указывающие на протекание ферроптоза, были значительно ниже в опухолях, размещённых в жире, что соответствовало образцам тканей пациентов с продвинутыми колоректальным и желудочным раком.
Железные «сейфы» внутри раковых клеток
Ферроптоз зависит от доступного свободного железа; при достаточном его количестве запускается лавинообразная окислительная порча мембран, приводящая к гибели клетки. Раковые клетки могут нейтрализовать эту угрозу, запасая железо внутри белковых оболочек — ферритина. Исследователи проверили, не перенастраивает ли окружающий жир обращение с железом в опухоли. Они выращивали раковые клетки в кондиционированной среде, полученной из человеческой и мышиной жировой ткани, и обнаружили, что такая среда делает клетки заметно более устойчивыми к ферроптозу. Протеомный профиль показал сильное увеличение обеих основных субъединиц ферритина при отсутствии значимых изменений других известных регуляторов ферроптоза. При этом пул свободного внутриклеточного железа фактически уменьшился. При уменьшении экспрессии ферритина защитный эффект среды, полученной из жира, исчезал, а опухоли в жировых участках становились меньше и более чувствительными к повреждению, опосредованному железом.
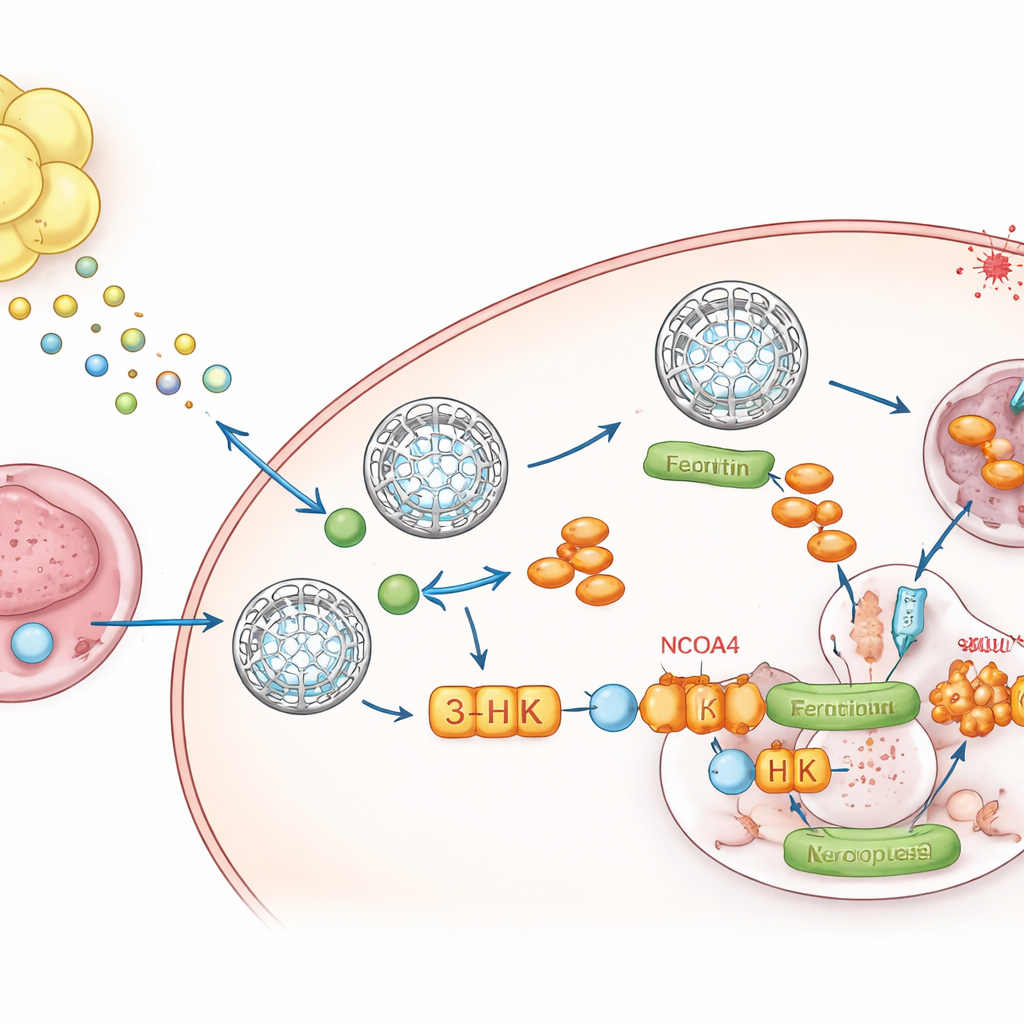
Метаболический вестник от жира к опухоли
Чтобы выяснить, что именно секретирует жир, группа обратилась к метаболомике — анализу малых молекул. Одно соединение, кинуренин, продукт распада аминокислоты триптофана, постоянно выделялось в кондиционированной среде и в опухолях, растущих в жире. Жидкость, окружающая эти опухоли, содержала много кинуренина и мало триптофана, что свидетельствует о местной перестройке метаболизма. Окружающая жировая ткань экспрессировала высокие уровни энзимов IDO1 и TDO2, синтезирующих кинуренин, а одиночное ядерное РНК‑секвенирование показало, что адипоциты и их предшественники являются основными источниками. При воздействии кинуренина раковые клетки увеличивали уровень ферритина, снижали свободное железо и становились устойчивыми к ферроптозу. Блокада IDO1 и TDO2 в жире подавляла этот рост ферритина, если только кинуренин не вводили обратно.
Одна молекула, блокирующая клапан выхода железа
Кинуренин действует не в одиночку. Внутри опухолевых клеток он превращается в ряд метаболитов. Селективно блокируя отдельные этапы пути, авторы выявили ключевой промежуточный продукт — 3‑гидроксикинуренин (3‑ГК). Даже в низких дозах 3‑ГК стабилизировал ферритин, снижал высвобождение железа и сильно защищал клетки от ферроптоза. Механистически 3‑ГК связывался непосредственно с белком NCOA4, который обычно доставляет ферритин в клеточные «перерабатывающие центры», где тот расщепляется и освобождается железо. Структурные и биофизические эксперименты показали, что 3‑ГК «пристыковывается» к NCOA4 и мешает его взаимодействию с ферритином, эффективно замораживая эти железные «сейфы» и лишая ферроптоз металла, необходимого для запуска. При удалении NCOA4 3‑ГК уже не мог повышать уровень ферритина и защищать клетки от ферроптотической гибели.
Преобразование защиты в терапевтическую мишень
Поскольку ферроптотическая гибель раковых клеток может усиливать антиопухолевый иммунитет, путь 3‑ГК–ферритин, индуцируемый жиром, объясняет, почему метастазы, богатые жиром — например, перитонеальные импланты при колоректальном или желудочном раке — часто устойчивы к иммунотерапии. В нескольких моделях на мышах двойная ингибиция IDO1 и TDO2 снижала уровни кинуренина и 3‑ГК в нише опухоль–жир, уменьшала накопление ферритина и делала опухоли гораздо более уязвимыми к индуктам ферроптоза. Наиболее впечатляюще, сочетание ингибиторов IDO1/TDO2 с антителами анти‑PD‑1 обеспечивало значительно лучшее подавление опухоли, в том числе в моделях перитонеальных метастаз, и этот эффект исчезал при химическом блокировании ферроптоза. Клинические данные поддерживали эти наблюдения: перитонеальные метастазы демонстрировали более высокий уровень ферритина и меньшее повреждение липидов по сравнению с первичными опухолями, а генетические подписи, предсказывающие обилие 3‑ГК, коррелировали с более продвинутой стадией болезни и худшей выживаемостью.
Что это значит для будущего лечения рака
Эта работа раскрывает ранее скрытый диалог между жиром и опухолью: окружающая адипозная ткань синтезирует кинуренин, поставляет его в раковые клетки, где он преобразуется в 3‑ГК, который удерживает железо внутри ферритина и блокирует ферроптоз. Тем самым жир не только помогает опухолям противостоять препаратам, нацеленным на ферроптоз, но и ослабляет способность иммунной системы и ингибиторов контрольных точек уничтожать их. Прерывание оси кинуренин–3‑ГК–ферритин, например сочетанной ингибиции IDO1/TDO2, может снять эту защиту и сделать опухоли, расположенные в жире, значительно более восприимчивыми к иммунотерапии и другим методам лечения.
Цитирование: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Ключевые слова: микроокружение опухоли, ферроптоз, путь кинуренина, периопухолевая жировая ткань, иммунотерапия рака