Clear Sky Science · ar
النسيج الدهني المحيط بالأورام يعزز مقاومة الفيروسوبتوزيس عبر قمع الفيريتينوفاجي بوساطة 3‑هيدروكسيكينورينين
الدهون حول الأورام: حامٍ خفي
تنمو العديد من الأورام على تماس وثيق مع نسيج دهني لين ومرن. وبعيدًا عن كونه متفرجًا سلبيًا، يمكن لهذه الدهون المجاورة أن تساعد الأورام سرًا على النجاة من كل من العلاج الكيميائي والعلاجات المناعية الحديثة. تكشف هذه الدراسة عن آلية مفاجئة عبرها يعوق النسيج الدهني المحيط نوعًا من موت الخلايا المعتمد على الحديد داخل الخلايا السرطانية، وتُبيّن كيف أن تعطيل هذا الدرع قد يجعل العلاجات الحالية أكثر فعالية، خصوصًا في السرطانات البطنية التي تنتشر على أسطح دهنية.
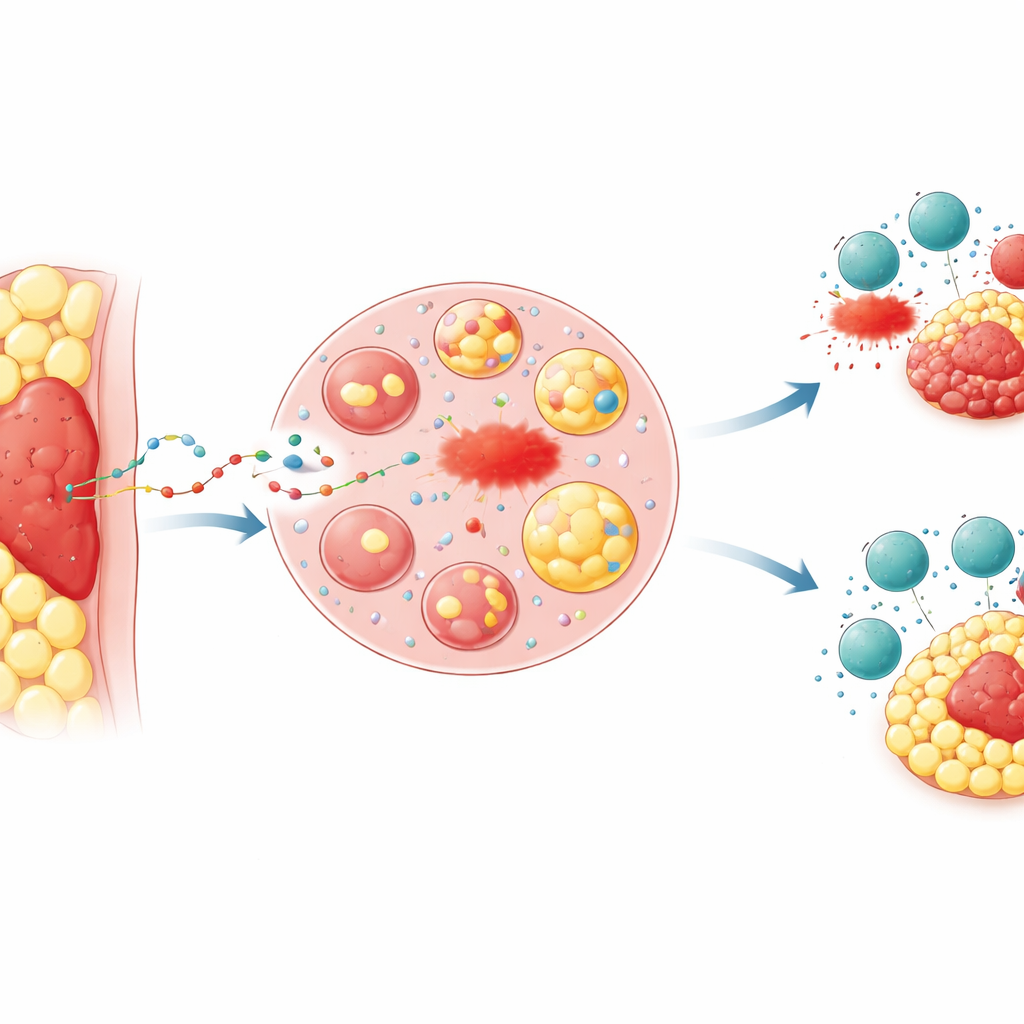
عندما يمنح الموقع ميزة للأورام
لاحظ الأطباء منذ زمن أن الأورام المطمورة داخل الدهون، مثل سرطانات القولون والمعدة المتقدمة التي تغزو البريتوان، غالبًا ما تستجيب للعلاج بشكل ضعيف وتؤدي إلى نتائج أسوأ. ركز الباحثون على "النسيج الدهني المحيط بالورم"—حلقة الدهون المحيطة مباشرة بالورم. في نماذج فئران، زرعوا نفس الخلايا السرطانية إما تحت الجلد حيث هناك دهون قليلة، أو مباشرة داخل وسادة دهنية. نمت الأورام المتربعة في الدهون أسرع، وكانت أصعب قتلًا بالأدوية التي تحفز شكلًا من أشكال موت الخلايا يدعى الفيروبتوزيس، وكانت أقل حساسية لهجوم الخلايا التائية القاتلة أو للعلاج المناعي المضاد لـ PD‑1. كانت مؤشرات التلف الدهني الكيميائية، التي تشير إلى حدوث الفيروبتوزيس، أقل بكثير في الأورام المدمجة بالدهون، مما يعكس أنماطًا شوهدت في عينات أنسجة من مرضى مصابين بسرطانات القولون والمعدة المتقدمة.
صناديق حديدية داخل الخلايا السرطانية
يعتمد الفيروبتوزيس على الحديد الحر؛ عندما يتوفر ما يكفي من الحديد، يساهم في تأكسد هائل لغشاء الخلايا يقتل الخلية. تستطيع الخلايا السرطانية مواجهة هذا التهديد بتخزين الحديد داخل أغلفة بروتينية تسمى فيريتين. تساءل الفريق عما إذا كان النسيج الدهني المجاور يعيد برمجة تعامل الورم مع الحديد. نَمَوا الخلايا السرطانية في وسط مستخلص من أنسجة دهنية بشرية وفأرية فوجدوا أن هذا الوسط "المشروط" جعل الخلايا أكثر مقاومة بكثير للفيروبتوزيس. كشف التحليل البروتيومي عن زيادة قوية في كلتا وحدتي الفريتين الرئيسيتين، دون تغييرات كبيرة في منظمات الفيروبتوزيس المعروفة الأخرى. في الوقت نفسه، انخفض مخزون الحديد الحر داخل الخلايا فعليًا. عندما خفض الباحثون تعبير الفريتين، زال التأثير الوقائي للوسط المشتق من الدهون، وأصبحت الأورام في مواقع غنية بالدهون أصغر وأكثر حساسية للأضرار المعتمدة على الحديد.
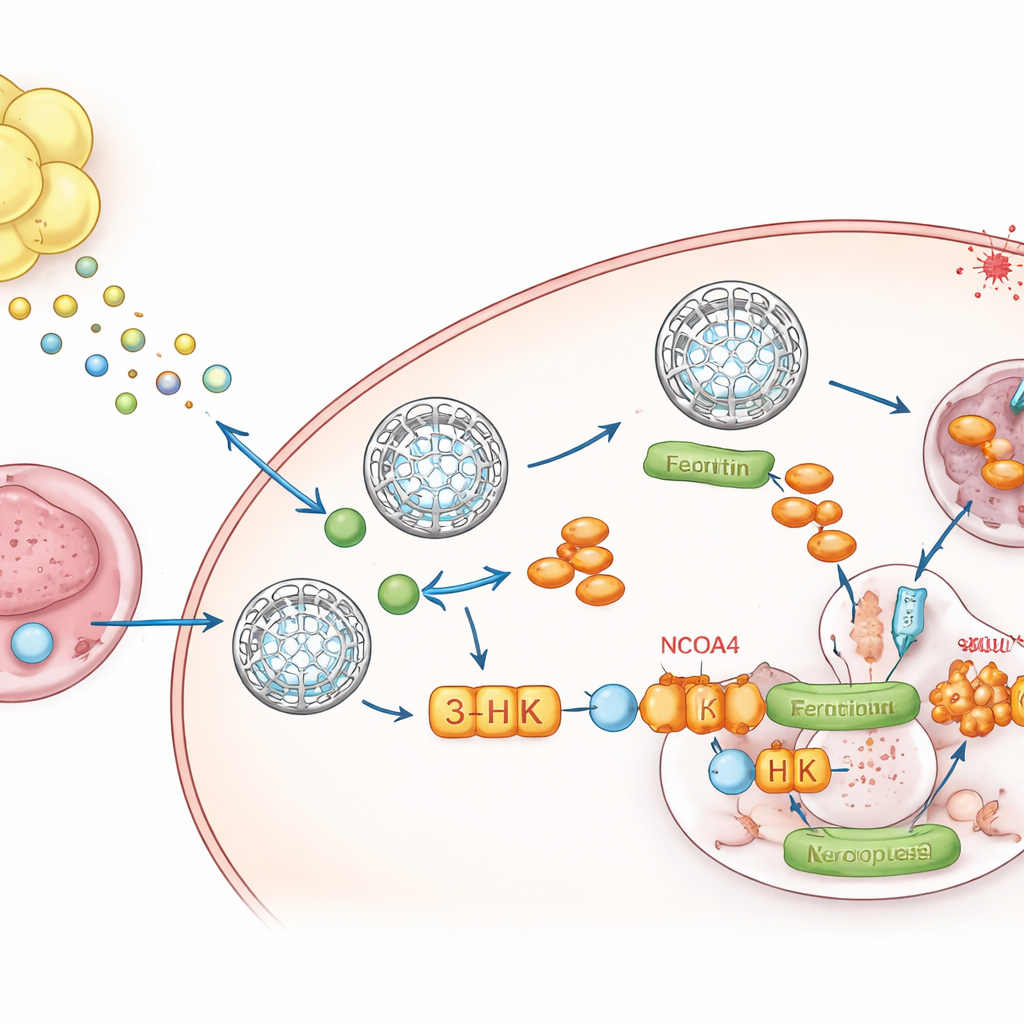
رسول أيضي من الدهون إلى الورم
لتحديد ما الذي ترسله الدهون، لجأ الفريق إلى علم الأيض الصغير الجزيئات، وهو مسح للجزيئات الصغيرة. برز مركب واحد، الكينورينين، ناتج تحلل الحمض الأميني تريبتوفان، باعتباره مرتفعًا باستمرار في الأوساط المشروطة بالدهن وفي الأورام التي تنمو داخل الدهون. كان السائل الذي يغمر هذه الأورام غنيًا بالكينورينين وفقيرًا بالتريبتوفان، ما يدل على أن البيئة المحلية مُعاد تهيئتها. عبرت الدهون المحيطة عن مستويات عالية من الإنزيمين IDO1 وTDO2 اللذين يصنعان الكينورينين، وأظهر تسلسل الرنا الوحيد النوى أن الخلايا الدهنية وخلاياها السلفية كانت المصادر الرئيسية. عندما تعرضت الخلايا السرطانية للكينورينين، زادت مستويات الفريتين، وانخفض الحديد الحر، ورفضت الخضوع للفيروبتوزيس. إيقاف IDO1 وTDO2 في الدهون ألغى هذه الزيادة في الفريتين ما لم يُعاد إدخال الكينورينين.
جزيء واحد يغلق صمام تحرير الحديد
الكينورينين لا يعمل وحيدًا. داخل الخلايا الورمية يُحول ضمن مسار إلى عدة مستقلبات. عبر حجب خطوات محددة، اكتشف المؤلفون أن أحد الوسائط، 3‑هيدروكسيكينورينين (3‑HK)، هو الفاعل الرئيسي. 3‑HK، حتى بجرعات منخفضة، ثبت الفريتين، وخفض تحرير الحديد، وحمى الخلايا بشدة من الفيروبتوزيس. من الناحية الميكانيكية، ارتبط 3‑HK مباشرة ببروتين يدعى NCOA4، الذي عادة ما يصطحب الفريتين إلى "مراكز إعادة التدوير" الخلوية حيث يكسر ويُطلق الحديد. أظهرت تجارب هيكلية وبيوفيزيائية أن 3‑HK يلتصق بـ NCOA4 ويمنعه من الالتحام مع الفريتين، مجمّدًا فعليًا هذه الصناديق الحديدية في مكانها ويجوع الفيروبتوزيس من المعدن اللازم لإشعاله. عندما أُزيل NCOA4، لم يعد بإمكان 3‑HK رفع الفريتين أو حماية الخلايا من موت الفيروبتوزيس.
تحويل الدرع إلى هدف علاجي
نظرًا لأن موت الفيروبتوزيس للخلايا السرطانية يمكن أن يعزز المناعة المضادة للورم، يقدم مسار 3‑HK‑الفريتين الذي تقوده الدهون تفسيرًا لسبب مقاومة النقائل الغنية بالدهون، مثل زوائد الصفاق من سرطانات القولون أو المعدة، للعلاجات المناعية. في نماذج فأرية متعددة، خفض التثبيط المزدوج لـ IDO1 وTDO2 الكينورينين و3‑HK في موضع الورم‑الدهون، وقلل تراكم الفريتين، وجعل الأورام أكثر عرضة بشكل كبير لمحفزات الفيروبتوزيس. والأكثر بروزًا، أن الجمع بين مثبطات IDO1/TDO2 والأجسام المضادة المضادة لـ PD‑1 أنتج تحكمًا أقوى بكثير في الورم، بما في ذلك في نماذج النقائل الصفاقية، وفقد هذا الفائدة عندما حُجب الفيروبتوزيس كيميائيًا. دعمت بيانات المرضى هذه النتائج: أظهرت النقائل الصفاقية فريتينًا أعلى وتلفًا دهنيًا أقل من الأورام الأولية، كما أن تواقيع جينية تتنبأ بوفرة 3‑HK ارتبطت بمرض أكثر تقدّمًا وببقاء أسوأ.
ماذا يعني هذا لرعاية السرطان المستقبلية
تكشف هذه الدراسة عن حوار خفي سابقًا بين الدهون والورم حيث يصنع النسيج الدهني المحيط الكينورينين، يزوده للخلايا السرطانية، وبالتالي يزيد مستويات 3‑HK التي تقفل الحديد داخل الفريتين وتعيق الفيروبتوزيس. وبهذا، لا تساعد الدهون الأورام على مقاومة الأدوية الموجهة نحو الفيروبتوزيس فحسب، بل تُضعف أيضًا قدرة الجهاز المناعي ومثبطات نقاط التفتيش على تدميرها. عبر قطع محور الكينورينين–3‑HK–الفريتين، على سبيل المثال بالمثبطات المشتركة لـ IDO1/TDO2، قد يصبح بإمكان الأطباء نزع هذا الدرع الواقي وجعل الأورام المغروسة في الدهون أكثر استجابة للعلاج المناعي وعلاجات أخرى.
الاستشهاد: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
الكلمات المفتاحية: بيئة الورم الدقيقة, الفيروبتوزيس, مسار الكينورينين, النسيج الدهني المحيط بالورم, مناعة السرطان العلاجية