Clear Sky Science · sv
Peritumoralt adipös vävnad främjar ferroptosresistens genom 3‑hydroxykynurenin‑medierad hämning av ferritinofagi
Fett runt tumörer: en dold beskyddare
Många cancerformer växer i nära kontakt med mjukt, vadderat fett. Långt ifrån att vara en passiv åskådare kan detta närliggande fett i hemlighet hjälpa tumörer att överleva både kemoterapi och moderna immunterapier. Denna studie avslöjar ett överraskande sätt på vilket fettet kring tumörer blockerar en järn‑driven form av celldöd i cancerceller, och visar hur störning av denna sköld skulle kunna göra befintliga behandlingar mer effektiva, särskilt vid bukcancerspridning över fettklädda ytor.
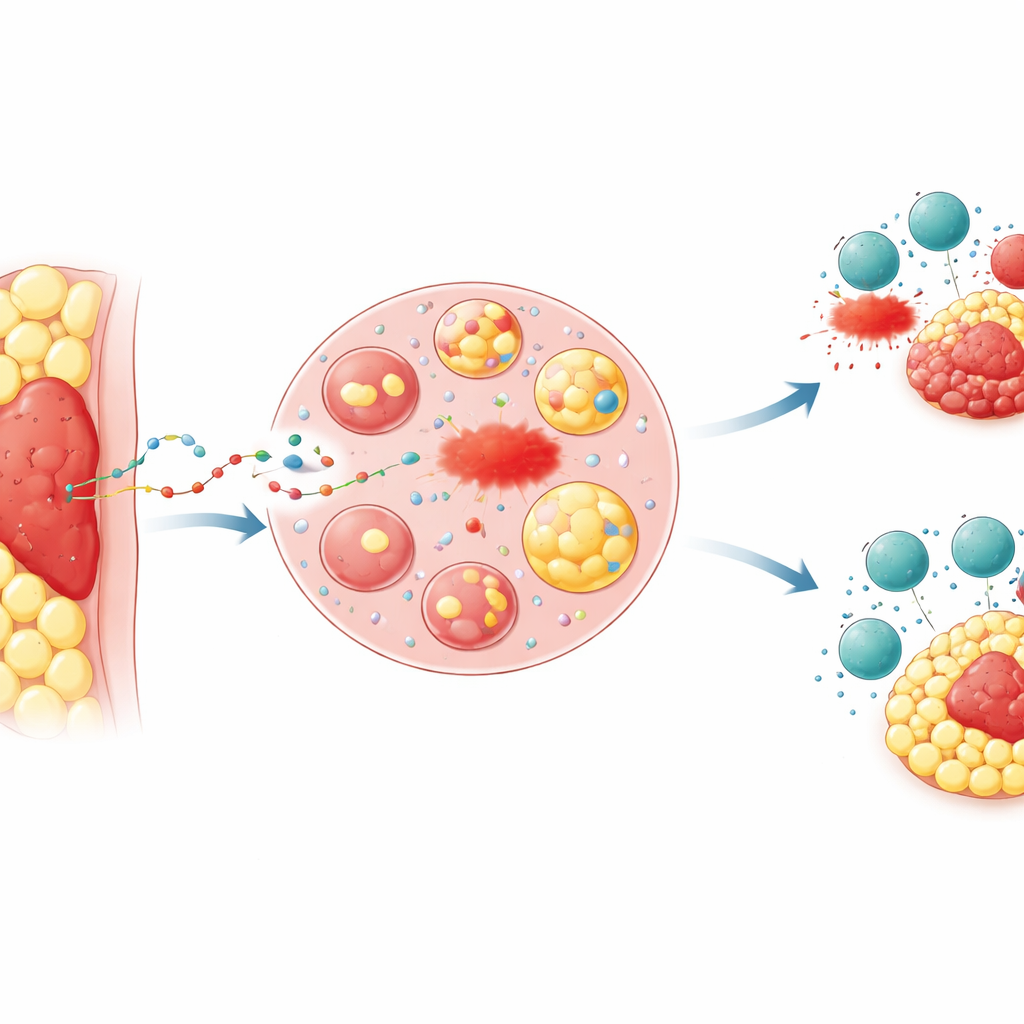
När läget ger tumörer fördel
Läkare har länge noterat att tumörer inbäddade i fett, såsom avancerade kolorektala och magsäckscancer som invaderar bukhinnan, ofta svarar dåligt på behandling och ger sämre utfall. Forskarna fokuserade på den ”peritumorala adipösa vävnaden” — ringen av fett som omedelbart omger en tumör. I musmodeller implanterade de samma cancerceller antingen under huden, där det finns lite fett, eller direkt i en fettkudde. Tumörer placerade i fett växte snabbare, var svårare att döda med läkemedel som utlöser en form av celldöd kallad ferroptos, och var mindre känsliga för T‑cellsbaserad immunattack eller anti‑PD‑1‑immunterapi. Kemiska markörer för lipid‑skador, som signalerar att ferroptos pågår, var mycket lägre i fettinbäddade tumörer, vilket speglade mönster som sågs i vävnadsprover från patienter med avancerad kolorektal och gastrisk cancer.
Järnlås inuti cancerceller
Ferroptos är beroende av fritt järn; när tillräckligt med järn finns tillgängligt driver det okontrollerad oxidation av cellmembran, vilket dödar cellen. Cancerceller kan dämpa detta hot genom att lagra järn inuti proteinskal kallade ferritin. Teamet undersökte om det omkringliggande fettet på något sätt omprogrammerade tumörernas järnhantering. De odlade cancerceller i vätska från mänsklig och musadipös vävnad och fann att detta ”konditionerade” medium gjorde cellerna märkbart mer motståndskraftiga mot ferroptos. Proteomprofilering visade en stark ökning av båda huvudsubenheterna i ferritin, utan större förändringar i andra kända ferroptosregulatorer. Samtidigt sjönk mängden fritt järn inne i cellerna. När forskarna sänkte ferritinnivåerna försvann det skyddande effekten från fett‑deriverat medium, och tumörer i fett‑rika miljöer blev mindre och mer känsliga för järn‑driven skada.
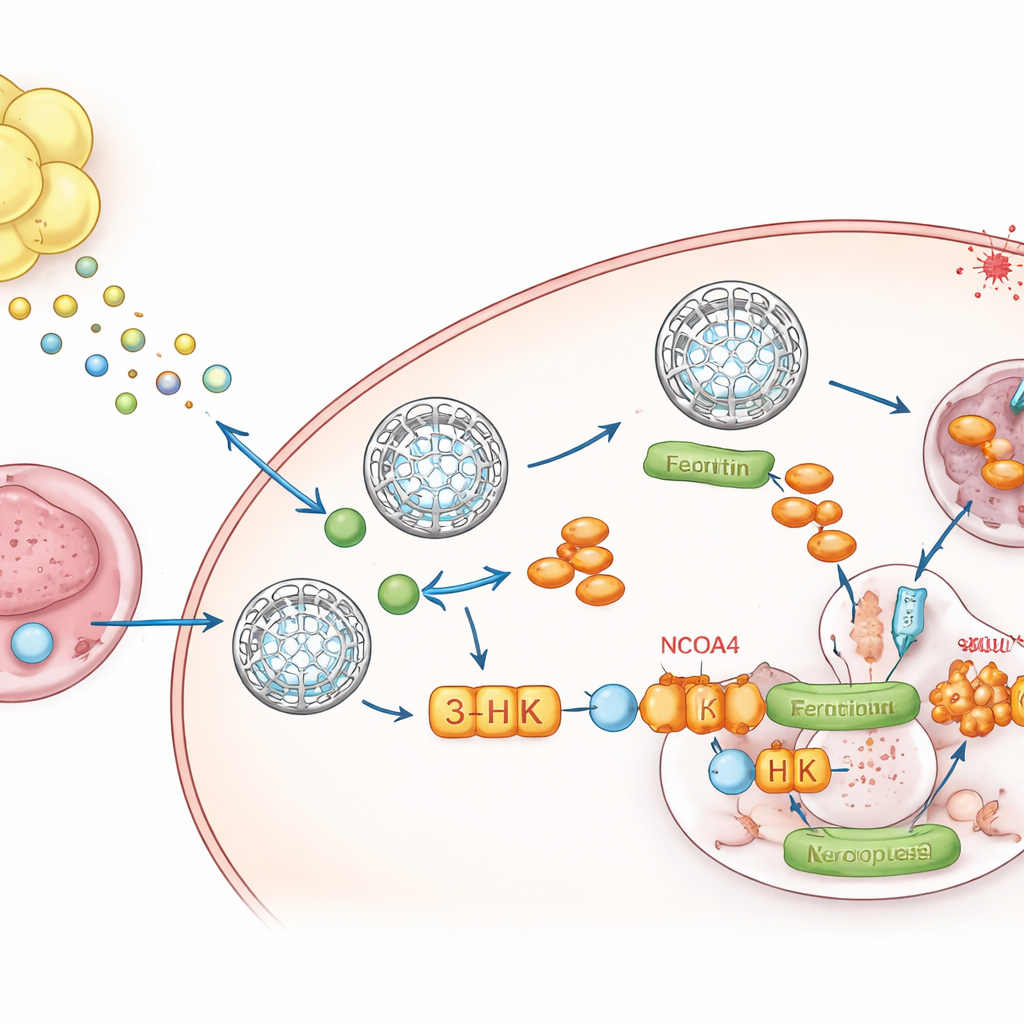
En metabolisk budbärare från fett till tumör
För att ta reda på vad fettet skickade vände teamet sig till metabolomik, en undersökning av små molekyler. En förening, kynurenin, en nedbrytningsprodukt av aminosyran tryptofan, framträdde som konsekvent förhöjd i fett‑konditionerade medier och i tumörer som växte i fett. Vätskan som ombad dessa tumörer innehöll mycket kynurenin och lite tryptofan, vilket visar att den lokala miljön är omprogrammerad. Det omgivande fettet uttryckte höga nivåer av enzymerna IDO1 och TDO2 som bildar kynurenin, och singelnukleär RNA‑sekvensering visade att adipocyter och deras prekursorceller var huvudkällorna. När cancerceller exponerades för kynurenin ökade de ferritinnivåerna, sänkte fritt järn och blev motståndskraftiga mot ferroptos. Blockering av IDO1 och TDO2 i fettet eliminerade denna ferritinstigning om inte kynurenin tillsattes igen.
En enda molekyl som blockerar järnets utlopp
Kynurenin agerar inte ensam. Inne i tumörceller omvandlas det längs en väg till flera metaboliter. Genom att selektivt blockera individuella steg upptäckte författarna att ett mellanled, 3‑hydroxykynurenin (3‑HK), är huvudaktören. 3‑HK, även i låga doser, stabiliserade ferritin, minskade järnfrisättning och skyddade kraftigt celler från ferroptos. Mekaniskt band 3‑HK direkt till ett protein kallat NCOA4, som normalt eskorterar ferritin till cellens ”återvinningscentraler” där det bryts ner och järn frigörs. Strukturella och biofysiska experiment visade att 3‑HK fäster vid NCOA4 och förhindrar dess dokning med ferritin, vilket effektivt fryser dessa järnlås på plats och berövar ferroptos metall den behöver för att tändas. När NCOA4 togs bort kunde 3‑HK inte längre höja ferritin eller försvara celler mot ferroptotisk död.
Att vända skölden till ett terapeutiskt mål
Där ferroptotisk död av cancerceller kan stärka antitumör immunitet erbjuder den fettdrivna 3‑HK–ferritin‑banan en förklaring till varför fett‑rika metastaser, såsom peritoneala implantat från kolon‑ eller magsäckscancer, ofta motstår immunterapi. I flera musmodeller sänkte dubbel hämmning av IDO1 och TDO2 kynurenin och 3‑HK i tumör‑fett‑nischen, minskade ferritinansamling och gjorde tumörerna mycket mer sårbara för ferroptos‑inducerare. Mest anmärkningsvärt gav kombinationen av IDO1/TDO2‑hämmare med anti‑PD‑1‑antikroppar långt starkare tumörkontroll, även i modeller för peritoneal metastas, och denna fördel försvann när ferroptos kemiskt blockerades. Patientdata stödde dessa fynd: peritoneala metastaser visade högre ferritin och lägre lipid‑skador än primärtumörer, och genuttryckssignaturer som förutsade rikliga 3‑HK‑nivåer korrelerade med mer avancerad sjukdom och sämre överlevnad.
Vad detta betyder för framtida cancervård
Detta arbete avslöjar en tidigare dold dialog mellan fett och tumör där den omgivande adipösa vävnaden tillverkar kynurenin, förser cancerceller med den, och därigenom höjer 3‑HK‑nivåerna som låser in järn i ferritin och blockerar ferroptos. Genom detta hjälper fettet inte bara tumörer att stå emot läkemedel som riktar sig mot ferroptos, utan försvagar också immunsystemets och checkpoint‑hämmarnas förmåga att förstöra dem. Genom att avbryta denna kynurenin–3‑HK–ferritin‑axel, till exempel med kombinerade IDO1/TDO2‑hämmare, kan kliniker potentiellt ta bort denna skyddande sköld och göra fettinbäddade cancerformer mycket mer mottagliga för immunterapi och andra behandlingar.
Citering: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Nyckelord: tumörmikromiljö, ferroptos, kynurenin‑väg, peritumoralt adipöst vävnad, cancerimmunterapi