Clear Sky Science · fr
Le tissu adipeux péri-tumoral favorise la résistance à la ferroptose par la suppression de la ferritinophagie médiée par la 3‑hydroxykynurénine
La graisse autour des tumeurs : un protecteur caché
De nombreux cancers se développent en contact direct avec du tissu adipeux moelleux. Loin d’être un simple spectateur, cette graisse voisine peut aider en secret les tumeurs à survivre à la fois à la chimiothérapie et aux immunothérapies modernes. Cette étude met au jour une manière surprenante par laquelle la graisse entourant les tumeurs bloque un type de mort cellulaire dépendant du fer à l’intérieur des cellules cancéreuses, et montre comment perturber ce bouclier pourrait améliorer l’efficacité des traitements existants, en particulier dans les cancers abdominaux qui se propagent sur des surfaces graisseuses.
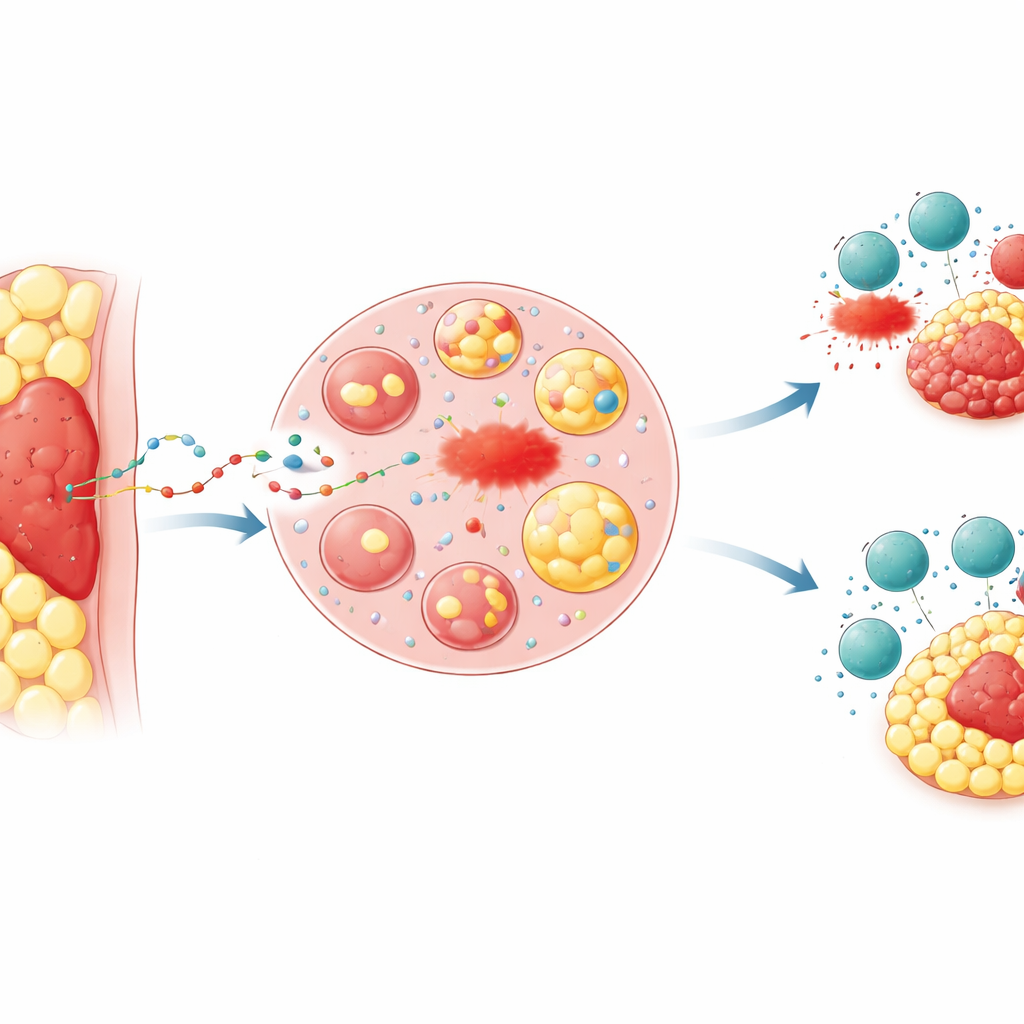
Quand l’emplacement donne un avantage aux tumeurs
Les cliniciens ont longtemps observé que les tumeurs enfouies dans la graisse, comme les cancers colorectaux et gastriques avancés qui envahissent le péritoine, répondent souvent mal au traitement et entraînent des pronostics plus mauvais. Les chercheurs se sont focalisés sur le « tissu adipeux péri‑tumoral » — l’anneau de graisse immédiatement entourant une tumeur. Chez la souris, ils ont implanté les mêmes cellules cancéreuses soit sous la peau, où la graisse est peu abondante, soit directement dans un dépôt adipeux. Les tumeurs nichées dans la graisse croissaient plus vite, étaient plus difficiles à détruire avec des médicaments induisant une forme de mort cellulaire appelée ferroptose, et étaient moins sensibles à l’attaque des lymphocytes T cytotoxiques ou à l’immunothérapie anti‑PD‑1. Les marqueurs chimiques des dommages lipidiques, qui indiquent la survenue de la ferroptose, étaient beaucoup plus faibles dans les tumeurs intégrées à la graisse, reflétant des profils observés sur des échantillons de patients atteints de cancers colorectaux et gastriques avancés.
Des coffres‑forts à fer à l’intérieur des cellules cancéreuses
La ferroptose dépend du fer libre ; lorsque suffisamment de fer est disponible, il favorise l’oxydation incontrôlée des membranes cellulaires, entraînant la mort de la cellule. Les cellules cancéreuses peuvent atténuer cette menace en stockant le fer à l’intérieur de coques protéiques appelées ferritines. L’équipe a cherché à savoir si la graisse voisine reprogrammait la gestion du fer par la tumeur. Ils ont cultivé des cellules cancéreuses dans le liquide conditionné provenant de tissu adipeux humain et murin et ont constaté que ce milieu « conditionné » rendait les cellules nettement plus résistantes à la ferroptose. Le profil protéomique a révélé une forte augmentation des deux principales sous‑unités de la ferritine, sans modifications majeures d’autres régulateurs connus de la ferroptose. Parallèlement, le pool de fer libre à l’intérieur des cellules a en réalité diminué. Lorsque les chercheurs ont réduit l’expression de la ferritine, l’effet protecteur du milieu dérivé de la graisse a disparu, et les tumeurs dans des sites riches en graisse sont devenues plus petites et plus sensibles aux dommages liés au fer.
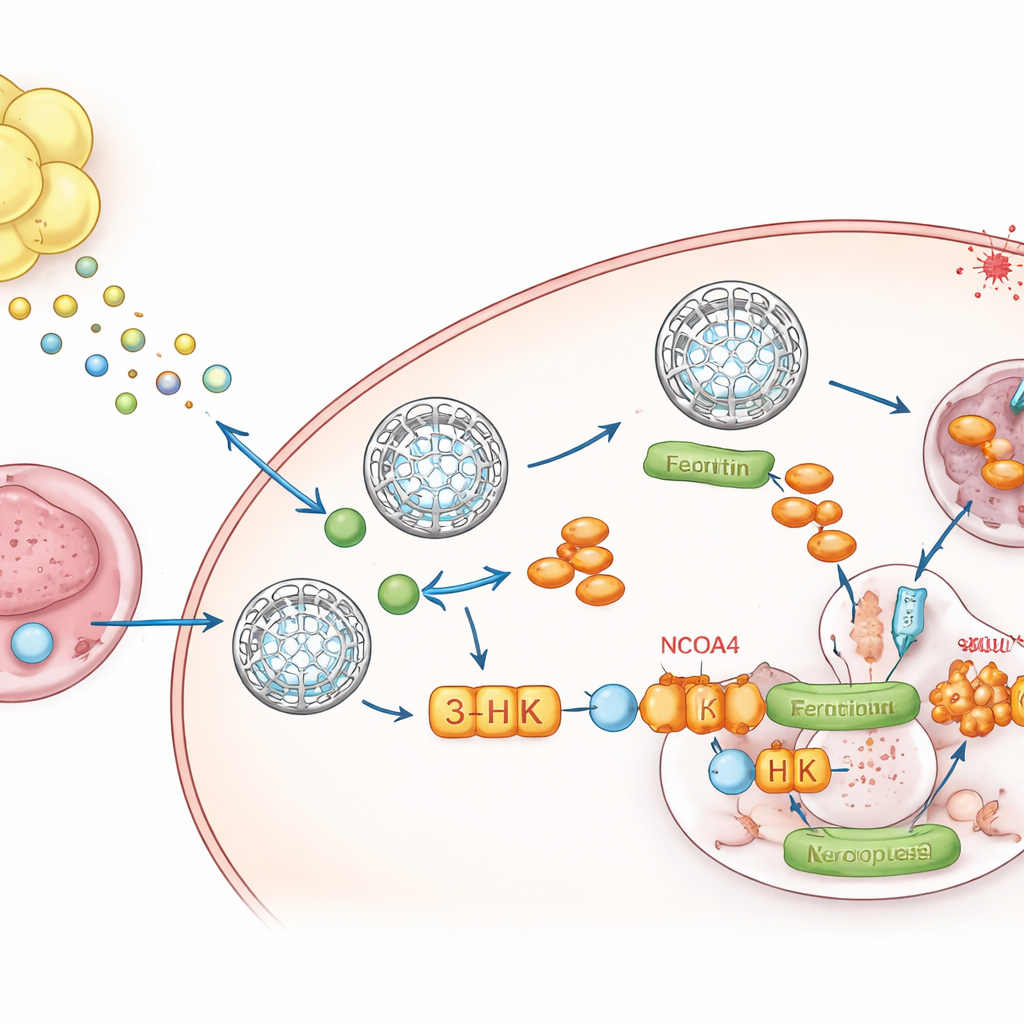
Un messager métabolique de la graisse vers la tumeur
Pour identifier ce que la graisse envoyait, l’équipe s’est tournée vers la métabolomique, une analyse des petites molécules. Un composé, la kynurénine, produit de dégradation de l’acide aminé tryptophane, est apparu comme systématiquement élevé dans les milieux conditionnés par la graisse et dans les tumeurs croissant au sein de la graisse. Le liquide entourant ces tumeurs contenait beaucoup de kynurénine et peu de tryptophane, montrant que l’environnement local est reprogrammé. Le tissu adipeux environnant exprimait des niveaux élevés des enzymes IDO1 et TDO2 qui synthétisent la kynurénine, et le séquençage d’ARN de noyaux uniques a montré que les adipocytes et leurs cellules précurseurs en étaient les principales sources. Lorsque les cellules cancéreuses étaient exposées à la kynurénine, elles augmentaient leurs niveaux de ferritine, réduisaient le fer libre et résistaient à la ferroptose. Le blocage d’IDO1 et de TDO2 dans la graisse abolissait cette augmentation de la ferritine, sauf si la kynurénine était réintroduite.
Une seule molécule qui bloque la soupape de libération du fer
La kynurénine n’agit pas seule. À l’intérieur des cellules tumorales, elle est convertie le long d’une voie en plusieurs métabolites. En bloquant sélectivement des étapes individuelles, les auteurs ont découvert qu’un intermédiaire, la 3‑hydroxykynurénine (3‑HK), est l’acteur clé. La 3‑HK, même à faibles doses, stabilisait la ferritine, réduisait la libération de fer et protégeait fortement les cellules de la ferroptose. D’un point de vue mécanistique, la 3‑HK se liait directement à une protéine nommée NCOA4, qui escorte normalement la ferritine vers les « centres de recyclage » cellulaires où elle est dégradée et où le fer est libéré. Des expériences structurales et biophysiques ont montré que la 3‑HK se fixe sur NCOA4 et l’empêche de s’apparier à la ferritine, gelant effectivement ces coffres‑forts à fer en place et privant la ferroptose du métal dont elle a besoin pour s’enclencher. Lorsque NCOA4 était supprimée, la 3‑HK ne pouvait plus augmenter la ferritine ni protéger les cellules contre la mort par ferroptose.
Transformer le bouclier en cible thérapeutique
Parce que la mort ferroptotique des cellules cancéreuses peut renforcer l’immunité antitumorale, la voie 3‑HK–ferritine induite par la graisse offre une explication à la résistance fréquente des métastases riches en graisse, comme les implants péritonéaux issus de cancers du côlon ou de l’estomac, aux immunothérapies. Dans plusieurs modèles murins, l’inhibition conjointe d’IDO1 et de TDO2 a abaissé la kynurénine et la 3‑HK dans le micro‑environnement tumeur‑graisse, réduit l’accumulation de ferritine et rendu les tumeurs beaucoup plus vulnérables aux inducteurs de ferroptose. De manière particulièrement frappante, l’association d’inhibiteurs IDO1/TDO2 avec des anticorps anti‑PD‑1 a produit un contrôle tumoral bien plus marqué, y compris dans des modèles de métastases péritonéales, et ce bénéfice disparaissait lorsque la ferroptose était bloquée chimiquement. Les données patientes étayaient ces résultats : les métastases péritonéales présentaient une ferritine plus élevée et des dommages lipidiques plus faibles que les tumeurs primaires, et des signatures géniques prédictives d’abondance en 3‑HK corrélaient avec une maladie plus avancée et une survie moindre.
Ce que cela signifie pour la prise en charge future du cancer
Ce travail révèle une conversation jusque‑là cachée entre la graisse et la tumeur, dans laquelle le tissu adipeux environnant fabrique de la kynurénine, l’apporte aux cellules cancéreuses et élève ainsi les niveaux de 3‑HK qui enferment le fer à l’intérieur de la ferritine et bloquent la ferroptose. Ce faisant, la graisse aide non seulement les tumeurs à résister aux médicaments ciblant la ferroptose, mais elle affaiblit aussi la capacité du système immunitaire et des inhibiteurs de points de contrôle à les détruire. En interrompant cet axe kynurénine–3‑HK–ferritine, par exemple avec des inhibiteurs combinés d’IDO1/TDO2, les cliniciens pourraient être capables d’enlever ce bouclier protecteur et de rendre les cancers enfouis dans la graisse bien plus sensibles à l’immunothérapie et à d’autres traitements.
Citation: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Mots-clés: microenvironnement tumoral, ferroptose, voie de la kynurénine, tissu adipeux péri-tumoral, immunothérapie du cancer