Clear Sky Science · pt
O tecido adiposo peritumoral promove resistência à ferroptose por supressão da ferritinofagia mediada por 3‑hidroxiquinurenina
Gordura ao Redor dos Tumores: Um Protetor Oculto
Muitos cânceres crescem em contato próximo com tecido adiposo macio e acolchoado. Longe de ser um espectador passivo, essa gordura próxima pode secretamente ajudar os tumores a sobreviver tanto à quimioterapia quanto às imunoterapias modernas. Este estudo revela uma maneira surpreendente pela qual a gordura que envolve os tumores bloqueia um tipo de morte celular dependente de ferro nas células cancerosas e mostra como perturbar esse escudo pode tornar tratamentos existentes mais eficazes, especialmente em cânceres abdominais que se disseminam por superfícies adiposas.
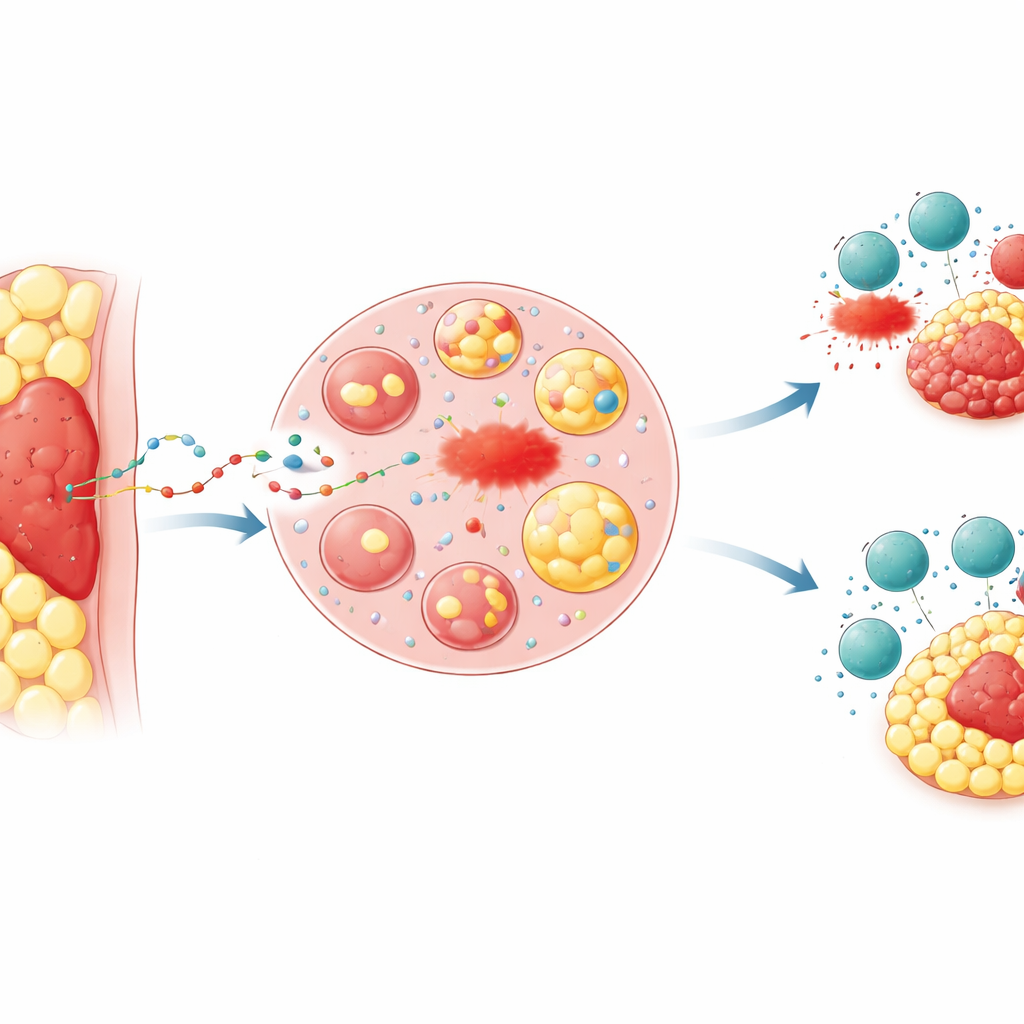
Quando a Localização Dá Vantagem aos Tumores
Médicos há muito tempo observam que tumores enterrados na gordura, como cânceres avançados de cólon e estômago que invadem o revestimento abdominal, costumam responder mal ao tratamento e levar a piores desfechos. Os pesquisadores concentraram‑se no “tecido adiposo peritumoral”—o anel de gordura imediatamente ao redor de um tumor. Em modelos de camundongo, implantaram as mesmas células cancerosas seja sob a pele, onde há pouca gordura, seja diretamente em uma almofada de gordura. Tumores alojados na gordura cresceram mais rápido, foram mais difíceis de erradicar com fármacos que induzem uma forma de morte celular chamada ferroptose, e foram menos sensíveis ao ataque imunológico de células T citotóxicas ou à imunoterapia anti‑PD‑1. Marcadores químicos de dano lipídico, que sinalizam a ocorrência de ferroptose, foram muito mais baixos em tumores embebidos na gordura, espelhando padrões observados em amostras de tecido de pacientes com câncer colorretal e gástrico avançados.
Caixas‑forte de Ferro Dentro das Células Cancerosas
A ferroptose depende do ferro livre; quando há ferro suficiente disponível, ele impulsiona a oxidação descontrolada das membranas celulares, matando a célula. As células cancerosas podem amortecer essa ameaça ao armazenar ferro dentro de conchas proteicas chamadas ferritina. A equipe investigou se a gordura próxima de alguma forma reconfigurava o manejo do ferro pelo tumor. Cultivaram células cancerosas em meio condicionado por tecido adiposo humano e de camundongo e descobriram que esse meio “condicionado” tornava as células marcadamente mais resistentes à ferroptose. O perfil proteômico revelou um forte aumento em ambas as subunidades principais da ferritina, sem mudanças importantes em outros reguladores conhecidos da ferroptose. Ao mesmo tempo, o pool de ferro livre dentro das células caiu. Quando os pesquisadores silenciaram a ferritina, o efeito protetor do meio derivado da gordura desapareceu, e tumores em locais ricos em gordura ficaram menores e mais sensíveis ao dano induzido pelo ferro.
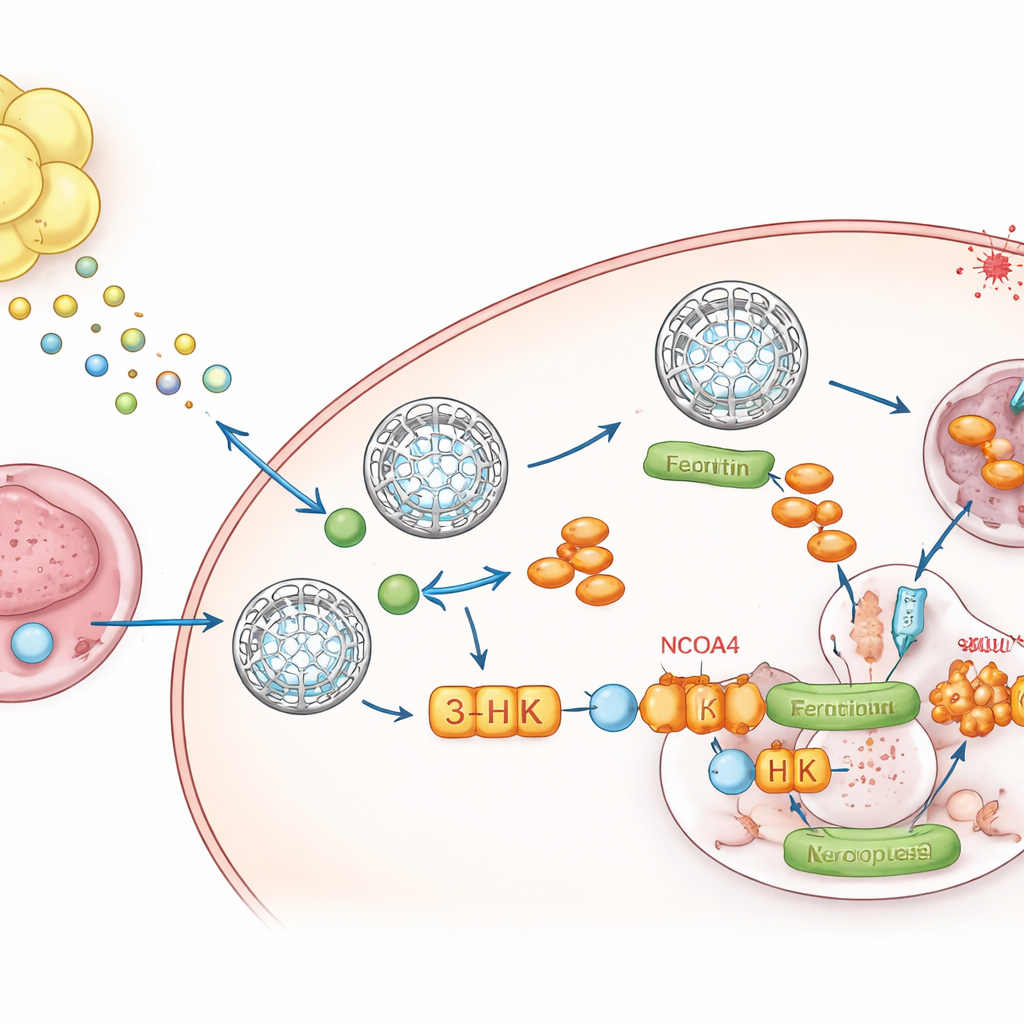
Um Mensageiro Metabólico da Gordura para o Tumor
Para identificar o que a gordura estava enviando, a equipe recorreu à metabolômica, um levantamento de pequenas moléculas. Um composto, quinurenina, um produto de degradação do aminoácido triptofano, destacou‑se por estar consistentemente elevado em meios condicionados por gordura e em tumores que cresciam dentro da gordura. O fluido que banhava esses tumores continha alta quinurenina e baixo triptofano, mostrando que o ambiente local está reprogramado. A gordura circundante expressava altos níveis das enzimas IDO1 e TDO2 que sintetizam quinurenina, e o sequenciamento de RNA de núcleo único mostrou que os adipócitos e suas células precursoras eram as principais fontes. Quando as células cancerosas foram expostas à quinurenina, aumentaram os níveis de ferritina, reduziram o ferro livre e resistiram à ferroptose. Bloquear IDO1 e TDO2 na gordura aboliu esse aumento de ferritina, a menos que a quinurenina fosse acrescentada novamente.
Uma Única Molécula que Bloqueia a Válvula de Liberação do Ferro
A quinurenina não age sozinha. Dentro das células tumorais ela é convertida ao longo de uma via em vários metabólitos. Ao bloquear seletivamente etapas individuais, os autores descobriram que um intermediário, 3‑hidroxiquinurenina (3‑HK), é o agente chave. A 3‑HK, mesmo em baixas doses, estabilizou a ferritina, reduziu a liberação de ferro e protegeu fortemente as células contra a ferroptose. Mecanisticamente, a 3‑HK ligou‑se diretamente a uma proteína chamada NCOA4, que normalmente escolta a ferritina até os “centros de reciclagem” celulares onde ela é degradada e o ferro é liberado. Experimentos estruturais e biofísicos mostraram que a 3‑HK se prende à NCOA4 e impede sua ancoragem à ferritina, congelando efetivamente essas caixas‑forte de ferro no lugar e privando a ferroptose do metal necessário para se iniciar. Quando a NCOA4 foi removida, a 3‑HK não pôde mais elevar a ferritina nem defender as células contra a morte por ferroptose.
Transformando o Escudo em Alvo Terapêutico
Como a morte ferroptótica de células cancerosas pode aumentar a imunidade antitumoral, a via 3‑HK–ferritina impulsionada pela gordura oferece uma explicação para o motivo pelo qual metástases ricas em gordura, como implantes peritoneais de câncer de cólon ou estômago, frequentemente resistem à imunoterapia. Em múltiplos modelos de camundongo, a inibição dupla de IDO1 e TDO2 reduziu quinurenina e 3‑HK no nicho tumor‑gordura, diminuiu o acúmulo de ferritina e tornou os tumores muito mais vulneráveis a indutores de ferroptose. Mais marcante ainda, a combinação de inibidores de IDO1/TDO2 com anticorpos anti‑PD‑1 produziu controle tumoral bem mais forte, inclusive em modelos de metástase peritoneal, e esse benefício foi perdido quando a ferroptose foi bloqueada quimicamente. Dados de pacientes corroboraram essas descobertas: metástases peritoneais mostraram maior ferritina e menor dano lipídico do que tumores primários, e assinaturas gênicas que preveem abundância de 3‑HK correlacionaram‑se com doença mais avançada e pior sobrevida.
O Que Isso Significa para o Cuidado do Câncer no Futuro
Este trabalho revela uma conversa anteriormente oculta entre gordura e tumor, na qual o tecido adiposo circundante fabrica quinurenina, a fornece às células cancerosas e, assim, eleva os níveis de 3‑HK que trancam o ferro dentro da ferritina e bloqueiam a ferroptose. Ao fazer isso, a gordura não apenas ajuda os tumores a resistir a fármacos direcionados à ferroptose, mas também enfraquece a capacidade do sistema imunológico e dos inibidores de checkpoint de destruí‑los. Ao interromper esse eixo quinurenina–3‑HK–ferritina, por exemplo com inibidores combinados de IDO1/TDO2, os clínicos podem ser capazes de arrancar esse escudo protetor e tornar cânceres embebidos em gordura muito mais responsivos à imunoterapia e a outros tratamentos.
Citação: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Palavras-chave: microambiente tumoral, ferroptose, via da quinurenina, tecido adiposo peritumoral, imunoterapia do câncer