Clear Sky Science · pl
Tkanka tłuszczowa wokół guza promuje oporność na ferroptozę poprzez tłumienie ferritinofagii zależne od 3‑hydroksykinureniny
Tłuszcz wokół guzów: ukryty obrońca
Wiele nowotworów rozwija się w bliskim kontakcie z miękką, miękką tkanką tłuszczową. Daleka od bycia biernym widzem, przylegająca tkanka tłuszczowa może potajemnie pomagać guzom przetrwać zarówno chemioterapię, jak i nowoczesne immunoterapie. To badanie ujawnia zaskakujący mechanizm, dzięki któremu tłuszcz otaczający guzy blokuje rodzaj śmierci komórkowej zależnej od żelaza w komórkach nowotworowych, i pokazuje, jak przerwanie tej tarczy mogłoby poprawić skuteczność istniejących terapii, zwłaszcza w nowotworach jamy brzusznej rozsiewających się po tłustych powierzchniach.
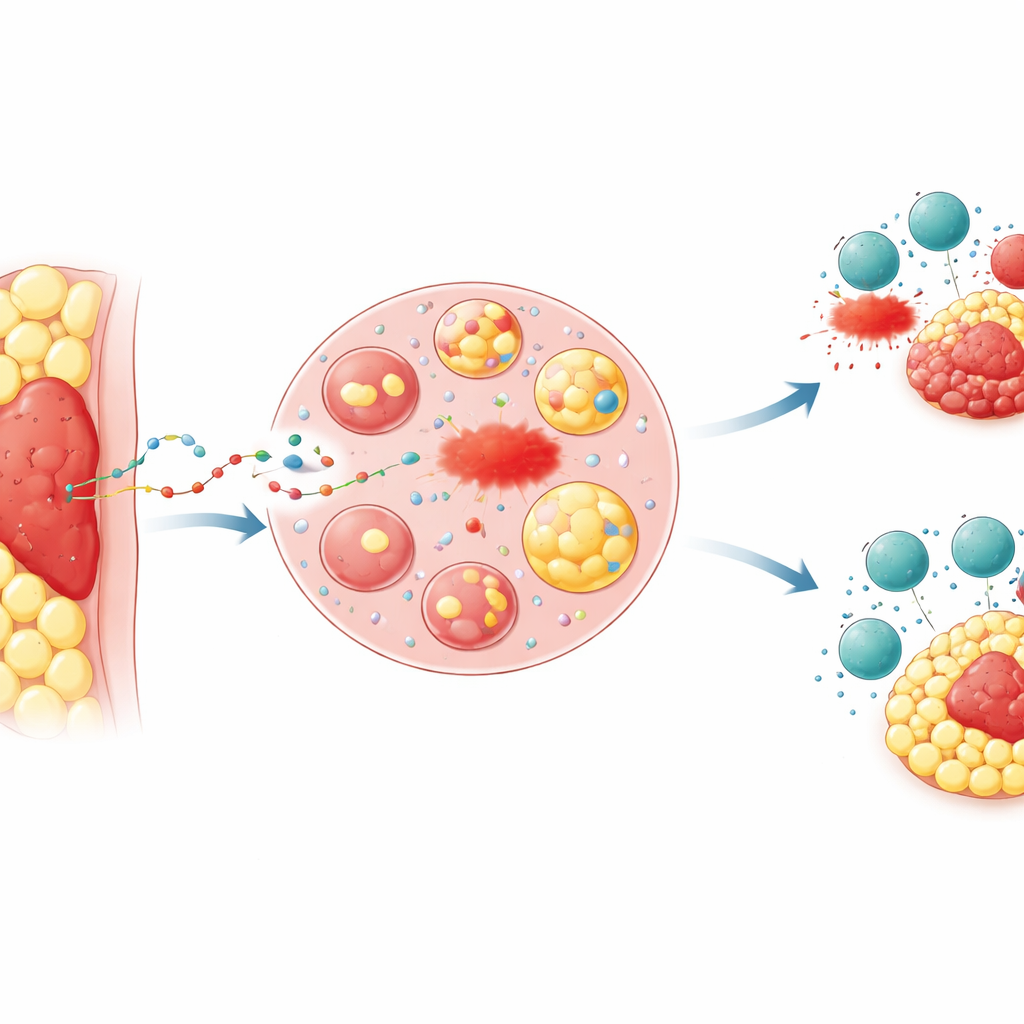
Kiedy lokalizacja daje guzom przewagę
Lekarze od dawna zauważają, że guzy zagnieżdżone w tłuszczu, takie jak zaawansowane nowotwory jelita grubego i żołądka naciekające błonę otrzewnową, często słabo reagują na leczenie i prowadzą do gorszych wyników. Badacze skoncentrowali się na „tkance tłuszczowej okołoguza” — pierścieniu tłuszczu otaczającym guz. W modelach mysich wszczepili te same komórki nowotworowe albo pod skórę, gdzie jest niewiele tłuszczu, albo bezpośrednio do poduszki tłuszczowej. Guzy osadzone w tłuszczu rosły szybciej, były trudniejsze do zniszczenia lekami wywołującymi formę śmierci komórkowej zwaną ferroptozą oraz mniej wrażliwe na atak komórek T‑zabójczych lub immunoterapię przeciw PD‑1. Chemiczne markery uszkodzeń lipidów, sygnalizujące zachodzenie ferroptozy, były znacznie niższe w guzach zanurzonych w tłuszczu, co odzwierciedlało wzorce obserwowane w próbkach tkanek od pacjentów z zaawansowanym rakiem jelita grubego i żołądka.
Żelazne sejfy w komórkach nowotworowych
Ferroptoza zależy od wolnego żelaza; gdy jest go wystarczająco dużo, napędza niekontrolowaną oksydację błon komórkowych, co prowadzi do śmierci komórki. Komórki nowotworowe mogą neutralizować to zagrożenie, magazynując żelazo wewnątrz białkowych „skrytek” zwanych ferratyną. Zespół badał, czy otaczający tłuszcz w jakiś sposób przeprogramowuje gospodarkę żelazem w guzie. Hodowali komórki nowotworowe w płynach pochodzących z tkanki tłuszczowej ludzi i myszy i stwierdzili, że takie „uwarunkowane” medium sprawiało, że komórki były wyraźnie bardziej oporne na ferroptozę. Profilowanie proteomiczne wykazało silny wzrost obu głównych podjednostek ferratyny, bez istotnych zmian w innych znanych regulatorach ferroptozy. Jednocześnie pula wolnego żelaza wewnątrz komórek faktycznie się zmniejszyła. Gdy badacze wyciszyli ferratynę, ochronny efekt medium pochodzącego z tłuszczu zniknął, a guzy w miejscach bogatych w tłuszcz stały się mniejsze i bardziej wrażliwe na uszkodzenia zależne od żelaza.
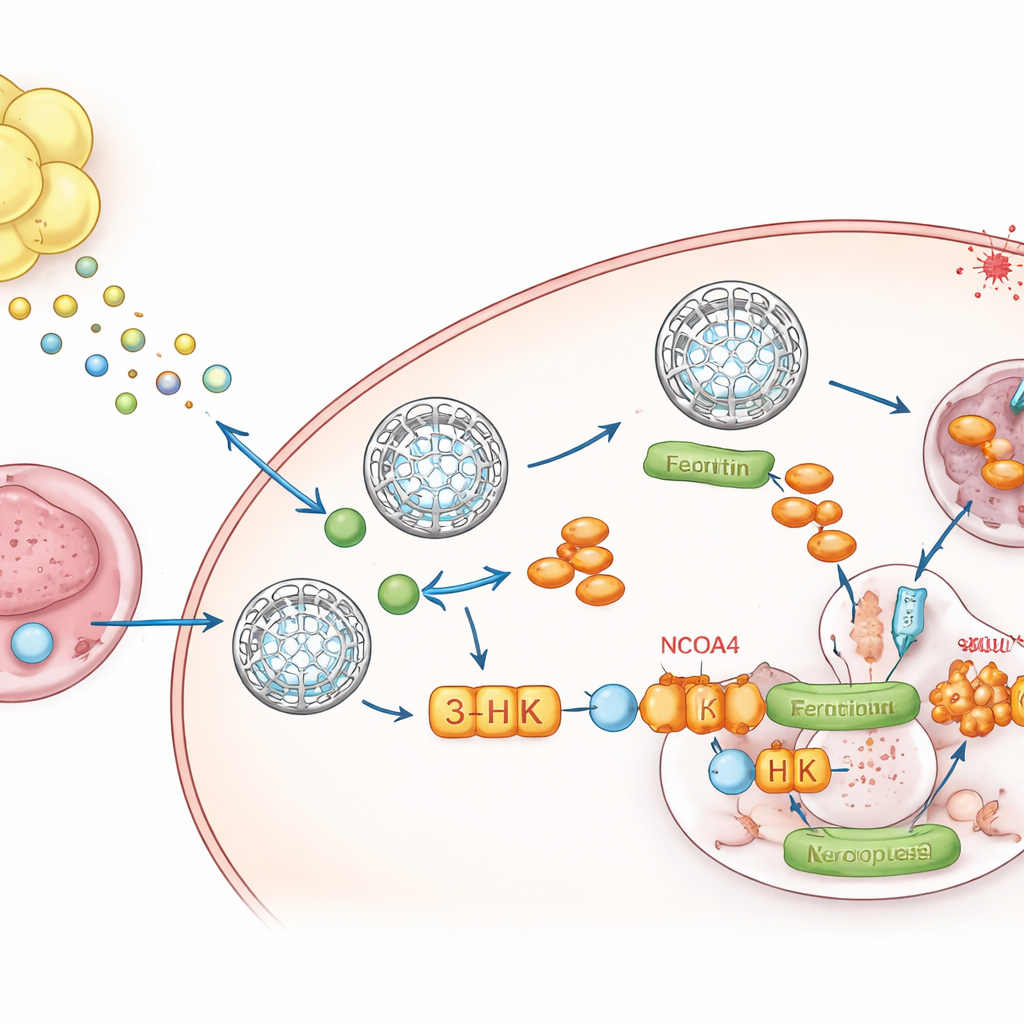
Metaboliczny posłaniec z tłuszczu do guza
Aby ustalić, co tłuszcz przekazuje, zespół sięgnął po metabolomikę — przegląd małych cząsteczek. Jedna z nich, kynurenina, produkt rozpadu aminokwasu tryptofanu, wyróżniała się jako konsekwentnie podwyższona w mediach uwarunkowanych przez tłuszcz i w guzach rozwijających się w tłuszczu. Płyn otaczający te guzy zawierał dużo kynureniny i mało tryptofanu, co dowodzi, że lokalne środowisko zostało przeprogramowane. Otaczający tłuszcz wykazywał wysoką ekspresję enzymów IDO1 i TDO2 produkujących kynureninę, a sekwencjonowanie pojedynczych jąder komórkowych pokazało, że adipocyty i ich komórki prekursorowe były głównymi źródłami. Gdy komórki nowotworowe były wystawione na działanie kynureniny, podnosiły poziom ferratyny, obniżały wolne żelazo i opierały się ferroptozie. Zablokowanie IDO1 i TDO2 w tłuszczu znosiło ten wzrost ferratyny, o ile nie dodano ponownie kynureniny.
Pojedyncza cząsteczka, która blokuje zawór uwalniający żelazo
Kynurenina nie działa sama. Wewnątrz komórek nowotworowych jest przekształcana wzdłuż szlaku do kilku metabolitów. Poprzez selektywne blokowanie poszczególnych kroków autorzy odkryli, że kluczowym odgrywa rolę jeden pośrednik — 3‑hydroksykinurenina (3‑HK). 3‑HK, nawet w niskich dawkach, stabilizowała ferratynę, ograniczała uwalnianie żelaza i silnie chroniła komórki przed ferroptozą. Mechanistycznie 3‑HK wiązała się bezpośrednio z białkiem NCOA4, które normalnie eskortuje ferratynę do komórkowych „centrów recyklingu”, gdzie jest rozkładana i żelazo jest uwalniane. Badania strukturalne i biofizyczne wykazały, że 3‑HK przyczepia się do NCOA4 i uniemożliwia mu dokowanie z ferratyną, skutecznie zamrażając te żelazne sejfy w miejscu i pozbawiając ferroptozę metalu, którego potrzebuje do zapłonu. Gdy NCOA4 został usunięty, 3‑HK nie mogła już podnieść poziomu ferratyny ani chronić komórek przed śmiercią ferroptotyczną.
Przekształcanie tarczy w cel terapeutyczny
Ponieważ śmierć ferroptotyczna komórek nowotworowych może wzmacniać odporność przeciwnowotworową, napędzana przez tłuszcz oś 3‑HK–ferratyna daje wyjaśnienie, dlaczego przerzuty bogate w tłuszcz, takie jak implanty otrzewnowe z raka jelita grubego czy żołądka, często opierają się immunoterapii. W wielu modelach mysich podwójne zahamowanie IDO1 i TDO2 obniżało poziomy kynureniny i 3‑HK w niszy guz–tłuszcz, zmniejszało nagromadzenie ferratyny i czyniło guzy znacznie bardziej podatnymi na induktory ferroptozy. Co najbardziej uderzające, połączenie inhibitorów IDO1/TDO2 z przeciwciałami anty‑PD‑1 dało znacznie silniejszą kontrolę guza, także w modelach przerzutów otrzewnowych, a korzyść ta zniknęła, gdy ferroptoza została chemicznie zablokowana. Dane od pacjentów potwierdziły te odkrycia: przerzuty otrzewnowe wykazywały wyższą ferratynę i niższe uszkodzenia lipidów niż guzy pierwotne, a sygnatury genowe przewidujące obfitość 3‑HK korelowały z bardziej zaawansowaną chorobą i gorszym przeżyciem.
Co to oznacza dla przyszłej opieki onkologicznej
Ta praca ujawnia wcześniej ukrytą rozmowę między tłuszczem a guzem, w której otaczająca tkanka tłuszczowa wytwarza kynureninę, dostarcza ją komórkom nowotworowym, a w rezultacie podnosi poziomy 3‑HK, które blokują uwalnianie żelaza z ferratyny i hamują ferroptozę. W ten sposób tłuszcz nie tylko pomaga guzom przetrwać leki ukierunkowane na ferroptozę, lecz także osłabia zdolność układu odpornościowego i inhibitorów punktów kontrolnych do ich eliminacji. Przerywając tę oś kynurenina–3‑HK–ferratyna, na przykład za pomocą skojarzonej inhibitory IDO1/TDO2, klinicyści mogą pozbawić tę ochronną tarczę i uczynić guzy osadzone w tłuszczu znacznie bardziej podatnymi na immunoterapię i inne terapie.
Cytowanie: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Słowa kluczowe: mikrośrodowisko guza, ferroptoza, szlak kynureninowy, tkanka tłuszczowa okołoguza, immunoterapia nowotworów