Clear Sky Science · es
El tejido adiposo peritumoral promueve la resistencia a la ferroptosis mediante la supresión de la ferritinofagia mediada por 3‑hidroxikinurenina
La grasa alrededor de los tumores: un protector oculto
Muchos cánceres crecen en estrecho contacto con tejido adiposo blando y acolchado. Lejos de ser un espectador pasivo, esta grasa cercana puede ayudar en secreto a que los tumores sobrevivan tanto a la quimioterapia como a las inmunoterapias modernas. Este estudio descubre una forma sorprendente en la que la grasa que rodea a los tumores bloquea un tipo de muerte celular impulsada por el hierro dentro de las células cancerosas, y muestra cómo desactivar este escudo podría mejorar la eficacia de los tratamientos existentes, especialmente en los cánceres abdominales que se diseminan por superficies grasas.
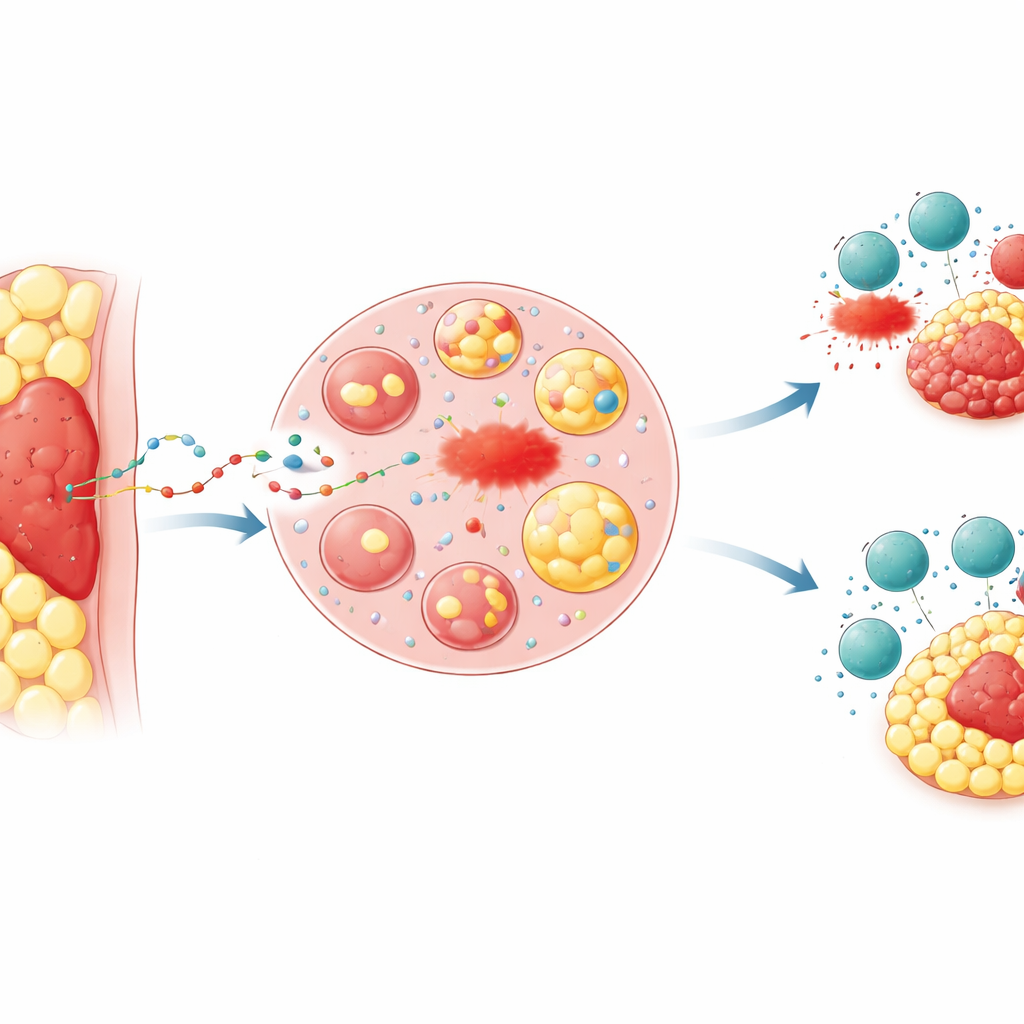
Cuando la ubicación da ventaja a los tumores
Los médicos han observado durante mucho tiempo que los tumores enterrados en grasa, como los cánceres avanzados de colon y estómago que invaden el revestimiento abdominal, a menudo responden mal al tratamiento y se asocian a peores resultados. Los investigadores se centraron en el “tejido adiposo peritumoral”, el anillo de grasa que rodea inmediatamente a un tumor. En modelos de ratón, implantaron las mismas células cancerosas bien bajo la piel, donde hay poca grasa, o directamente en una almohadilla grasa. Los tumores alojados en la grasa crecieron más rápido, fueron más difíciles de eliminar con fármacos que inducen una forma de muerte celular llamada ferroptosis, y fueron menos sensibles al ataque inmune de células T citotóxicas o a la inmunoterapia anti‑PD‑1. Los marcadores químicos de daño lipídico, que indican la ocurrencia de ferroptosis, fueron mucho más bajos en tumores incrustados en grasa, reflejando patrones observados en muestras de tejido de pacientes con cánceres colorrectales y gástricos avanzados.
Cajas fuertes de hierro dentro de las células cancerosas
La ferroptosis depende del hierro libre; cuando hay suficiente hierro disponible, fomenta la oxidación descontrolada de las membranas celulares, matando la célula. Las células cancerosas pueden amortiguar esta amenaza almacenando hierro dentro de estructuras proteicas llamadas ferritina. El equipo se preguntó si la grasa cercana de algún modo reprogramaba el manejo del hierro por los tumores. Cultivaron células cancerosas en líquido procedente de tejido adiposo humano y de ratón y encontraron que este medio “condicionado” hacía que las células fueran claramente más resistentes a la ferroptosis. El perfil proteómico reveló un notable aumento en ambas subunidades principales de la ferritina, sin cambios importantes en otros reguladores conocidos de la ferroptosis. Al mismo tiempo, la reserva de hierro libre dentro de las células disminuyó. Cuando los investigadores redujeron la expresión de ferritina, el efecto protector del medio derivado de la grasa desapareció, y los tumores en sitios ricos en grasa se hicieron más pequeños y más sensibles al daño inducido por el hierro.
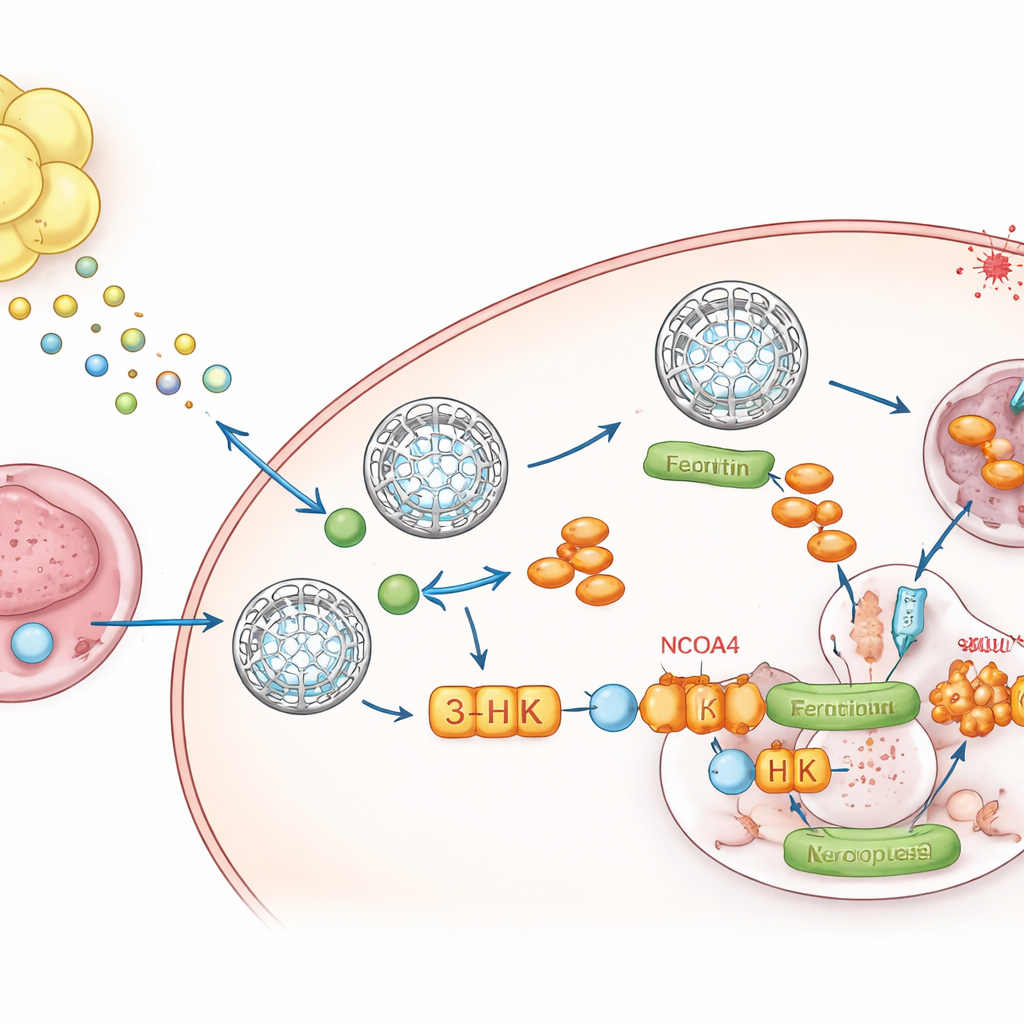
Un mensajero metabólico de la grasa al tumor
Para identificar qué estaba enviando la grasa, el equipo recurrió a la metabolómica, un análisis de pequeñas moléculas. Un compuesto, la quinurenina, producto de degradación del aminoácido triptófano, destacó por estar consistentemente elevado en los medios condicionados por grasa y en los tumores que crecían dentro de la grasa. El líquido que bañaba estos tumores contenía mucha quinurenina y poco triptófano, lo que muestra que el entorno local está reprogramado. La grasa circundante expresó altos niveles de las enzimas IDO1 y TDO2 que generan quinurenina, y la secuenciación de ARN de núcleo único mostró que los adipocitos y sus células precursoras eran las principales fuentes. Cuando las células cancerosas se expusieron a quinurenina, aumentaron los niveles de ferritina, disminuyeron el hierro libre y resistieron la ferroptosis. Bloquear IDO1 y TDO2 en la grasa abolió este aumento de ferritina, a menos que se añadiera quinurenina de nuevo.
Una molécula única que bloquea la válvula de liberación de hierro
La quinurenina no actúa sola. Dentro de las células tumorales se convierte a lo largo de una vía en varios metabolitos. Al bloquear selectivamente pasos individuales, los autores descubrieron que un intermedio, la 3‑hidroxikinurenina (3‑HK), es el actor clave. La 3‑HK, incluso a dosis bajas, estabilizó la ferritina, redujo la liberación de hierro y protegió con fuerza a las células de la ferroptosis. Mecanísticamente, la 3‑HK se unió directamente a una proteína llamada NCOA4, que normalmente escolta la ferritina hacia los “centros de reciclaje” celulares donde se degrada y se libera el hierro. Experimentos estructurales y biofísicos mostraron que la 3‑HK se acopla a NCOA4 y le impide anclarse a la ferritina, congelando efectivamente estas cajas fuertes de hierro en su lugar y privando a la ferroptosis del metal que necesita para encenderse. Cuando se eliminó NCOA4, la 3‑HK ya no pudo elevar la ferritina ni defender a las células contra la muerte ferroptótica.
Convertir el escudo en un objetivo terapéutico
Dado que la muerte ferroptótica de las células cancerosas puede potenciar la inmunidad antitumoral, la vía 3‑HK–ferritina impulsada por la grasa ofrece una explicación de por qué las metástasis ricas en grasa, como los implantes peritoneales de cánceres de colon o estómago, a menudo resisten la inmunoterapia. En múltiples modelos de ratón, la inhibición dual de IDO1 y TDO2 redujo la quinurenina y la 3‑HK en el nicho tumor‑grasa, disminuyó la acumulación de ferritina y hizo que los tumores fueran mucho más vulnerables a los inductores de ferroptosis. De forma más llamativa, la combinación de inhibidores de IDO1/TDO2 con anticuerpos anti‑PD‑1 produjo un control tumoral mucho más potente, incluso en modelos de metástasis peritoneal, y este beneficio se perdió cuando la ferroptosis fue bloqueada químicamente. Los datos de pacientes apoyaron estos hallazgos: las metástasis peritoneales mostraron mayor ferritina y menor daño lipídico que los tumores primarios, y las firmas génicas que predicen abundancia de 3‑HK se correlacionaron con enfermedad más avanzada y peor supervivencia.
Qué significa esto para la atención del cáncer en el futuro
Este trabajo revela una conversación hasta ahora oculta entre la grasa y el tumor, en la que el tejido adiposo circundante fabrica quinurenina, la suministra a las células cancerosas y, de este modo, eleva los niveles de 3‑HK que atrapan el hierro dentro de la ferritina y bloquean la ferroptosis. Al hacerlo, la grasa no solo ayuda a los tumores a resistir los fármacos dirigidos a la ferroptosis, sino que también reduce la capacidad del sistema inmune y de los inhibidores de puntos de control para destruirlos. Al interrumpir este eje quinurenina–3‑HK–ferritina, por ejemplo con inhibidores combinados de IDO1/TDO2, los clínicos podrían ser capaces de despojar a estos cánceres incrustados en grasa de su escudo protector y hacerlos mucho más sensibles a la inmunoterapia y a otros tratamientos.
Cita: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Palabras clave: microambiente tumoral, ferroptosis, vía de la quinurenina, tejido adiposo peritumoral, inmunoterapia contra el cáncer