Clear Sky Science · it
Il tessuto adiposo peritumorale promuove la resistenza alla ferroptosi mediante la soppressione della ferritinofagia mediata da 3‑idrossichinurenina
Il grasso intorno ai tumori: un protettore nascosto
Molti tumori crescono a stretto contatto con il tessuto adiposo morbido e cedevole. Lungi dall’essere un osservatore passivo, questo grasso vicino può segretamente aiutare i tumori a sopravvivere sia alla chemioterapia sia alle moderne immunoterapie. Questo studio svela un modo sorprendente in cui il tessuto adiposo peritumorale blocca un tipo di morte cellulare guidata dal ferro all’interno delle cellule tumorali e mostra come interrompere questo scudo potrebbe migliorare l’efficacia dei trattamenti esistenti, specialmente nei tumori addominali che si diffondono su superfici adipose.
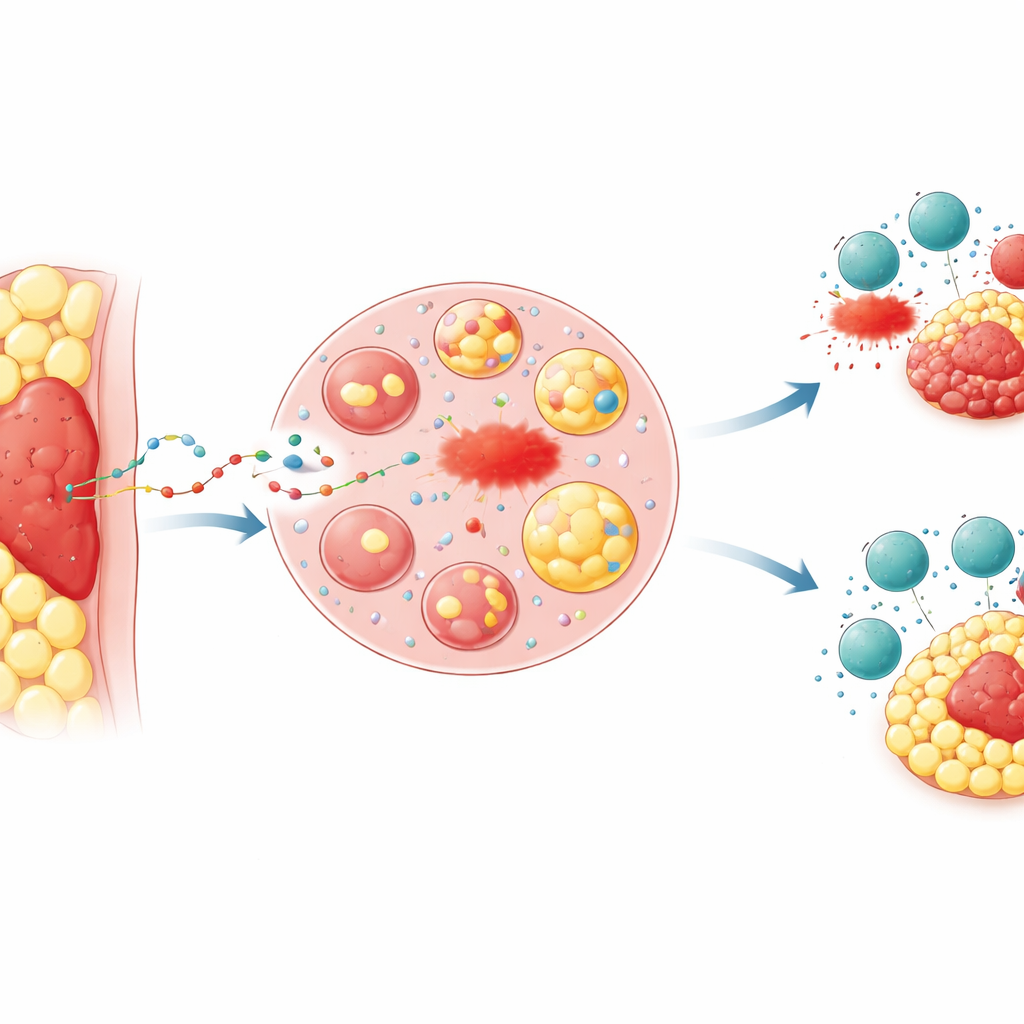
Quando la posizione dà un vantaggio al tumore
I medici hanno da tempo osservato che i tumori sepolti nel grasso, come i carcinomi avanzati del colon e dello stomaco che invadono la sierosa addominale, spesso rispondono male alle terapie e causano esiti peggiori. I ricercatori si sono concentrati sul “tessuto adiposo peritumorale” — l’anello di grasso che circonda immediatamente un tumore. In modelli murini hanno impiantato le stesse cellule tumorali sotto la pelle, dove c’è poco grasso, oppure direttamente in un deposito adiposo. I tumori annidati nel grasso crescevano più in fretta, erano più difficili da eliminare con farmaci che inducono una forma di morte cellulare chiamata ferroptosi e risultavano meno sensibili all’attacco da parte dei linfociti T citotossici o all’immunoterapia anti‑PD‑1. I marcatori chimici del danno lipidico, che indicano l’insorgenza della ferroptosi, erano molto più bassi nei tumori inseriti nel grasso, rispecchiando i modelli osservati nei campioni tissutali di pazienti con carcinoma colorettale e gastrico avanzato.
Scrigni di ferro all’interno delle cellule tumorali
La ferroptosi dipende dal ferro libero; quando è disponibile in quantità sufficiente, promuove l’ossidazione incontrollata delle membrane cellulari, uccidendo la cellula. Le cellule tumorali possono tamponare questa minaccia immagazzinando il ferro dentro involucri proteici chiamati ferritina. Il gruppo ha chiesto se il grasso circostante riorganizzasse in qualche modo la gestione del ferro nel tumore. Hanno coltivato cellule tumorali in un mezzo derivato da tessuto adiposo umano e murino e hanno scoperto che questo mezzo “condizionato” rendeva le cellule marcamente più resistenti alla ferroptosi. Il profilo proteomico ha rivelato un forte aumento di entrambe le subunità principali della ferritina, senza cambiamenti importanti in altri noti regolatori della ferroptosi. Allo stesso tempo, la riserva di ferro libero all’interno delle cellule è invece diminuita. Quando i ricercatori hanno silenziato la ferritina, l’effetto protettivo del mezzo derivato dal grasso è scomparso e i tumori in sedi ricche di grasso sono diventati più piccoli e più sensibili al danno indotto dal ferro.
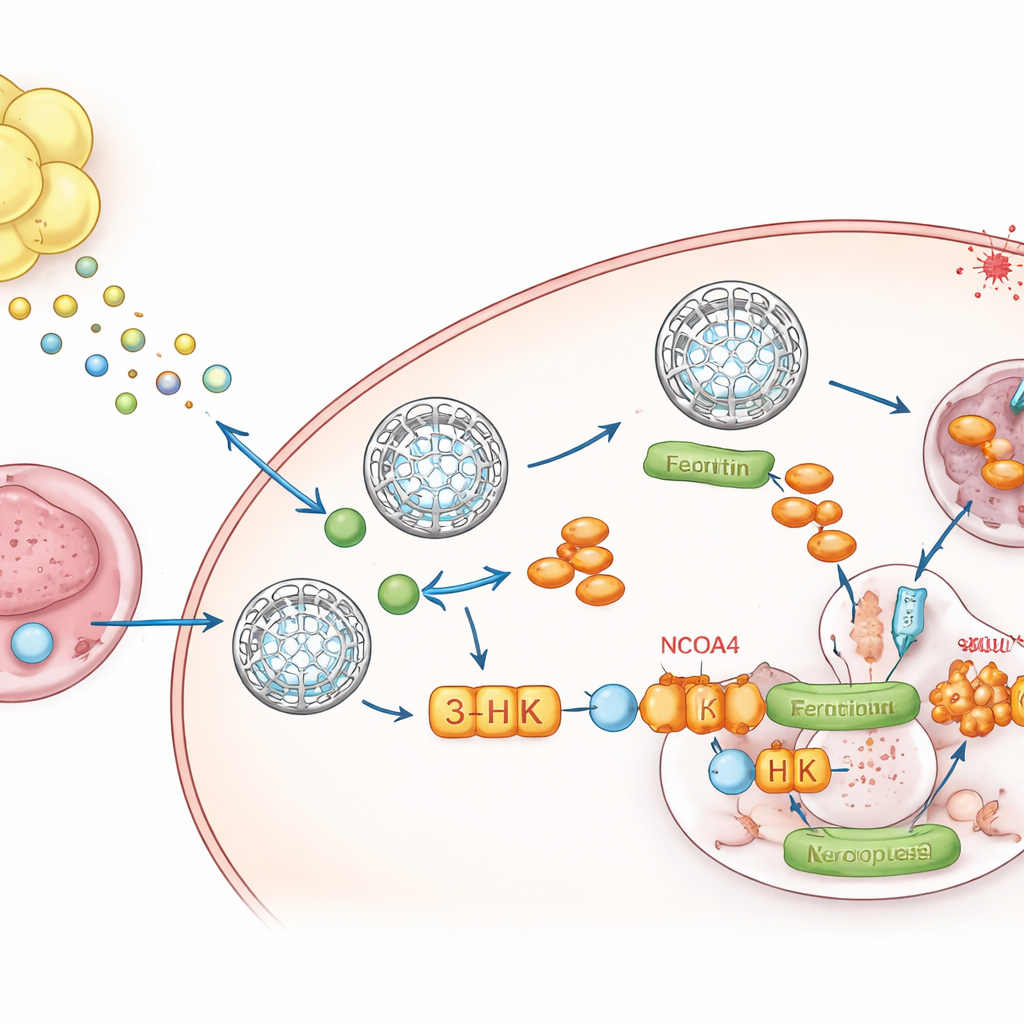
Un messaggero metabolico dal grasso al tumore
Per identificare cosa il grasso stesse inviando, il team ha ricorso alla metabolomica, un’analisi delle piccole molecole. Un composto, la chinurenina, un prodotto di degradazione dell’amminoacido triptofano, si è distinto come costantemente elevato nei mezzi condizionati dal grasso e nei tumori che crescevano nel grasso. Il fluido che bagna questi tumori conteneva alti livelli di chinurenina e bassi livelli di triptofano, mostrando che l’ambiente locale è rimodellato. Il tessuto adiposo circostante esprimeva alti livelli degli enzimi IDO1 e TDO2 che producono chinurenina, e il sequenziamento dell’RNA a singolo nucleo ha mostrato che gli adipociti e le loro cellule precursori erano le principali fonti. Quando le cellule tumorali sono state esposte alla chinurenina, hanno aumentato i livelli di ferritina, ridotto il ferro libero e resistito alla ferroptosi. Inibire IDO1 e TDO2 nel grasso aboliva questo aumento di ferritina a meno che la chinurenina non venisse aggiunta ex novo.
Una singola molecola che blocca la valvola di rilascio del ferro
La chinurenina non agisce da sola. All’interno delle cellule tumorali viene convertita lungo una via metabolica in diversi metaboliti. Bloccando selettivamente singoli passaggi, gli autori hanno scoperto che un intermedio, la 3‑idrossichinurenina (3‑HK), è il protagonista chiave. La 3‑HK, anche a basse dosi, stabilizzava la ferritina, riduceva il rilascio di ferro e proteggeva fortemente le cellule dalla ferroptosi. Dal punto di vista meccanicistico, la 3‑HK si legava direttamente a una proteina chiamata NCOA4, che normalmente accompagna la ferritina verso i “centri di riciclo” cellulari dove essa viene degradata e il ferro rilasciato. Esperimenti strutturali e biofisici hanno mostrato che la 3‑HK si aggancia a NCOA4 e ne impedisce l’interazione con la ferritina, congelando di fatto questi scrigni di ferro al loro posto e privando la ferroptosi del metallo necessario per scatenarsi. Quando NCOA4 è stato rimosso, la 3‑HK non riusciva più ad aumentare la ferritina né a difendere le cellule dalla morte ferroptotica.
Trasformare lo scudo in un bersaglio terapeutico
Poiché la morte ferroptotica delle cellule tumorali può potenziare l’immunità antitumorale, la via 3‑HK–ferritina indotta dal grasso offre una spiegazione del perché le metastasi ricche di grasso, come gli impianti peritoneali da tumori del colon o dello stomaco, spesso resistono all’immunoterapia. In diversi modelli murini, l’inibizione duale di IDO1 e TDO2 ha ridotto chinurenina e 3‑HK nel microambiente tumore‑grasso, diminuito l’accumulo di ferritina e reso i tumori molto più vulnerabili agli induttori di ferroptosi. In modo particolarmente significativo, la combinazione di inibitori di IDO1/TDO2 con anticorpi anti‑PD‑1 ha prodotto un controllo tumorale molto più efficace, anche nei modelli di metastasi peritoneali, e questo beneficio è scomparso quando la ferroptosi è stata bloccata chimicamente. Dati clinici supportano queste osservazioni: le metastasi peritoneali mostravano livelli più alti di ferritina e minore danno lipidico rispetto ai tumori primari, e i profili genici che prevedevano abbondanza di 3‑HK correlavano con malattia più avanzata e sopravvivenza peggiore.
Cosa significa questo per la cura del cancro in futuro
Questo lavoro rivela una conversazione fino ad ora nascosta tra grasso e tumore, nella quale il tessuto adiposo circostante produce chinurenina, la fornisce alle cellule tumorali e porterà così a livelli aumentati di 3‑HK che rinchiudono il ferro nella ferritina e bloccano la ferroptosi. Così facendo, il grasso non solo aiuta i tumori a resistere ai farmaci mirati alla ferroptosi, ma attenua anche la capacità del sistema immunitario e degli inibitori dei checkpoint di eliminarli. Interrompendo quest’asse chinurenina–3‑HK–ferritina, per esempio con inibitori combinati di IDO1/TDO2, i clinici potrebbero essere in grado di rimuovere questo scudo protettivo e rendere i tumori inseriti nel grasso molto più sensibili all’immunoterapia e ad altri trattamenti.
Citazione: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
Parole chiave: microambiente tumorale, ferroptosi, via della chinurenina, tessuto adiposo peritumorale, immunoterapia oncologica