Clear Sky Science · he
הרקמה השומנית סביב הגידול מקדמת עמידות לפרוטוזת־ברזל דרך דיכוי פריטינופאגיה בתיווך 3‑הידרוקסיקינורנין
השומן סביב הגידולים: מגן סמוי
מגוון סרטן גדל במגע הדוק עם שומן רך ובולע. רחוק מלהיות משקיף פסיבי, השומן הסמוך יכול בעקיפין לסייע לגידולים לשרוד הן כימותרפיה והן אימונותרפיות עדכניות. מחקר זה חושף מנגנון מפתיע שבו השומן שמקיף גידולים חוסם צורת מוות תאית מונעת‑ברזל בתוך תאים סרטניים, ומראה כיצד הפרעה למגן זה עשויה לחזק את השפעת הטיפולים הקיימים, במיוחד בסרטנים של חלל הבטן המתפשטים על משטחים שומניים.
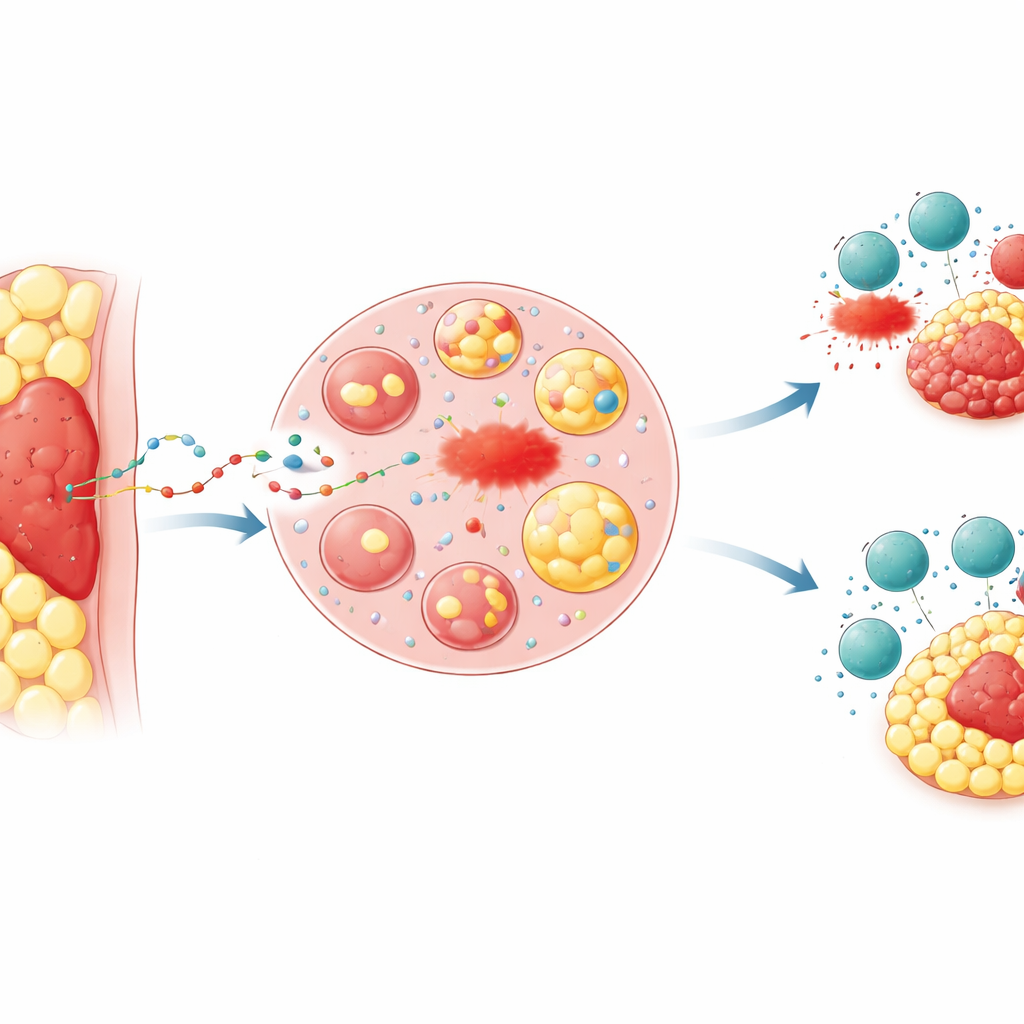
מתי המיקום נותן לגידול יתרון
רופאים ידעו זמן רב כי גידולים הטבונים בתוך שומן, כמו סרטן המעי הגס והקיבה במערכות מתקדמות הפולש לתוך הצפק, מגיבים לעתים גרוע לטיפול ומנבאים תוצאות פחות טובות. החוקרים בחנו את ה"רקמת השומן הפריטומורלית"—טבעת השומן הסמוכה המיידית לגידול. במודלים עכבריים הם השתילו את אותם תאי סרטן או מתחת לעור, שם יש מעט שומן, או ישירות לתוך כרית שומן. גידולים שקועי‑שומן גדלו מהר יותר, היו קשים יותר להשמדה בעזרת תרופות שמזרזות צורת מוות תאית שנקראת פרוטוזת‑ברזל, והיו פחות רגישים למתקפות חיסוניות של תאי T קטלניים או לאימונותרפיה נגד PD‑1. סימנים כימיים של נזק לליפידים, המציינים שקורה פרוטוזת‑ברזל, היו נמוכים בהרבה בגידולים מוטמנים בשומן — תבנית המשקפת דגימות רקמה של מטופלים עם סרטן מעי גס וקיבה מתקדמים.
קופסאות נעילה של ברזל בתוך תאי סרטן
פרוטוזת‑ברזל תלויה בברזל חופשי; כשריכוז הברזל גבוה מספיק הוא מזין חמצון מתפרץ של ממברנות התא, ההורג את התא. תאים סרטניים יכולים להצטייד באיום זה על‑ידי אחסון הברזל במעטפות חלבוניות שנקראות פריטין. הצוות שאל האם השומן הסמוך משנה את ניהול הברזל של הגידול. הם גידלו תאים סרטניים בתמיסת גידול שהופק מרקמות שומן אנושיות ועכבריות ומצאו שתווך "ממותג" זה הפך את התאים לעמידים באופן משמעותי לפרוטוזת‑ברזל. פרופיל חלבונים חשף עלייה חזקה בשתי תתי־היחידות העיקריות של הפריטין, ללא שינויים משמעותיים בווסתי פרוטוזת‑ברזל ידועים אחרים. במקביל, מאגר הברזל החופשי בתאים ירד. כאשר החוקרים השביתו פריטין, האפקט המגן של תווך שמקורו בשומן נעלם, וגידולים באתרים עשירים בשומן הפכו קטנים יותר ורגישים יותר לנזק מוּנחה‑ברזל.
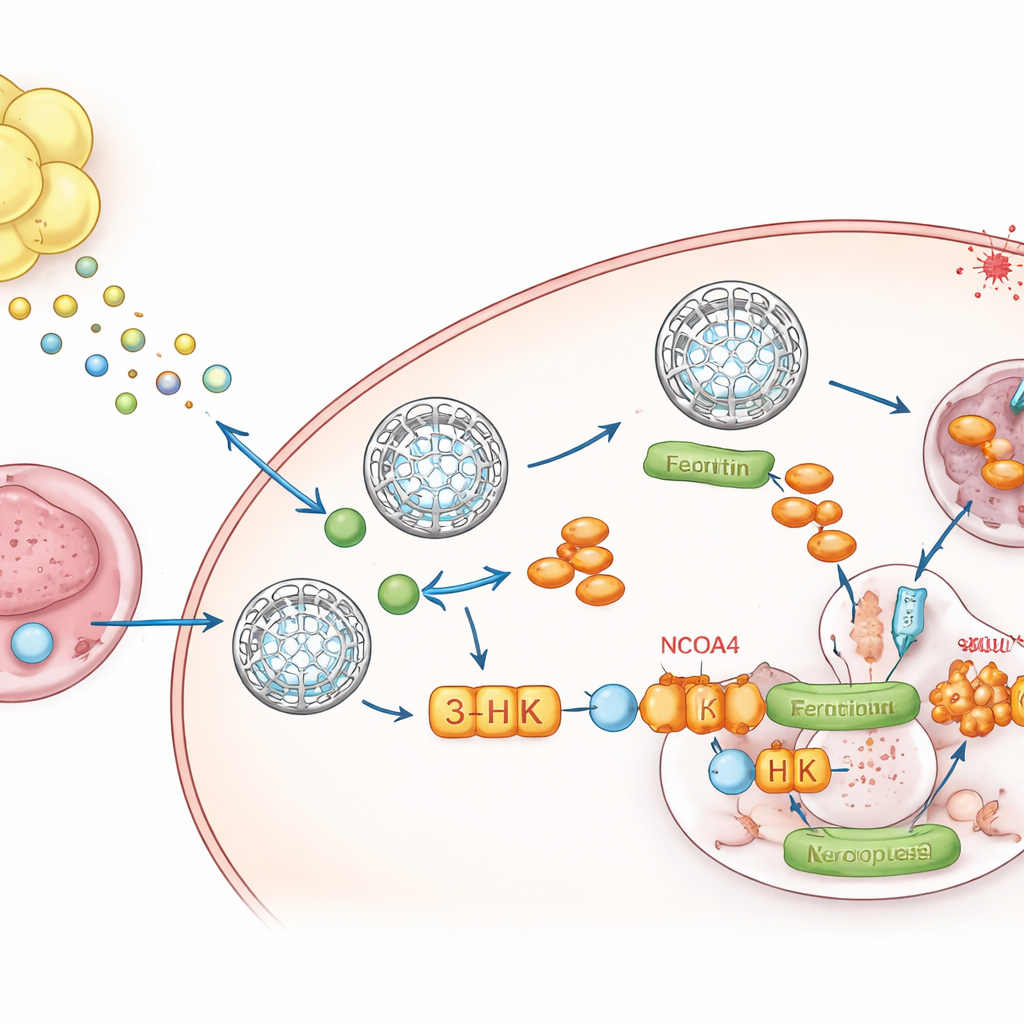
שליח מטבולי מהשומן אל הגידול
כדי לזהות מה השומן משדר, הצוות פנה למטבולומיקה, סקר של מולקולות קטנות. תרכובת אחת, קינורנין — תוצר פירוק של חומצת האמינו טריפטופן — בלטה כעולה בעקביות בתווכים ממקור שומני ובגידולים גדלים בתוך שומן. הנוזל שמקלח גידולים אלה הכיל רמות גבוהות של קינורנין ורמות נמוכות של טריפטופן, מה שמראות שהמיקרו‑סביבה המקומית עברה רה‑וירינג. השומן הסובב הביע רמות גבוהות של האנזימים IDO1 ו‑TDO2 המייצרים קינורנין, ותאי גרעין יחידים (single‑nucleus RNA sequencing) הראו שהאדיפוציטים ותאי‑האם שלהם הם המקורות העיקריים. כאשר תאים סרטניים נחשפו לקינורנין, הם הגדילו את רמות הפריטין, הורידו את הברזל החופשי והפכו לעמידים לפרוטוזת‑ברזל. חסימת IDO1 ו‑TDO2 בשומן ביטלה את עליית הפריטין אלא אם הוחזר קינורנין חיצוני.
מולקולה יחידה שסוגרת את שסתום שחרור הברזל
קינורנין אינו פועל לבדו. בתוך תאי הגידול הוא מומר לאורך מסלול למספר מטבוליטים. באמצעות עיכוב סלקטיבי של צעדים בודדים, המחברים גילו שמתווך אחד, 3‑הידרוקסיקינורנין (3‑HK), הוא השחקן המרכזי. 3‑HK, אפילו במינונים נמוכים, ייצוב פריטין, הפחית שחרור ברזל והגן בעוצמה על התאים מפני פרוטוזת‑ברזל. במכניזם, 3‑HK נקשר ישירות לחלבון הנקרא NCOA4, שאחריתו היא להסיע פריטין ל"מרכזי מיחזור" תאיים שבהם הוא מפורק והברזל משתחרר. ניסויים מבניים וביופיזיקליים הראו כי 3‑HK נצמד ל‑NCOA4 ומונע ממנו לעגון בפריטין, ובכך מקפיא בפועל את קופסאות‑נעילת הברזל ומרעיב את הפרוטוזת‑ברזל מהמטל שהוא זקוק לו כדי להתלקח. כאשר NCOA4 הוסר, 3‑HK כבר לא הצליח להעלות פריטין או להגן על תאים מפני מוות פרוטוזתי.
הפיכת המגן למטרה טיפולית
מכיוון שמוות פרוטוזתי של תאים סרטניים יכול להגביר חיסון נגד הגידול, ציר ה‑3‑HK–פריטין המונע על‑ידי שומן מספק הסבר לכך שמטסטזות עשירות‑שומן, כמו נטיעות צפקיות מסרטן המעי או הקיבה, לעתים קרובות עמידות לאימונותרפיה. במודלים עכבריים מרובים, עיכוב כפול של IDO1 ו‑TDO2 הוריד את ריכוזי הקינורנין וה‑3‑HK בנישת הגידול‑שומן, צמצם הצטברות פריטין והפך גידולים לפגיעים הרבה יותר למזרזי פרוטוזת‑ברזל. הממצא המדהים ביותר היה כי שילוב מעכבי IDO1/TDO2 עם נוגדני anti‑PD‑1 ניבא שליטה חזקה בהרבה על הגידול, כולל במודלים של גרורות צפקיות, ותועלת זו נעלמה כשפרוטוזת‑הברזל נחסמה כימית. נתוני מטופלים תמכו בממצאים: גרורות צפקיות הראו פריטין גבוה ונזק שומני נמוך יותר לעומת הגידולים הראשוניים, וחתימות גנטיות שמנבאות שפע 3‑HK היקשרו למחלה מתקדמת יותר ולהישרדות פחות טובה.
מה משמעות הדבר לטיפול בסרטן בעתיד
עבודה זו מגלה שיחה שהייתה חבויה בין שומן לגידול שבה רקמת השומן הסובבת מייצרת קינורנין, מספקת אותו לתאים סרטניים, ובכך מגדילה רמות 3‑HK שמנעלות את הברזל בתוך הפריטין וחוסמות פרוטוזת‑ברזל. בכך השומן לא רק מסייע לגידולים לעמוד בתרופות המכוונות לפרוטוזת‑ברזל, אלא גם מצמצם את היכולת של המערכת החיסונית ומחסומי‑נקודות‑בקרה (checkpoint inhibitors) להרוס אותם. על‑ידי שיבוש ציר הקינורנין–3‑HK–פריטין, למשל עם שילוב מעכבי IDO1/TDO2, קלינאים עשויים להסיר את המגן הזה ולהפוך סרטן מוטמן‑שומן לרגיש הרבה יותר לאימונותרפיה ולטיפולים אחרים.
ציטוט: Zhang, YY., Han, Y., Tan, YT. et al. Peritumoural adipose tissue promotes ferroptosis resistance by 3-hydroxykynurenine-mediated suppression of ferritinophagy. Nat Cell Biol 28, 783–796 (2026). https://doi.org/10.1038/s41556-026-01907-x
מילות מפתח: מיקרו‑סביבה של הגידול, פרוטוזת‑ברזל (פרורפטוזיס), מסלול הקינורנין, רקמת שומן פריטומורלית, אימונותרפיה של סרטן