Clear Sky Science · zh
线粒体作为聚集倾向蛋白的藏匿隔间,阻碍高效降解
为何蛋白团块关系到大脑健康
在许多脑部疾病中,如阿尔茨海默病、帕金森病和亨廷顿病,某些蛋白质会失去正确折叠并在神经细胞内聚集成团。这些黏性的团块会干扰关键过程,并最终导致细胞死亡。这项研究提出了一个看似简单的问题:既然细胞已有强大的“垃圾处理”系统,为什么不能更有效地清除这些有问题的蛋白?答案将视线引向细胞内一个意想不到的地点——线粒体,通常被称为细胞的“发电站”。
细胞清理队及其局限
我们的细胞不断合成并降解蛋白质。当蛋白质错误折叠时,一条主要的处置通路是泛素–蛋白酶体系统,类似于先标记垃圾再送入碎纸机的传送带。异常蛋白先被小分子(泛素)标记,然后被送入桶状机器(蛋白酶体)中,分解成无害的小片段。该系统尤其擅长早期发现受损蛋白,防止它们变成大而不溶的团块。然而在神经退行性疾病中,尽管此处置系统可能仍然在功能上大体完好,团块仍会积累。这个难题提示问题可能不仅在于“碎纸机”的能力,还在于这些“垃圾”是否真的到达了那里。
寻找改变蛋白降解的基因开关
为探查哪些因素决定聚集倾向蛋白的命运,研究人员构建了一种带有荧光报告蛋白的人类细胞系,该报告蛋白易错折叠但不会立即致毒。随后他们进行了全基因组CRISPR–Cas9筛选,逐一关闭成千上万个基因,并根据细胞中有多少故障报告蛋白对细胞进行分选。这样他们能够精确识别出那些要么帮助细胞降解报告蛋白、要么使其在细胞内滞留更久的基因。正如预期,许多命中基因已知属于内质网表面的蛋白处置机器,内质网也是一个质量控制中心。但另一组更令人惊讶的基因指向了线粒体以及一个叫eIF5A的翻译因子,该因子已知会影响线粒体行为。
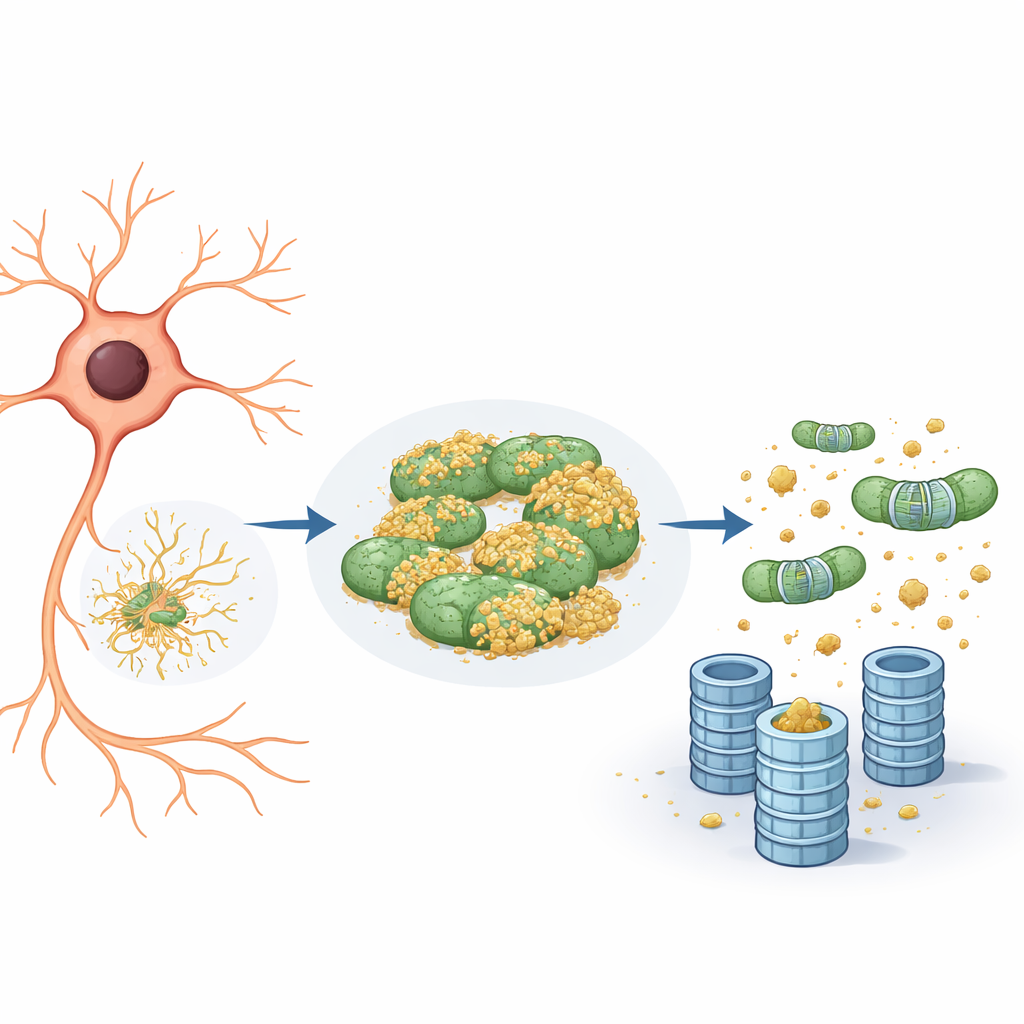
线粒体作为有害蛋白的藏匿处
更仔细的观察显示,该报告蛋白不仅倾向于与内质网相关联,也会与线粒体结合。在这些线粒体上,它大多未被标记,因此对蛋白酶体“碎纸机”不可见。当研究组降低eIF5A的活性——要么通过基因手段降低其水平,要么阻断它所需的一种独特化学修饰——发生了两件事:首先,线粒体网络变得更支离破碎并重新组织;其次,报告蛋白从线粒体上脱落,其降解加速,这一过程严格通过泛素–蛋白酶体系统而非通过自噬等细胞回收途径。实质上,线粒体充当了一个“藏匿隔间”,是有问题蛋白可以避开被标记和销毁的安全港。
从人工报告蛋白到与疾病相关的蛋白
导致这种行为的关键是一个被称为两亲螺旋的结构基序——一段短小、部分亲水部分亲脂的片段,帮助蛋白黏附于膜。当研究人员在报告蛋白中削弱这一螺旋时,该蛋白不太可能结合线粒体或形成聚集体,也不再在阻断eIF5A时显示出增强的降解。重要的是,多种与疾病相关的蛋白,包括突变的亨廷顿蛋白(亨廷顿病)和突变的α‑突触核蛋白(帕金森病),也含有两亲螺旋并且已知会错误定位到线粒体。在表达这些蛋白的细胞模型中,降低eIF5A活性或以其他方式扰乱线粒体网络,会使这些疾病相关蛋白从线粒体上解离,并更有效地被蛋白酶体清除,出现大聚集体的细胞数量也减少。
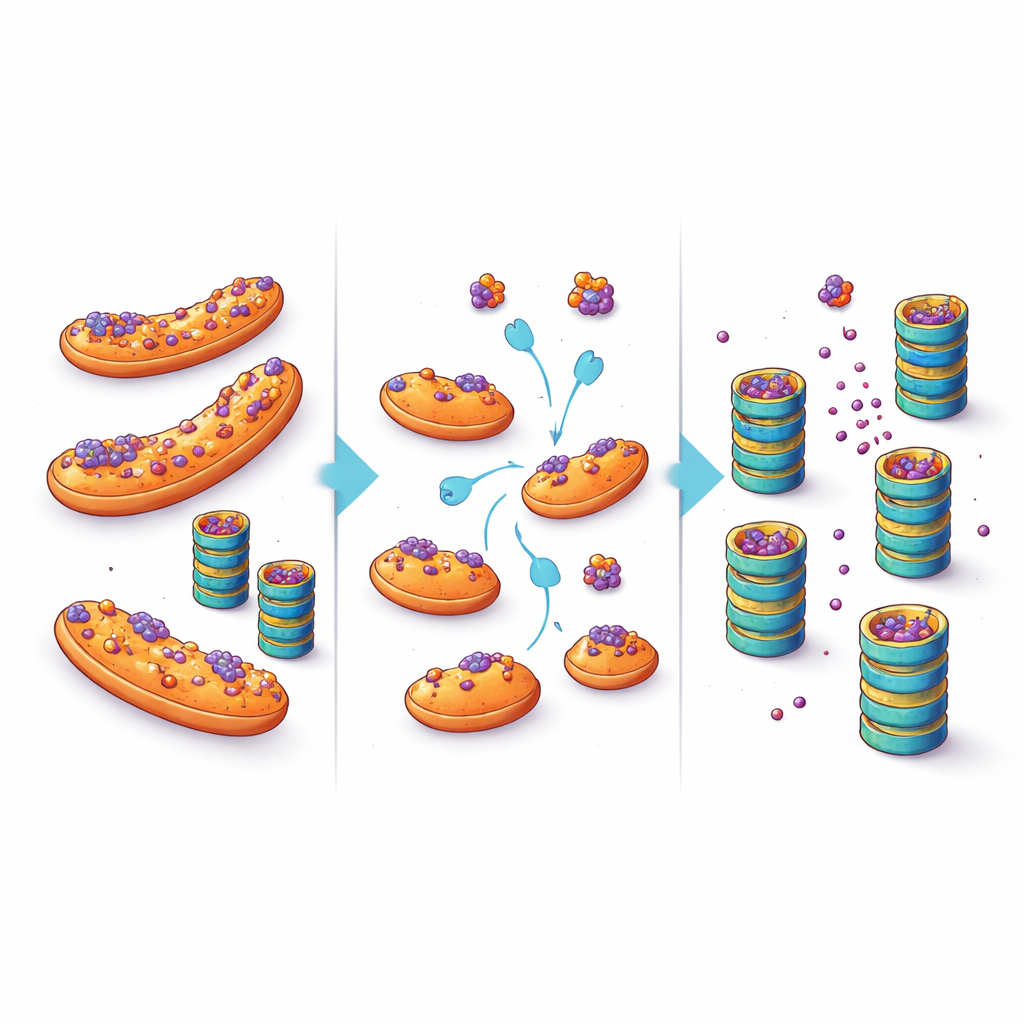
将细胞避难所变成治疗机遇
这些发现提示我们在考虑神经退行性疾病中蛋白质积累时应有新的视角。与其假定细胞的“碎纸机”只是被压垮或损坏,这项工作强调位置是一个关键因素:当易聚集的蛋白停靠在线粒体上时,它们对质量控制酶的可及性降低,降解速度变慢。通过将它们从这一避难所轻推出来——例如针对eIF5A等因子进行精确调节,或直接干扰它们停靠线粒体的能力——可能有望降低易受损神经元内的有毒蛋白水平。当然,任何未来的治疗都需要在此类干预与线粒体和eIF5A众多其他生理功能之间取得平衡,但该研究开启了一条诱人的治疗思路:不仅只是增强细胞“碎纸机”的力量,还要帮助错误折叠的蛋白找到通往它的路径。
引用: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
关键词: 线粒体, 蛋白聚集, 蛋白酶体, 神经退行性, eIF5A