Clear Sky Science · ja
ミトコンドリアは分解を妨げる凝集しやすいタンパク質の退避区画として機能する
なぜタンパク質の塊が脳の健康に重要なのか
アルツハイマー病、パーキンソン病、ハンチントン病など多くの脳疾患では、特定のタンパク質が本来の立体構造を失い、神経細胞内で凝集してしまいます。こうした粘着性の塊は重要な細胞プロセスを乱し、最終的に細胞死を引き起こすことがあります。本研究は見かけ上は単純な問いを投げかけます:もし細胞が強力なゴミ処理システムを持っているのなら、なぜ問題となるタンパク質をもっと効率的に取り除けないのか?その答えは細胞内部の予想外の場所――しばしば細胞の発電所と呼ばれるミトコンドリア――にたどり着きます。
細胞の清掃班とその限界
私たちの細胞はタンパク質を常に合成し、分解しています。タンパク質が誤って折りたたまれた場合、主要な処分経路の一つがユビキチン–プロテアソーム系であり、タグを付けてシュレッダーに流すコンベアのように働きます。問題のあるタンパク質はまず小さな分子(ユビキチン)で標識され、その後樽状の装置(プロテアソーム)に送り込まれて無害な断片に分解されます。このシステムは特に、タンパク質が大きく不溶性の塊になる前の早期段階で損傷タンパク質を捕らえるのが得意です。それでも神経変性疾患では凝集体が蓄積します。プロテアソーム系が概ね機能している場合でもです。この矛盾は、問題がシュレッダーの力だけでなく、ゴミが実際にそこに届くかどうかにもあることを示唆します。
タンパク質分解を変える遺伝的スイッチの探索
凝集しやすいタンパク質の運命を制御する因子を調べるため、研究者らは蛍光レポータータンパク質を組み込んだ特殊なヒト細胞株を作成しました。このレポーターは誤折りたたみしやすいよう設計されているが、直ちに毒性を示さないものです。次に、ゲノム全体を対象としたCRISPR–Cas9スクリーニングで多数の遺伝子を一つずつ不活化し、レポーターの蓄積量に基づいて細胞を振り分けました。これにより、レポーターの分解を助ける遺伝子や、逆に滞らせる遺伝子を特定できました。予想通り、多くのヒットはタンパク質処分機構の既知の構成要素、特に品質管理の拠点として機能する小胞体膜に関連していました。しかし、より意外な別の遺伝子群はミトコンドリアと、ミトコンドリアの挙動に影響を与えることで知られる翻訳因子eIF5Aを示しました。
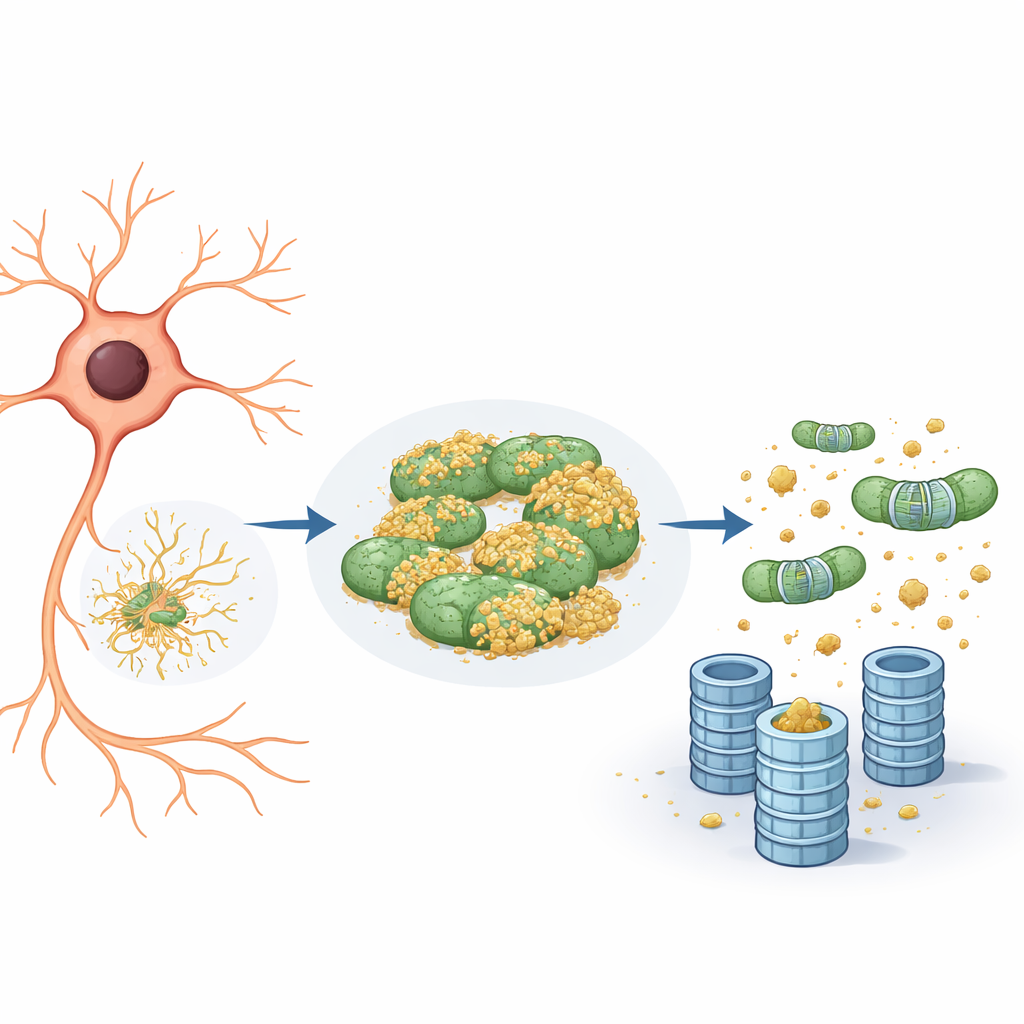
悪性タンパク質の隠れ場所としてのミトコンドリア
詳しく調べると、レポータータンパク質は小胞体だけでなくミトコンドリアにも結びつく傾向があることが明らかになりました。ミトコンドリア上ではレポーターは概して標識されず、したがってプロテアソームのシュレッダーからは見えにくくなっていました。研究チームがeIF5Aの活性を、遺伝的にその量を減らすか、機能に必要な独特な化学修飾を阻害することで低下させると、二つの変化が生じました。第一に、ミトコンドリアネットワークがより断片化して再編成されました。第二に、レポーターはミトコンドリアから離れ、分解が加速しましたが、その経路はオートファジーのような細胞の再利用経路ではなく、厳密にユビキチン–プロテアソーム系によるものでした。本質的にミトコンドリアは「退避区画」として働き、問題のあるタンパク質が標識され破壊されるのを逃れているように見えました。
人工レポーターから疾患関連タンパク質へ
この挙動の鍵は両親媒性ヘリックスと呼ばれる構造モチーフであることがわかりました。これは、水と脂の両方に親和性を示す短い領域で、タンパク質が膜に付着するのを助けます。研究者らがレポーターのこのヘリックスを弱めると、タンパク質はミトコンドリアに結合したり凝集したりする傾向が減り、eIF5Aを阻害しても分解促進は見られなくなりました。重要なのは、変異ハンチチン(ハンチントン病)や変異α‑シヌクレイン(パーキンソン病)など、いくつかの疾患関連タンパク質も両親媒性ヘリックスを含み、ミトコンドリアへ誤局在することが知られている点です。これらのタンパク質を発現する細胞モデルにおいて、eIF5A活性の低下やミトコンドリアネットワークの撹乱を引き起こすと、疾患タンパク質はミトコンドリアから離れ、プロテアソームによってより効率的に除去され、巨大な凝集体を示す細胞の割合が減少しました。
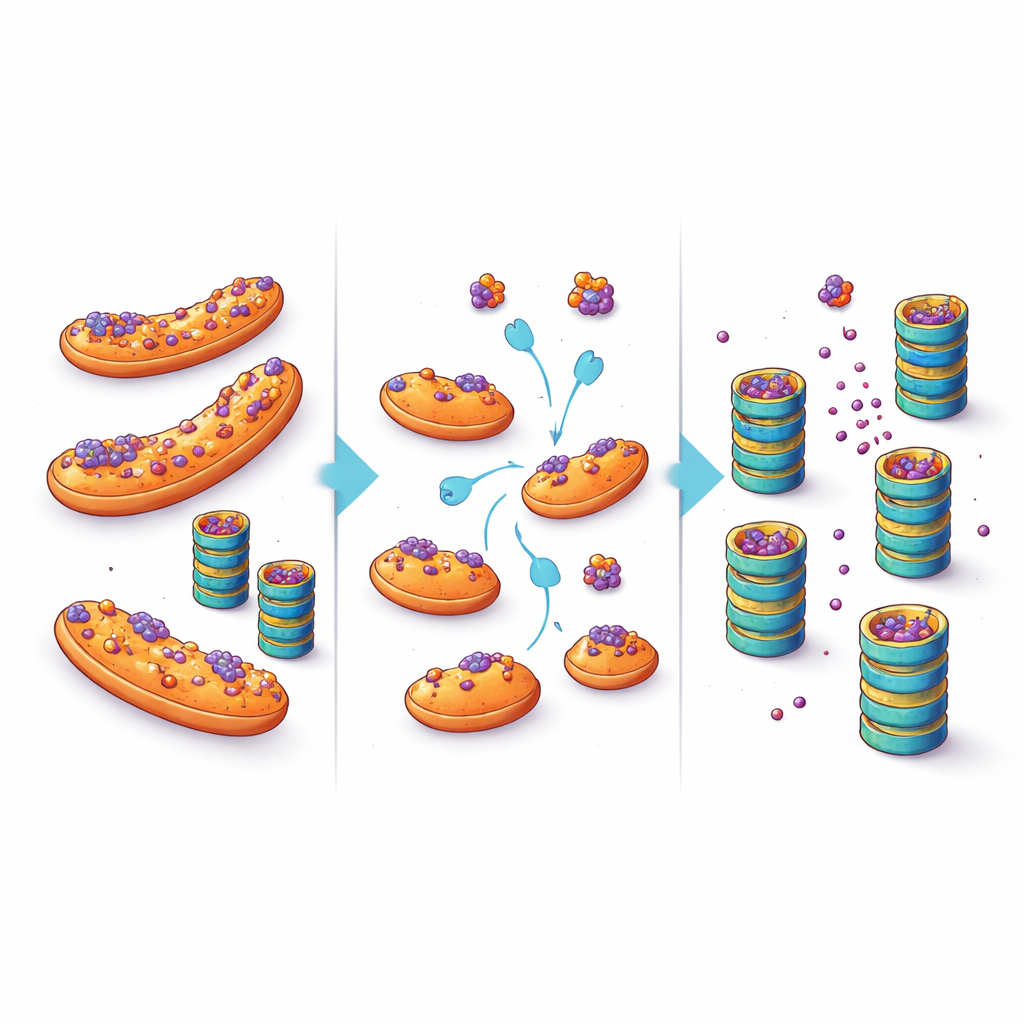
細胞の避難所を治療の機会に変える
これらの知見は、神経変性疾患におけるタンパク質蓄積の考え方に変化をもたらします。細胞のシュレッダーが単に圧倒されているか壊れていると考えるよりも、局所性が重要な要素であることが示されています。凝集しやすいタンパク質がミトコンドリアに留まると、品質管理酵素にとってアクセスしにくくなり、分解が遅くなります。eIF5Aのような因子を標的にするか、あるいはタンパク質がミトコンドリアに取り付く能力を直接妨げることで、これらのタンパク質をこの避難所から引き離し、脆弱なニューロン内の有害タンパク質量を減らすことが可能かもしれません。将来の治療ではミトコンドリアやeIF5Aの多様な役割とのバランスを取る必要はありますが、本研究は魅力的な治療の道筋を示します。すなわち、細胞のシュレッダーの力を上げるだけでなく、誤折りたたまれたタンパク質がそこに到達するのを助けるというアプローチです。
引用: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
キーワード: ミトコンドリア, タンパク質凝集, プロテアソーム, 神経変性, eIF5A