Clear Sky Science · ar
الميتوكوندريا تعمل كحجرة انتظار للبروتينات المائلة للتجمع مما يعيق تحللها الفعّال
لماذا تهم تكتلات البروتين لصحة الدماغ
في العديد من اضطرابات الدماغ مثل الزهايمر وباركنسون وهنتينغتون، تفقد بروتينات معينة شكلها الطبيعي وتتجمع داخل خلايا الأعصاب. هذه التكتلات اللاصقة يمكن أن تعطل عمليات حيوية وفي النهاية تقتل الخلايا. تطرح هذه الدراسة سؤالاً يبدو بسيطاً: إذا كانت الخلايا تمتلك بالفعل أنظمة قوية للتخلص من النفايات، فلماذا لا تتخلص ببساطة من هذه البروتينات المسببة للمشاكل بكفاءة أكبر؟ يقودنا الجواب إلى مكان غير متوقع داخل الخلية — الميتوكوندريا، التي تُعرف غالباً بأنها محطات طاقة الخلية.
فرق التنظيف الخلوية وحدودها
تُكوِّن خلايانا البروتينات باستمرار وتدمرها كذلك. عندما تنطوي البروتينات بشكل خاطئ، يكون أحد مسارات التخلص الرئيسية هو نظام اليوبكويتين–البروتيازوم، الذي يعمل مثل شريط ناقل لوضع الأوساخ الموسومة في مفرمة. تُوسَم البروتينات المعيبة أولاً بجزيئات صغيرة (اليوبكويتين) ثم تُغذى إلى آلات على شكل برميل (البروتيازومات) التي تمزقها إلى أجزاء غير ضارة. هذا النظام فعّال خصوصاً في التقاط البروتينات التالفة مبكراً، قبل أن تتصلب إلى تكتلات كبيرة غير قابلة للذوبان. ومع ذلك، في الأمراض العصبية التنكسية، تتراكم التكتلات رغم أن هذا النظام قد يظل وظيفياً إلى حد كبير. هذا اللغز يوحي بأن المشكلة قد لا تكمن فقط في قوة المفرمة، بل أيضاً في ما إذا كانت النفاية تصل إليها فعلاً.
البحث عن مفاتيح جينية تغير تحلل البروتين
لاستكشاف ما يتحكم بمصير البروتينات المائلة للتجمع، أنشأ الباحثون سلالة خلوية بشرية خاصة تحتوي على بروتين تقرير فلوري مصمم للانطواء بسهولة، من دون أن يكون ساماً فورياً. ثم استخدموا فحص CRISPR–Cas9 عبر الجينوم، إيقاف عمل آلاف الجينات واحدة تلو الأخرى وفرز الخلايا بحسب مقدار البروتين المتعطل الذي تراكم فيها. سمح لهم ذلك بتحديد جينات إما ساعدت الخلية على تدمير البروتين التقريري أو، على العكس، جعلته يبقى لفترة أطول. كما هو متوقع، كانت العديد من النتائج أجزاء معروفة من آلية التخلص من البروتين على سطح الشبكة الإندوبلازمية، وهي منظومة غشائية تعمل أيضاً كمحور لمراقبة الجودة. لكن مجموعة أخرى مفاجئة من الجينات أشارت إلى الميتوكوندريا وإلى عامل الترجمة المسمى eIF5A، المعروف بتأثيره على سلوك الميتوكوندريا.
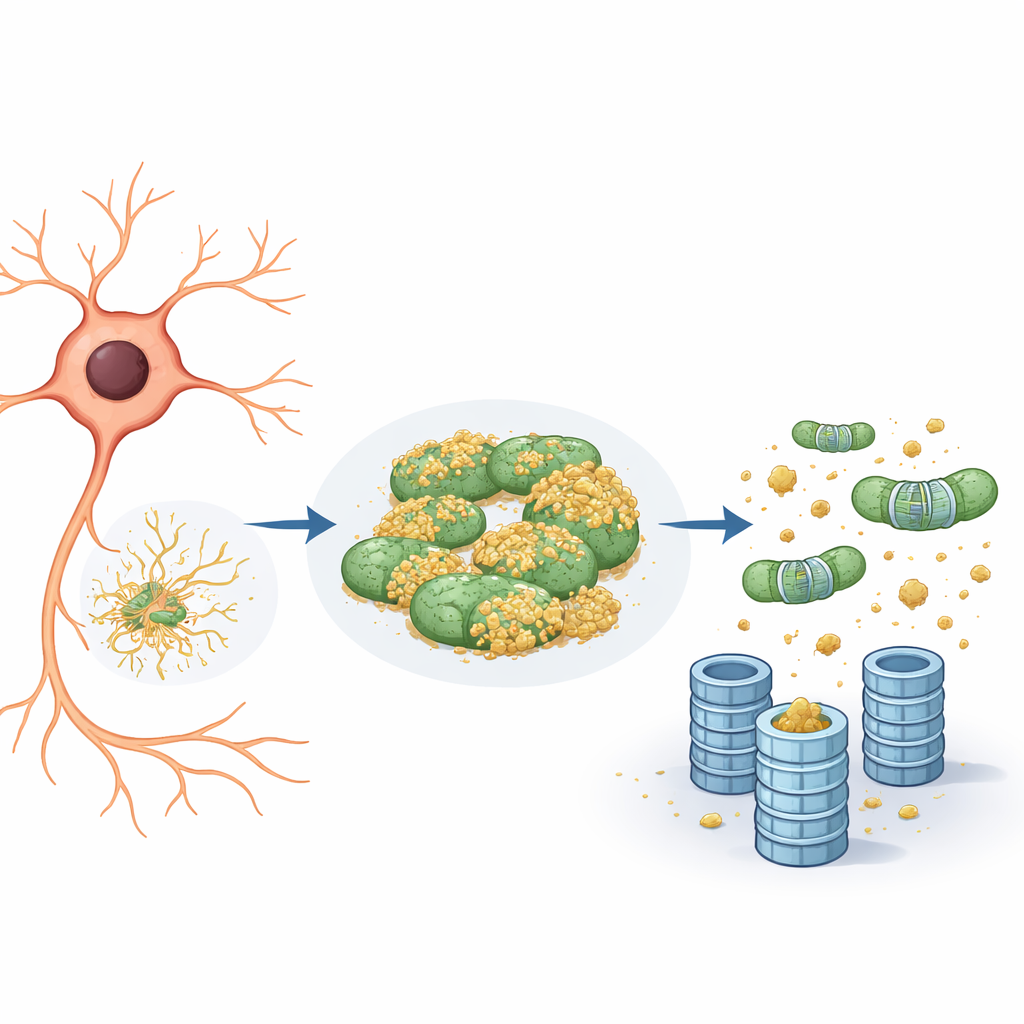
الميتوكوندريا كمكان إخفاء للبروتينات الضارة
كشف الفحص الدقيق أن البروتين التقريري كان يميل إلى الارتباط ليس فقط بالشبكة الإندوبلازمية بل أيضاً بالميتوكوندريا. على الميتوكوندريا، ظل البروتين إلى حد كبير غير موصوم وبالتالي غير مرئي للمفرمة البروتيازومية. عندما قلّص الفريق نشاط eIF5A — إما عن طريق خفض مستوياته جينياً أو عن طريق حظر تعديل كيميائي فريد يحتاجه ليعمل — حدث شيئان. أولاً، أصبح شبكة الميتوكوندريا أكثر تجزؤاً وأعيد تنظيمها. ثانياً، انفصل البروتين التقريري عن الميتوكوندريا وتسارع تحلله، وبشكل صارم عبر نظام اليوبكويتين–البروتيازوم بدلاً من خلال مسارات إعادة التدوير الخلوية مثل البلعمة الذاتية. في جوهرها، كانت الميتوكوندريا تعمل كـ"حجرة انتظار"، ملاذ آمن حيث يمكن للبروتينات المشكلة تجنب التأشير والتدمير.
من المرافقات الاصطناعية إلى البروتينات المرتبطة بالأمراض
اتضح أن مفتاح هذا السلوك هو نقش تركيبي يُسمى الحلزون المحب والممقوت للماء (amphipathic helix) — مقطع قصير محب جزئياً للماء وجزئياً للدهون يساعد البروتينات على الالتصاق بالغشاء. عندما خفف الباحثون هذا الحلزون في بروتينهم التقريري، أصبح البروتين أقل ميلاً للاقتران بالميتوكوندريا أو لتشكيل تكتلات ولم يعد يظهر تسريعاً في تحلله عند حظر eIF5A. ومن المهم أن عدة بروتينات مرتبطة بالأمراض، بما في ذلك هنتنغتين المتحول (في مرض هنتنغتون) وألفا‑سينوكلين المتحول (في مرض باركنسون)، تحتوي أيضاً على حلزونات محبة للماء/الدهون ومعروفة بإزاحتها إلى الميتوكوندريا. في نماذج خلوية تعبّر عن هذه البروتينات، أدى خفض نشاط eIF5A أو تعطيل تنظيم الميتوكوندريا إلى فصل بروتينات المرض عن الميتوكوندريا وإزالتها بكفاءة أكبر بواسطة البروتيازومات، مع وجود خلايا أقل تظهر تكتلات كبيرة.
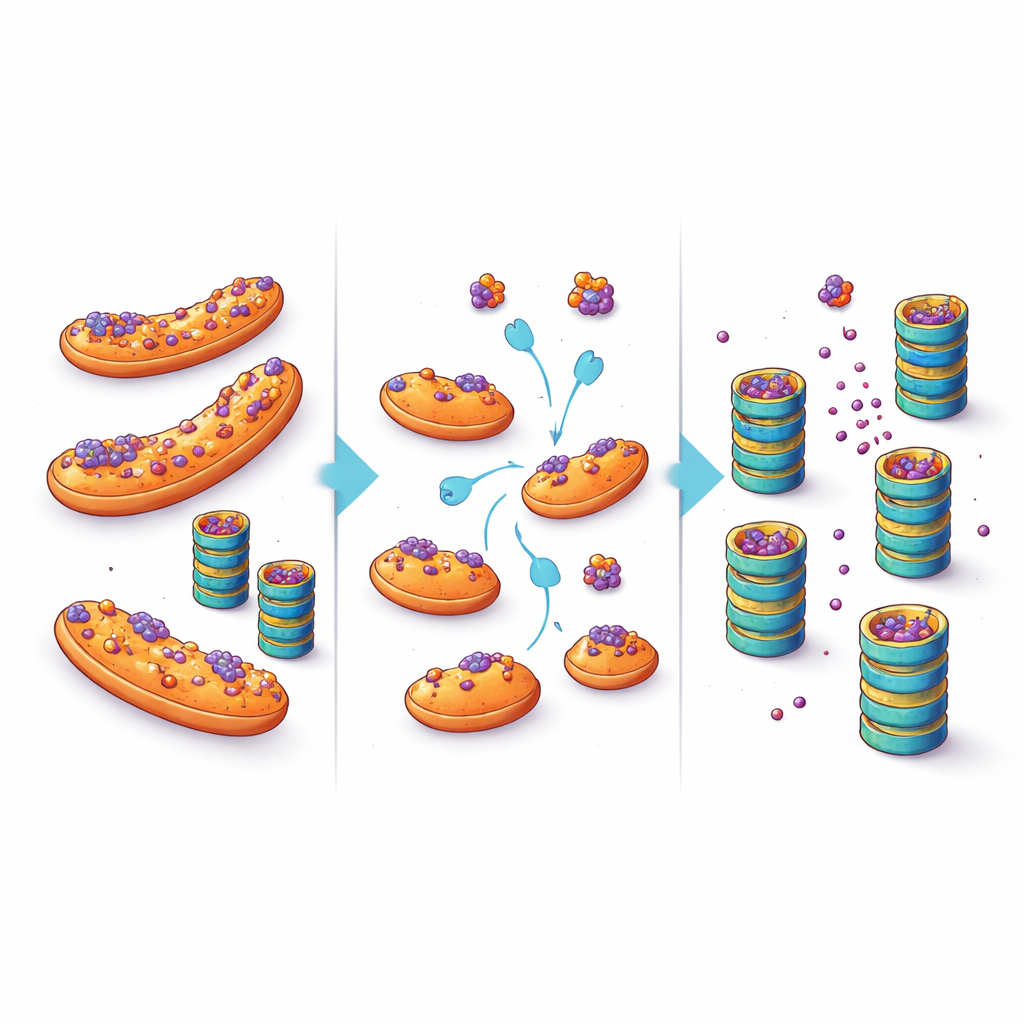
تحويل ملاذ خلوي إلى فرصة علاجية
تشير هذه النتائج إلى تحول في طريقة تفكيرنا بشأن تراكم البروتينات في الأمراض العصبية التنكسية. بدلاً من الافتراض أن المفرمات الخلوية مُعادلة أو معطلة ببساطة، تبرز هذه الدراسة أهمية الموقع كعامل حاسم: عندما تُركن البروتينات المائلة للتجمع على الميتوكوندريا، تصبح أقل وصولاً إلى إنزيمات مراقبة الجودة وتتحلل أبطأ. عن طريق دفعها بعيداً عن هذا الملاذ — من خلال تغييرات مستهدفة في عوامل مثل eIF5A أو عن طريق التدخل المباشر في قدرتها على الارتساء على الميتوكوندريا — قد يكون من الممكن خفض مستويات البروتينات السامة داخل الخلايا العصبية الضعيفة. وعلى الرغم من أن أي علاج مستقبلي سيحتاج إلى موازنة مثل هذه التدخلات مع الأدوار العديدة الأخرى للميتوكوندريا وeIF5A، تفتح هذه الدراسة مساراً علاجياً مغرياً: بدلاً من فقط رفع قدرة المفرمة الخلوية، ساعد البروتينات المطوية بشكل خاطئ على العثور على طريقها إليها.
الاستشهاد: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
الكلمات المفتاحية: الميتوكوندريا, تجميع البروتينات, البروتيازوم, اضطراب عصبي تنكسي, eIF5A