Clear Sky Science · fr
Les mitochondries servent de refuge pour des protéines sujettes à l’agrégation, entravant une dégradation efficace
Pourquoi les amas protéiques comptent pour la santé cérébrale
Dans de nombreux troubles cérébraux comme la maladie d’Alzheimer, de Parkinson et la maladie de Huntington, certaines protéines perdent leur conformation correcte et s’agglomèrent à l’intérieur des neurones. Ces amas collants peuvent perturber des processus vitaux et finir par tuer les cellules. Cette étude pose une question apparemment simple : si les cellules disposent déjà de systèmes d’élimination puissants, pourquoi n’éliminent-elles pas plus efficacement ces protéines problématiques ? La réponse conduit à un endroit inattendu dans la cellule : les mitochondries, souvent appelées centrales énergétiques de la cellule.
Les équipes de nettoyage cellulaires et leurs limites
Nos cellules fabriquent et détruisent constamment des protéines. Lorsqu’une protéine se déplie mal, une voie d’élimination majeure est le système ubiquitine–protéasome, qui fonctionne comme une chaîne de triage où les déchets sont étiquetés puis broyés. Les protéines défaillantes sont d’abord marquées par de petites molécules (ubiquitine) puis introduites dans des machines en forme de tonneau (protéasomes) qui les découpent en fragments inoffensifs. Ce système est particulièrement efficace pour repérer les protéines endommagées tôt, avant qu’elles ne durcissent en gros agrégats insolubles. Pourtant, dans les maladies neurodégénératives, des amas continuent de s’accumuler, même si ce système d’élimination peut rester en grande partie fonctionnel. Ce paradoxe suggère que le problème ne réside pas seulement dans la puissance du broyeur, mais aussi dans le fait que les déchets atteignent réellement celui-ci.
Identifier des bascules génétiques qui modulent la dégradation protéique
Pour explorer ce qui contrôle le sort des protéines sujettes à l’agrégation, les chercheurs ont créé une lignée cellulaire humaine spéciale contenant une protéine rapporteur fluorescente conçue pour se déplier facilement, sans être immédiatement toxique. Ils ont ensuite utilisé un criblage CRISPR–Cas9 à l’échelle du génome, inactivant des milliers de gènes un par un et triant les cellules selon la quantité du rapporteur défectueux accumulée. Cela leur a permis d’identifier des gènes qui aidaient la cellule à détruire le rapporteur ou, au contraire, le faisaient persister plus longtemps. Comme prévu, de nombreux résultats correspondaient à des éléments déjà connus de la machinerie d’élimination des protéines à la surface du réticulum endoplasmique, un système membranaire qui joue aussi le rôle de centre de contrôle qualité. Mais un autre groupe plus surprenant de gènes pointait vers les mitochondries et vers un facteur de traduction appelé eIF5A, connu pour influencer le comportement mitochondrial.
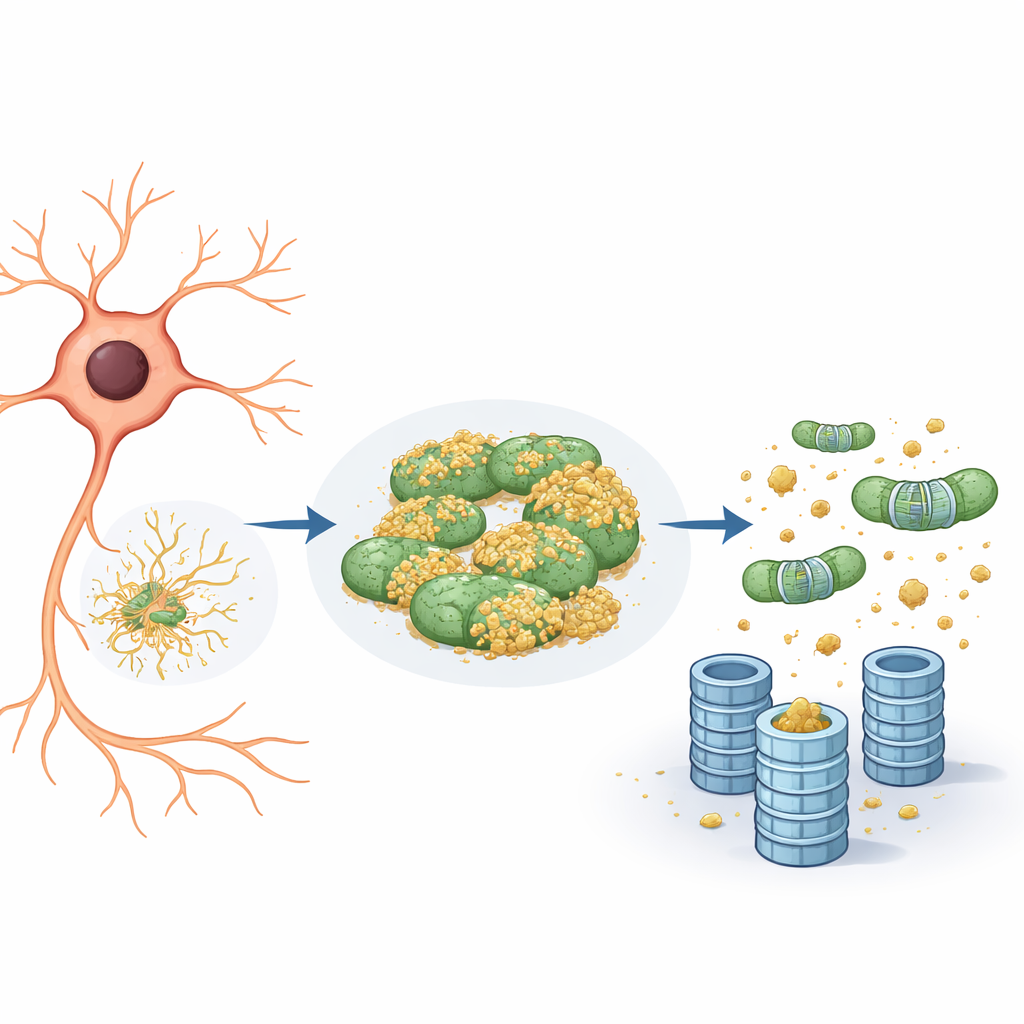
Les mitochondries comme cachette pour les protéines indésirables
Une inspection plus approfondie a révélé que la protéine rapporteur avait tendance à s’associer non seulement au réticulum endoplasmique mais aussi aux mitochondries. Sur les mitochondries, elle restait en grande partie non marquée et donc invisible pour le protéasome. Lorsque l’équipe a réduit l’activité d’eIF5A—soit en en diminuant les niveaux génétiquement, soit en bloquant une modification chimique unique nécessaire à sa fonction—deux choses se sont produites. D’une part, le réseau mitochondrial est devenu plus fragmenté et réorganisé. D’autre part, la protéine rapporteur s’est détachée des mitochondries et sa dégradation s’est accélérée, strictement via le système ubiquitine–protéasome plutôt que par des voies de recyclage cellulaire comme l’autophagie. En substance, les mitochondries agissaient comme un « compartiment refuge », un havre sûr où des protéines problématiques pouvaient éviter d’être marquées et détruites.
Des rapporteurs artificiels aux protéines liées aux maladies
La clé de ce comportement s’est avérée être un motif structural appelé hélice amphipathique—un court segment à la fois partiellement hydrophile et partiellement lipophile qui aide les protéines à adhérer aux membranes. Lorsque les chercheurs ont assoupli cette hélice dans leur rapporteur, la protéine avait moins tendance à se lier aux mitochondries ou à former des agrégats et n’affichait plus d’augmentation de dégradation lorsque eIF5A était bloqué. De façon importante, plusieurs protéines liées aux maladies, notamment l’huntingtine mutante (dans la maladie de Huntington) et l’α‑synucléine mutante (dans la maladie de Parkinson), contiennent également des hélices amphipathiques et sont connues pour se localiser de manière anormale aux mitochondries. Dans des modèles cellulaires exprimant ces protéines, diminuer l’activité d’eIF5A ou perturber autrement le réseau mitochondrial a provoqué la dissociation des protéines pathologiques des mitochondries et leur élimination plus efficace par les protéasomes, avec moins de cellules montrant de gros agrégats.
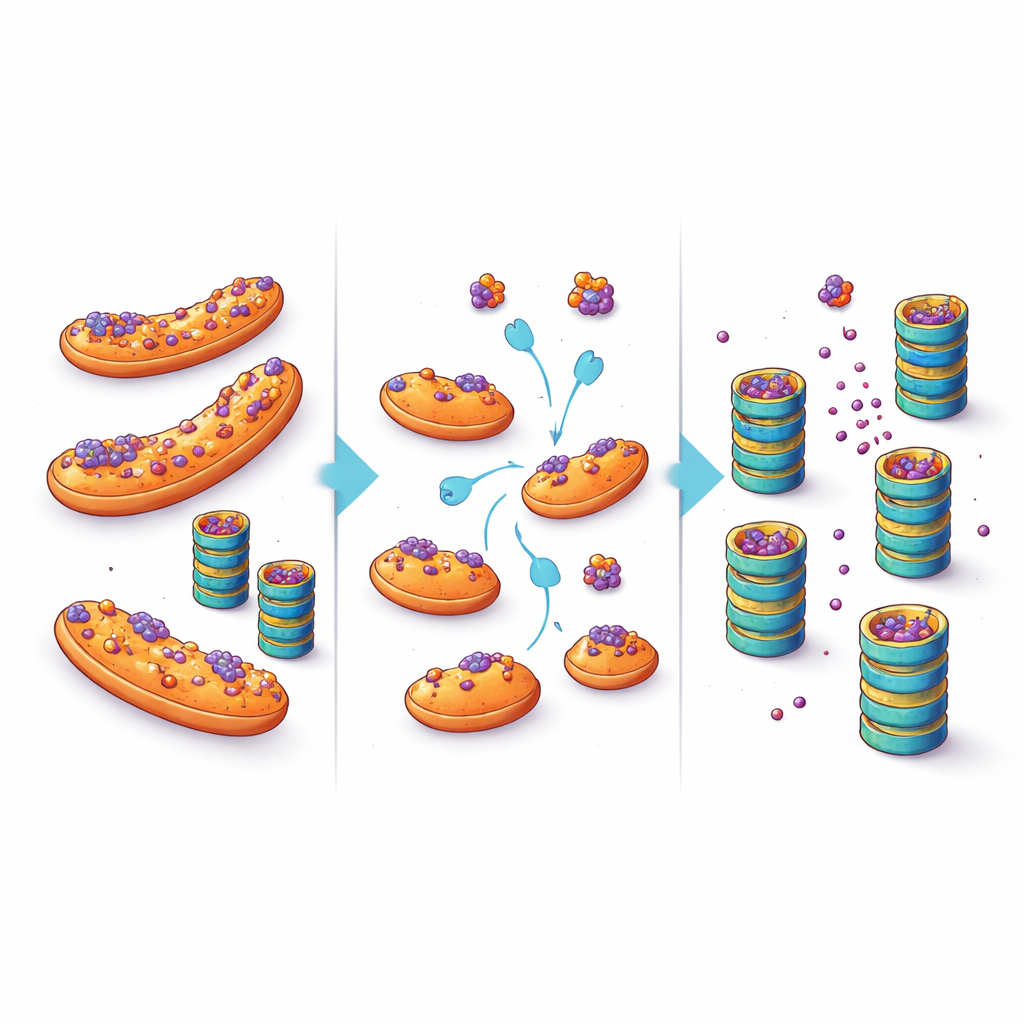
Transformer un refuge cellulaire en opportunité thérapeutique
Ces résultats suggèrent un changement de perspective sur l’accumulation protéique dans les maladies neurodégénératives. Plutôt que de supposer que les broyeurs cellulaires sont simplement dépassés ou défaillants, ce travail met en lumière l’importance de la localisation : lorsque des protéines sujettes à l’agrégation sont stationnées sur les mitochondries, elles sont moins accessibles aux enzymes de contrôle qualité et se dégradent plus lentement. En les poussant hors de ce refuge—par des modifications ciblées de facteurs comme eIF5A ou en empêchant directement leur capacité à s’ancrer sur les mitochondries—il pourrait être possible de réduire les niveaux de protéines toxiques dans les neurones vulnérables. Bien qu’un éventuel traitement doive équilibrer ces interventions avec les nombreuses autres fonctions des mitochondries et d’eIF5A, l’étude ouvre une voie thérapeutique séduisante : au lieu de se contenter de renforcer le broyeur cellulaire, aider les protéines mal repliées à y parvenir.
Citation: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Mots-clés: mitochondries, aggregation protéique, protéasome, neurodégénérescence, eIF5A