Clear Sky Science · es
Las mitocondrias actúan como un compartimento refugio para proteínas propensas a agregarse que impide su degradación eficiente
Por qué importan los cúmulos de proteínas para la salud cerebral
En muchos trastornos cerebrales, como el Alzheimer, el Parkinson y la enfermedad de Huntington, ciertas proteínas pierden su forma correcta y se agrupan dentro de las neuronas. Estos cúmulos pegajosos pueden alterar procesos vitales y, con el tiempo, provocar la muerte celular. Este estudio plantea una pregunta aparentemente sencilla: si las células ya cuentan con potentes sistemas de eliminación de desechos, ¿por qué no eliminan más eficazmente esas proteínas problemáticas? La respuesta conduce a un lugar inesperado dentro de la célula: las mitocondrias, a menudo llamadas las centrales energéticas de la célula.
Los equipos de limpieza celulares y sus límites
Nuestras células fabrican y destruyen proteínas de forma continua. Cuando las proteínas se pliegan mal, una ruta principal de eliminación es el sistema ubiquitina–proteasoma, que funciona como una cinta transportadora con etiquetas y una trituradora. Las proteínas defectuosas se marcan primero con pequeñas moléculas (ubiquitina) y luego se introducen en máquinas en forma de barril (proteasomas) que las descomponen en fragmentos inocuos. Este sistema es especialmente eficaz para detectar proteínas dañadas a tiempo, antes de que se endurezcan en grandes cúmulos insolubles. Sin embargo, en las enfermedades neurodegenerativas los cúmulos siguen acumulándose, aun cuando este sistema de eliminación puede permanecer mayoritariamente funcional. Ese enigma sugiere que el problema puede no residir solo en la potencia de la trituradora, sino también en si la basura llega realmente a ella.
Encontrar interruptores genéticos que modulan la degradación de proteínas
Para explorar qué controla el destino de proteínas propensas a agregarse, los investigadores crearon una línea celular humana especial con una proteína reportera fluorescente diseñada para plegarse mal con facilidad, pero sin ser inmediatamente tóxica. Luego emplearon una pantalla CRISPR–Cas9 a escala del genoma, desactivando miles de genes uno por uno y clasificando las células según la cantidad de reportero defectuoso que acumulaban. Esto les permitió identificar genes que o bien ayudaban a la célula a destruir el reportero o, por el contrario, hacían que persistiera más tiempo. Como era de esperar, muchos aciertos ya eran piezas conocidas de la maquinaria de eliminación de proteínas en la superficie del retículo endoplásmico, un sistema de membranas que también funciona como centro de control de calidad. Pero otro grupo, más sorprendente, apuntó a las mitocondrias y a un factor de traducción llamado eIF5A, conocido por influir en el comportamiento mitocondrial.
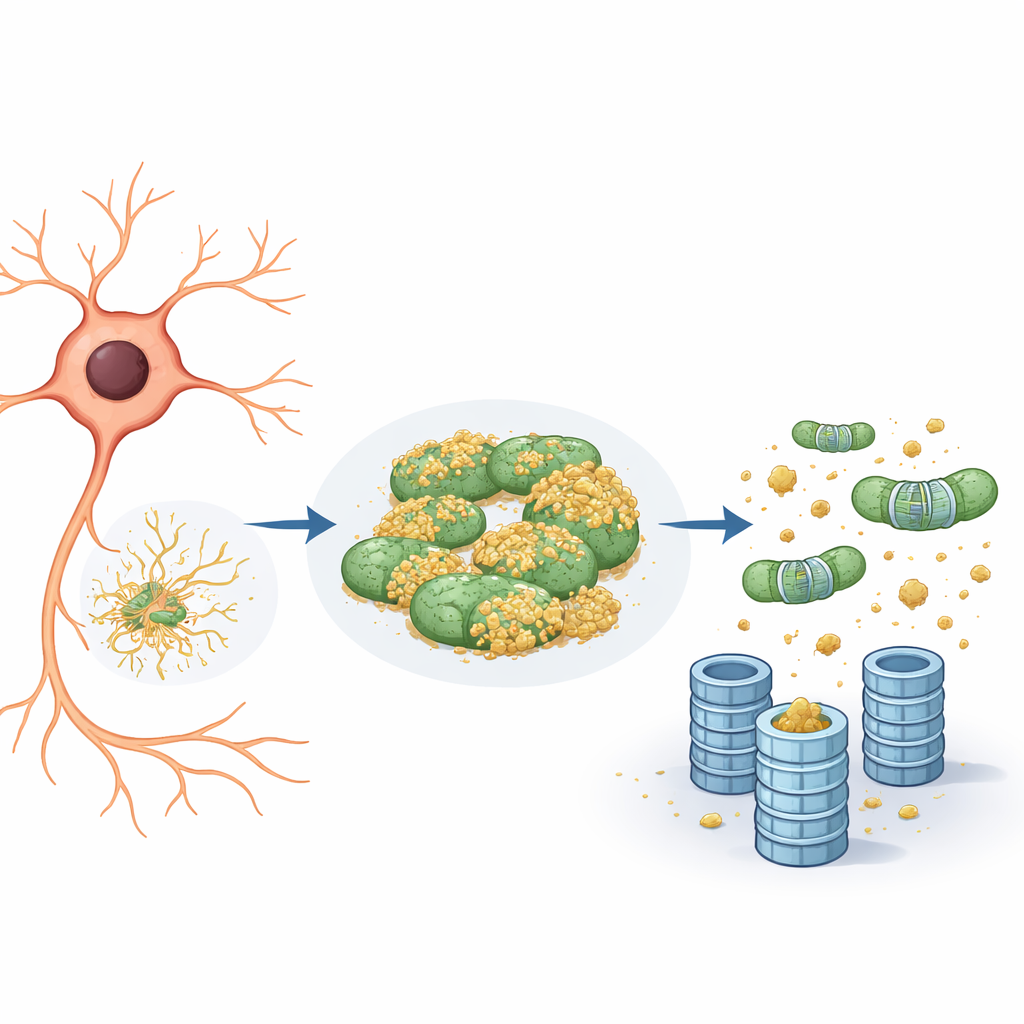
Las mitocondrias como escondite para proteínas dañinas
Una inspección más detallada reveló que la proteína reportera tendía a asociarse no solo con el retículo endoplásmico sino también con las mitocondrias. En las mitocondrias permanecía en gran medida sin marcar y, por tanto, invisible para la trituradora del proteasoma. Cuando el equipo redujo la actividad de eIF5A—ya fuera disminuyendo sus niveles genéticamente o bloqueando una modificación química única que necesita para funcionar—ocurrieron dos cosas. Primero, la red mitocondrial se volvió más fragmentada y se reorganizó. Segundo, la proteína reportera se desprendió de las mitocondrias y su degradación se aceleró, estrictamente a través del sistema ubiquitina–proteasoma y no por vías de reciclaje celular como la autofagia. En esencia, las mitocondrias actuaban como un “compartimento refugio”, un puerto seguro donde las proteínas problemáticas podían evitar ser etiquetadas y destruidas.
De reporteros artificiales a proteínas vinculadas a la enfermedad
La clave de este comportamiento resultó ser un motivo estructural llamado hélice anfipática: un segmento corto, en parte amante del agua y en parte amante de la grasa, que ayuda a las proteínas a adherirse a las membranas. Cuando los investigadores atenuaron esta hélice en su reportero, la proteína tenía menos probabilidad de unirse a las mitocondrias o formar agregados y dejó de mostrar una degradación aumentada cuando se bloqueaba eIF5A. Es importante señalar que varias proteínas relacionadas con enfermedades, incluida la huntingtina mutante (en la enfermedad de Huntington) y la α‑sinucleína mutante (en la enfermedad de Parkinson), también contienen hélices anfipáticas y se sabe que se deslocalizan a las mitocondrias. En modelos celulares que expresaban estas proteínas, disminuir la actividad de eIF5A o perturbar de otro modo la red mitocondrial hizo que las proteínas patológicas se disociaran de las mitocondrias y fueran eliminadas con mayor eficacia por los proteasomas, con menos células mostrando grandes agregados.
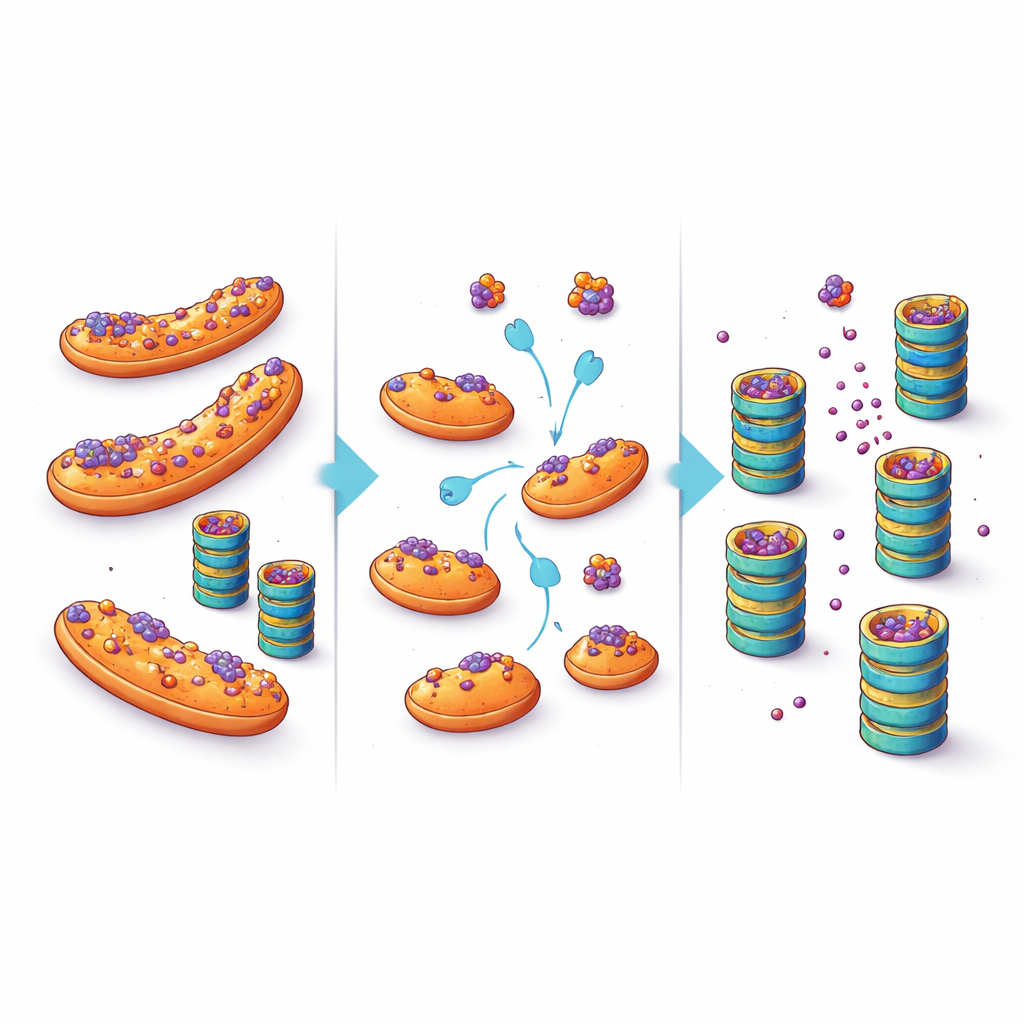
Convertir un refugio celular en una oportunidad terapéutica
Estos hallazgos sugieren un cambio en la forma de concebir la acumulación de proteínas en la neurodegeneración. En lugar de suponer que las trituradoras de la célula están simplemente sobrepasadas o rotas, este trabajo destaca la localización como un factor crucial: cuando las proteínas propensas a agregarse se estacionan en las mitocondrias, son menos accesibles a las enzimas de control de calidad y se degradan más lentamente. Al empujarlas fuera de este refugio—mediante cambios dirigidos en factores como eIF5A o interfiriendo directamente con su capacidad de anclarse a las mitocondrias—podría ser posible reducir los niveles de proteínas tóxicas dentro de las neuronas vulnerables. Aunque cualquier tratamiento futuro tendría que equilibrar tales intervenciones con las muchas otras funciones de las mitocondrias y de eIF5A, el estudio abre una vía terapéutica sugerente: en lugar de limitarse a aumentar la potencia de la trituradora celular, ayudar a que las proteínas mal plegadas lleguen hasta ella.
Cita: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Palabras clave: mitocondrias, agregación de proteínas, proteasoma, neurodegeneración, eIF5A