Clear Sky Science · nl
Mitochondriën dienen als toevluchtsoord voor aggregatie‑gevoelige eiwitten en beletten efficiënte afbraak
Waarom eiwitklonters ertoe doen voor de gezondheid van de hersenen
Bij veel hersenaandoeningen zoals de ziekte van Alzheimer, Parkinson en Huntington verliezen bepaalde eiwitten hun juiste vouwing en klonteren samen binnen zenuwcellen. Deze kleverige ophopingen kunnen vitale processen verstoren en uiteindelijk cellen doden. Deze studie stelt een schijnbaar simpele vraag: als cellen al krachtige opruimsystemen hebben, waarom ruimen ze deze probleem‑eiwitten dan niet efficiënter op? Het antwoord leidt naar een onverwachte plek in de cel: de mitochondriën, vaak de energiecentrales van de cel genoemd.
Cellulaire opruimploegen en hun beperkingen
Onze cellen maken en vernietigen voortdurend eiwitten. Als eiwitten verkeerd vouwen, is een belangrijke afbraakroute het ubiquitine–proteasoomsysteem, dat werkt als een geëtiketteerde vuilnisbelt met een versnipperaar. Misfunctionerende eiwitten worden eerst gemarkeerd met kleine moleculen (ubiquitine) en vervolgens in tonvormige machines (proteasomen) gevoerd die ze in onschadelijke stukjes kauwen. Dit systeem is vooral goed in het vroegtijdig herkennen van beschadigde eiwitten, voordat ze uitharden tot grote, onoplosbare klonters. Toch hopen zich in neurodegeneratieve ziektes klonters op, ook al kan dit afbraaksysteem grotendeels functioneel blijven. Die puzzel suggereert dat het probleem niet alleen in de kracht van de versnipperaar ligt, maar ook in de vraag of het vuil daadwerkelijk bij die versnipperaar terechtkomt.
Genetische schakelaars vinden die eiwitafbraak veranderen
Om te onderzoeken wat het lot van aggregatie‑gevoelige eiwitten bepaalt, maakten de onderzoekers een speciale menselijke cellijn met een fluorescerende rapportereiwit dat makkelijk verkeerd vouwt, maar niet direct toxisch is. Ze gebruikten vervolgens een genoom‑brede CRISPR–Cas9‑screen, schakelden duizenden genen één voor één uit en sorteerden cellen op basis van hoeveel van het defecte rapportereiwit ze ophoopten. Zo konden ze genen aanwijzen die de afbraak van het rapportereiwit bevorderden of, omgekeerd, ervoor zorgden dat het langer bleef hangen. Zoals verwacht waren veel getroffen genen al bekende onderdelen van het eiwit‑afvalmachinerie op het oppervlak van het endoplasmatisch reticulum, een membraansysteem dat ook als kwaliteitscontrolecentrum fungeert. Maar een andere, verrassende groep genen wees naar de mitochondriën en naar een translatiefactor genaamd eIF5A, die bekendstaat om zijn invloed op mitochondriale functies.
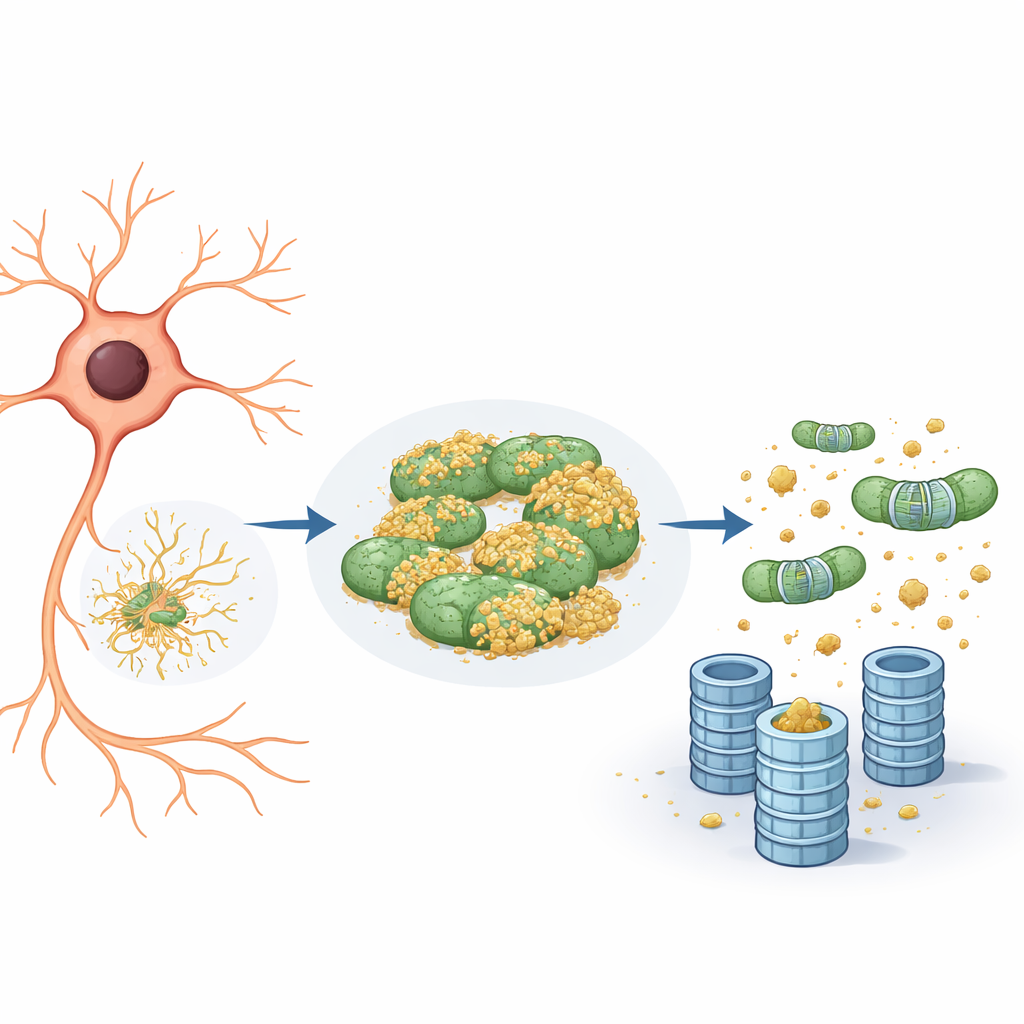
Mitochondriën als verstopplek voor foutieve eiwitten
Nauwkeuriger onderzoek toonde aan dat het rapportereiwit zich niet alleen aan het endoplasmatisch reticulum hechtte, maar ook aan mitochondriën. Op de mitochondriën bleef het grotendeels ongetagd en daardoor onzichtbaar voor het proteasoom. Toen het team de activiteit van eIF5A verminderde — hetzij door het genetisch te verlagen, hetzij door een unieke chemische modificatie die het nodig heeft te blokkeren — gebeurde er twee dingen. Ten eerste raakte het mitochondriale netwerk meer gefragmenteerd en gereorganiseerd. Ten tweede liet het rapportereiwit de mitochondriën los en versnelde de afbraak, strikt via het ubiquitine–proteasoomsysteem en niet via cellulaire recyclingroutes zoals autofagie. In wezen fungeerden mitochondriën als een “toevluchtsoord”: een veilige haven waar probleem‑eiwitten konden ontsnappen aan tagging en vernietiging.
Van kunstmatige rapportoren naar ziektegerelateerde eiwitten
De sleutel tot dit gedrag bleek een structureel motief te zijn, een amphipatische helix — een korte, deels water‑liefhebbende en deels vet‑liefhebbende segment dat eiwitten helpt aan membranen te blijven plakken. Toen de onderzoekers deze helix in hun rapporter verzwakten, was het eiwit minder geneigd zich aan mitochondriën te binden of aggregaten te vormen en vertoonde het geen versnelde afbraak meer wanneer eIF5A werd geblokkeerd. Belangrijk is dat meerdere ziektegerelateerde eiwitten, waaronder mutant huntingtine (bij de ziekte van Huntington) en mutant α‑synucleïne (bij de ziekte van Parkinson), ook amphipatische helices bevatten en bekendstaan om hun mislokalisatie naar mitochondriën. In celmodellen die deze eiwitten tot expressie brachten, leidde het verlagen van eIF5A‑activiteit of anderszins verstoren van het mitochondriale netwerk ertoe dat de ziekte‑eiwitten losraakten van mitochondriën en efficiënter door proteasomen werden geklaard, met minder cellen die grote aggregaten lieten zien.
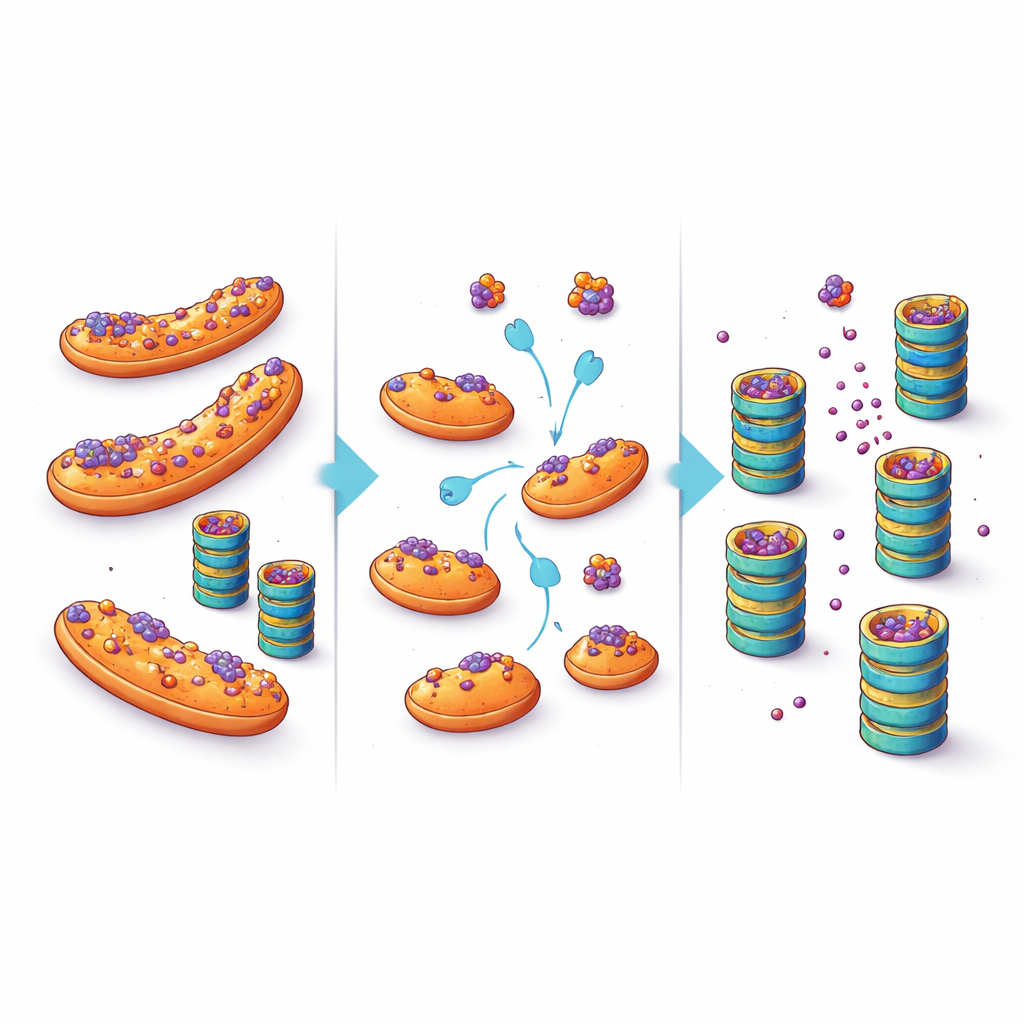
Een cellaire toevlucht omzetten in therapeutische kans
Deze bevindingen suggereren een verschuiving in hoe we denken over eiwitophoping bij neurodegeneratieve ziekten. In plaats van aan te nemen dat de cellulaire versnippers simpelweg overweldigd of kapot zijn, benadrukt dit werk locatie als een cruciale factor: wanneer aggregatie‑gevoelige eiwitten op mitochondriën geparkeerd staan, zijn ze minder toegankelijk voor kwaliteitszorg‑enzymen en worden ze langzamer afgebroken. Door ze weg te duwen uit dit toevluchtsoord — via gerichte veranderingen in factoren zoals eIF5A of door direct hun vermogen te verstoren zich aan mitochondriën te hechten — kan het mogelijk zijn de niveaus van toxische eiwitten in kwetsbare neuronen te verlagen. Hoewel een toekomstige behandeling zulke interventies zou moeten afwegen tegen de vele andere rollen van mitochondriën en eIF5A, opent de studie een aantrekkelijke therapeutische route: in plaats van alleen de kracht van de cellulaire versnipperaar op te voeren, help misgevouwen eiwitten hun weg ernaartoe te vinden.
Bronvermelding: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Trefwoorden: mitochondriën, eiwitaggregatie, proteasoom, neurodegeneratie, eIF5A