Clear Sky Science · he
המיטוכונדריה משמשת כמחסן זמני לחלבונים הנוטים להצטברות ומפריעה לפירוק יעיל
מדוע גושי חלבון חשובים לבריאות המוח
בהפרעות מוחיות רבות, כמו מחלת אלצהיימר, פרקינסון והנטינגטון, חלבונים מסוימים מאבדים את קיפולם התקין ומצטברים בתוך תאי עצב. גושים דביקים אלה עלולים להפריע לתהליכים חיוניים ולבסוף להרוג את התאים. המחקר שואל שאלה שנראית פשוטה: אם לתאים כבר קיימים מערכות פינוי חזקות, מדוע הם לא מיפטרים ביעילות מחלבונים הבעיתיים האלה? התשובה מובילה למקום בלתי צפוי בתוך התא — המיטוכונדריה, שמכונה לעתים תחנות הכוח של התא.
צוותי ניקיון תאיים והמגבלות שלהם
התאים שלנו מייצרים ומפרקים חלבונים באופן רציף. כאשר חלבונים מתקפלים באופן שגוי, נתיב פירוק מרכזי הוא מערכת האוביקוויטין–פרוטאוזום, שפועלת כמו קונוויייר של זיהוי אשפה וגריסה. חלבונים בעיתיים מוסמנים תחילה במולקולות קטנות (אוביקוויטין) ואז מוזנים למכונות בצורת חבית (פרוטאוזומים) שמפוררות אותם לחתיכות חסרות נזק. המערכת הזו יעילה במיוחד בלתפוס חלבונים פגומים בשלב מוקדם, לפני שהם מתקשים לגושים גדולים שאינם מסיסים. עם זאת, בהפרעות ניווניות צברי חלבון עדיין מצטברים, אף על פי שמערכת הפירוק עשויה להישאר פעילה במידה ניכרת. התעלומה הזו מרמזת שהבעיה אינה רק בחוזק ה'מגרסה', אלא גם בשאלה האם האשפה מגיעה אליה.
חיפוש מתגים גנטיים שמשנים את פירוק החלבון
כדי לחקור מה שולט בגורל חלבונים נוטי-הצטברות, החוקרים יצרו קו תאי אנושי מיוחד עם חלבון דיווח זוהר שמיועד להתקפל בקלות, אך ללא רעילות מיידית. הם השתמשו לאחר מכן בסקר CRISPR–Cas9 ברמת הגנום, כבוי אלפי גנים אחד-אחד ומיינו תאים לפי כמות חלבון הדיווח הבעייתי שהצטברה בהם. כך הצליחו לזהות גנים שעזרו לתא לפרק את הדיווח או, להפך, גרמו לו להחזיק מעמד זמן רב יותר. כצפוי, ממצאים רבים היו חלקים ידועים ממכונת הפינוי שעל גבי הרשת האנדופלסמית, מערכת ממברנית שגם משמשת כמרכז בקרת איכות. אך קבוצה נוספת ומפתיעה של גנים הכוונה למיטוכונדריה ולפקטור התרגום eIF5A, הידוע בהשפעתו על תפקוד המיטוכונדריה.
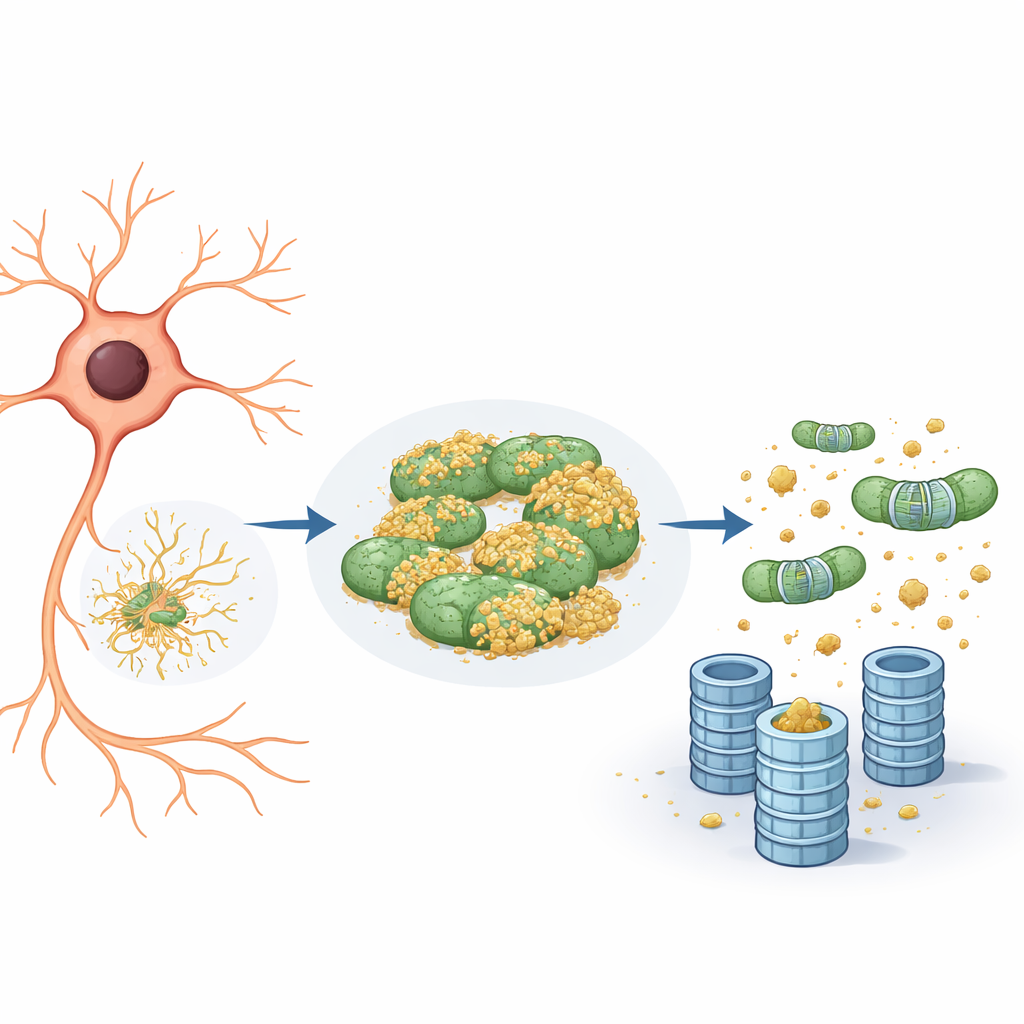
מיטוכונדריה כמקום מחבואה לחלבונים בעיתיים
בדיקה מעמיקה הראתה שחלבון הדיווח נטה להתייצב לא רק על הרשת האנדופלסמית אלא גם על המיטוכונדריה. על המיטוכונדריה הוא נשאר ברובו ללא סימון ולכן בלתי נראה לפרוטאוזום. כאשר הצוות הקטין את פעילות eIF5A — בין אם בהורדת רמותיו גנטית ובין אם על-ידי חסימת שינוי כימי ייחודי הנדרש לתפקודו — קרו שני דברים. ראשית, רשת המיטוכונדריה הפכה למפוצלת יותר ולאורגן באופן שונה. שנית, חלבון הדיווח התנתק מהמוחיטוכונדריה ופירוקו הואץ, באופן שתלוי לחלוטין במערכת האוביקוויטין–פרוטאוזום ולא בדרכי מחזור תאיות כמו אוטופאגיה. מהותית לכך, המיטוכונדריה פעלה כ"מחסן זמני" — נווה מפרץ בטוח שבו חלבונים בעיתיים יכלו להתחמק מסימון והרס.
מדיווחים מלאכותיים לחלבונים הקשורים למחלה
המפתח להתנהגות הזו התגלה כמוטיב מבני הנקרא הליקס אמפיפתי — מקטע קצר שאוהב חלקית מים וחלקית שומן ועוזר לחלבונים להיצמד לממברנות. כאשר החוקרים 'הריככו' את ההליקס הזה בחלבון הדיווח שלהם, החלבון הפך לפחות נוטה להיקשר למיטוכונדריה או ליצור אגגרגטים ולא הראה פירוק מוגבר כאשר eIF5A נחסם. חשוב לציין שמספר חלבונים הקשורים למחלות, כולל huntingtin המוטנטי (במחלת הנטינגטון) וα‑synuclein המוטנטי (במחלת פרקינסון), מכילים גם הם הליקסים אמפיפתיים ומוכרים כמתמזגים למיטוכונדריה. במודלים תאיים שמבטאים חלבונים אלה, הורדת פעילות eIF5A או הזזת רשת המיטוכונדריה גרמה לחלבוני המחלה להתנתק מהמיטוכונדריה ולהיות מנוקים ביעילות רבה יותר על ידי הפרוטאוזומים, כאשר פחות תאים הציגו אגגרגטים גדולים.
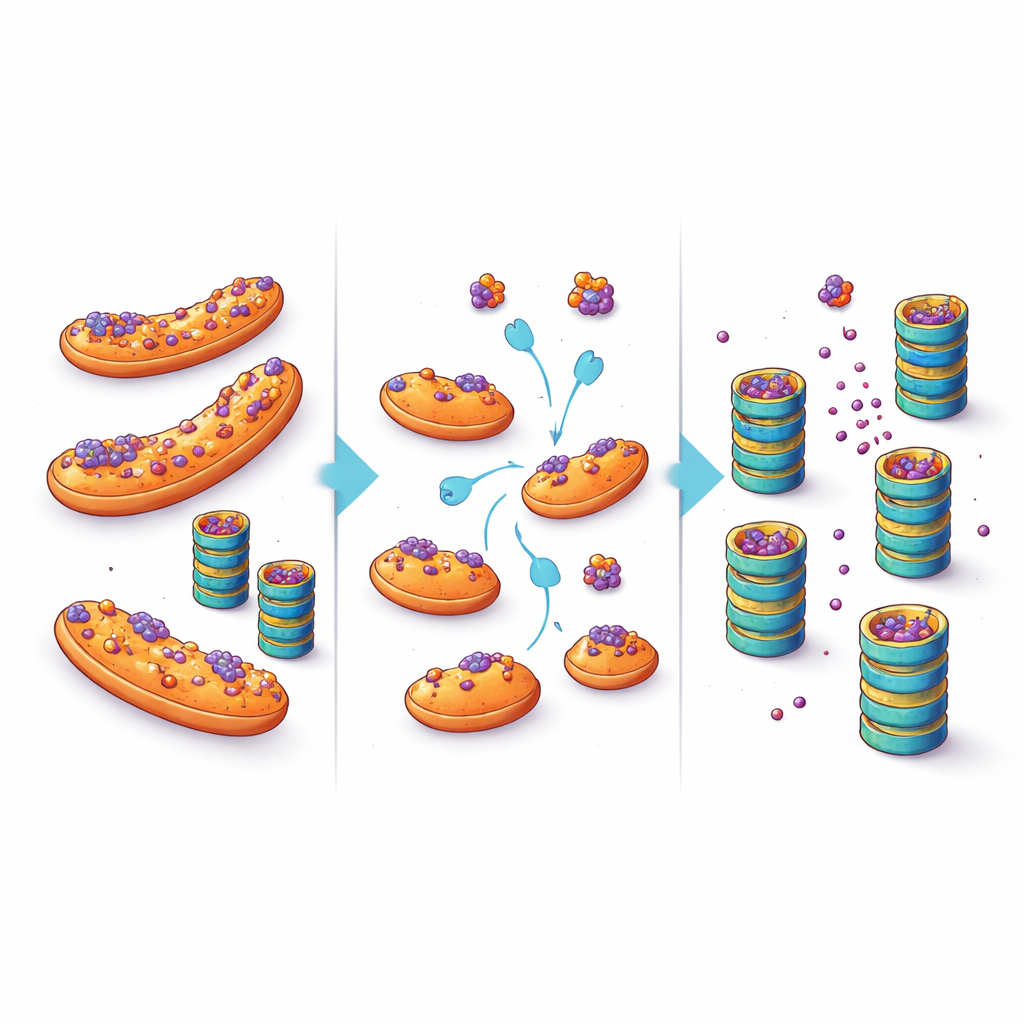
הפיכת מקלט תאי להזדמנות טיפולית
ממצאים אלה מציעים שינוי באופן שבו אנו מתייחסים להצטברות חלבונים במחלות ניווניות. במקום להניח שמכונות הגריסה של התא פשוט מוצפות או שבורות, עבודה זו מדגישה את המיקום כגורם מכריע: כאשר חלבונים נוטי-הצטברות מוסטלים על המיטוכונדריה, הם פחות נגישים לאנזימי בקרת האיכות ומתפרקים לאט יותר. על-ידי דחיפתם הרחק ממקלט זה — באמצעות שינויים ממוקדים בפקטורים כמו eIF5A או על-ידי התערבות ישירה ביכולתם לעגן על המיטוכונדריה — ייתכן שניתן להוריד את רמות החלבונים הרעילים בתוך נוירונים פגיעים. אף שתרופות עתידיות יידרשו לאזן התערבויות אלה מול התפקידים הרבים האחרים של המיטוכונדריה ו-eIF5A, המחקר פותח נתיב טיפולי מפתה: במקום רק להגביר את כוח ה'מגרסה' התאית, סייעו לחלבונים המתקפלים באופן שגוי למצוא את דרכם אליה.
ציטוט: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
מילות מפתח: מיטוכונדריה, הצטברות חלבונים, פרוטאוזום, ניורודגנרציה, eIF5A