Clear Sky Science · ru
Митохондрии служат укрытием для склонных к агрегации белков, мешая их эффективному разрушению
Почему скопления белков важны для здоровья мозга
При многих заболеваний мозга, таких как болезнь Альцгеймера, Паркинсона и Гентингтона, определённые белки теряют правильную трёхмерную структуру и скапливаются в виде слипшихся агрегаций внутри нейронов. Эти липкие скопления нарушают жизненно важные процессы и в конечном счёте приводят к гибели клеток. В исследовании поставлен на первый взгляд простой вопрос: если у клеток уже есть мощные механизмы утилизации «мусора», почему они не избавляются от проблемных белков эффективнее? Ответ приводит в неожиданное место внутри клетки — в митохондрии, часто называемые энергетическими станциями клетки.
Клеточные «уборщики» и их пределы
Наши клетки постоянно синтезируют и уничтожают белки. Когда белки неправильно сворачиваются, одним из основных путей утилизации является система убиквитин–протеасома, которая действует как конвейер с маркировкой мусора и «шредером». Непорядочные белки сначала помечаются небольшими молекулами (убиквитином), а затем подаются в бочкообразные комплексы (протеасомы), которые разрушают их на безвредные фрагменты. Эта система особенно эффективна на ранних стадиях — она ловит повреждённые белки до того, как те затвердевают в крупные нерастворимые сгустки. Тем не менее при нейродегенеративных заболеваниях агрегаты продолжают накапливаться, хотя сама система утилизации может оставаться в основном работоспособной. Эта загадка указывает, что проблема заключается не только в мощи «шредера», но и в том, достигает ли «мусор» вообще до него.
Поиск генетических переключателей, меняющих распад белков
Чтобы выяснить, что определяет судьбу склонных к агрегации белков, исследователи создали особую линию человеческих клеток с флуоресцентным репортерным белком, который легко неправильно сворачивается, но сам по себе не был немедленно токсичен. Затем они провели геномный скрин CRISPR–Cas9, поочерёдно выключая тысячи генов и сортируя клетки по тому, сколько дефектного репортера в них накапливается. Это позволило выявить гены, которые либо способствуют разрушению репортера, либо, напротив, удлиняют его присутствие. Как и ожидалось, многие «попадания» были уже известными компонентами системы утилизации на поверхности эндоплазматического ретикулума — мембранной системы, выполняющей также функции контроля качества. Но другая, более неожиданная группа генов указывала на митохондрии и на фактор трансляции eIF5A, известный тем, что влияет на поведение митохондрий.
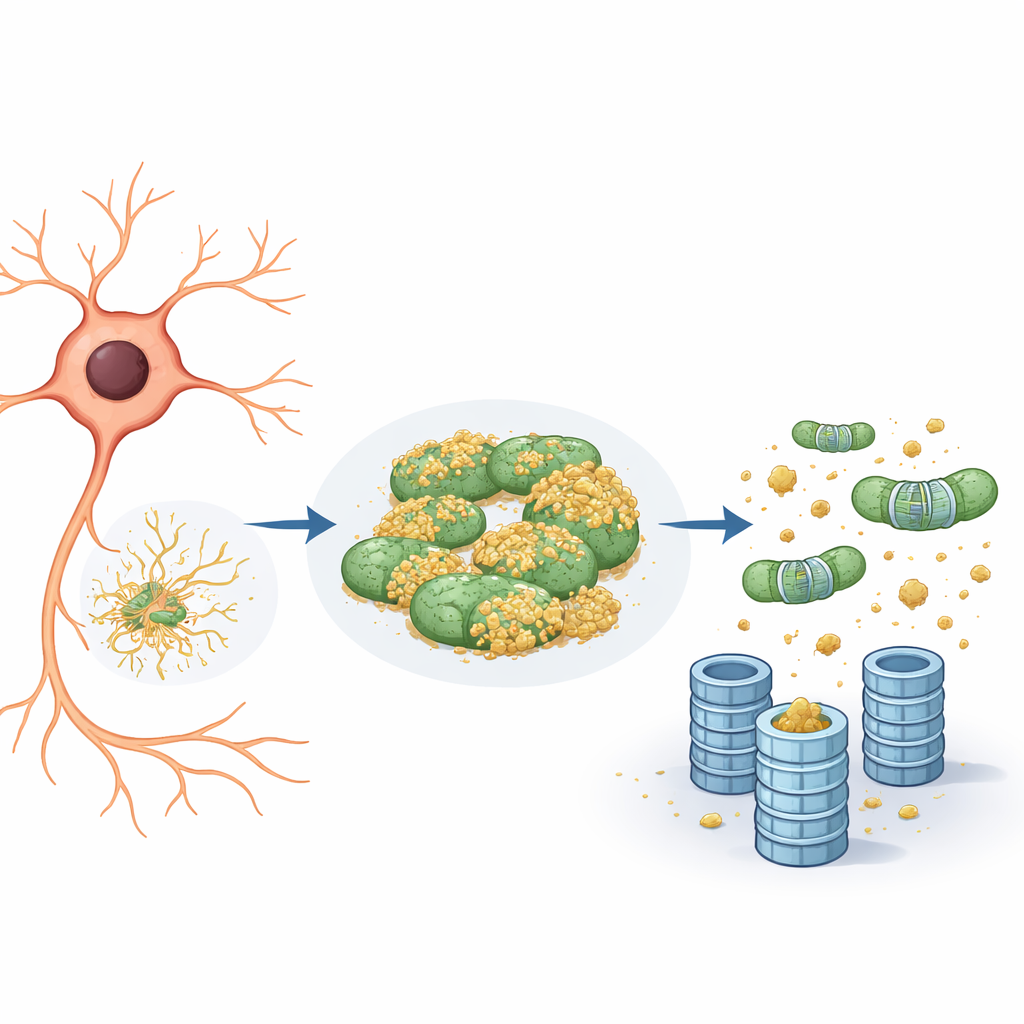
Митохондрии как укрытие для «плохих» белков
Более детальное изучение показало, что репортерный белок склонен ассоциироваться не только с эндоплазматическим ретикулумом, но и с митохондриями. На митохондриях он оставался в основном непомеченным и, следовательно, «невидимым» для протеасом. Когда команда снизила активность eIF5A — либо уменьшив его уровни генетически, либо блокируя уникальную химическую модификацию, необходимую для его функционирования — произошли две вещи. Во‑первых, митохондриальная сеть стала более фрагментированной и реорганизовалась. Во‑вторых, репортер открепился от митохондрий, и его разрушение ускорилось, причём строго через систему убиквитин–протеасома, а не через пути клеточного переработки вроде аутофагии. По сути, митохондрии выступали как «укрывающий компартмент» — безопасная гавань, где проблемные белки могли избегать пометки и уничтожения.
От искусственных репортеров к белкам, связанным с болезнями
Ключ к этому поведению оказался в структурном мотиве, называемом амфифатической спиралью — коротком сегменте, частично гидрофильном и частично гидрофобном, который помогает белкам прикрепляться к мембранам. Когда исследователи «смягчили» эту спираль в своём репортере, белок реже связывался с митохондриями или образовывал агрегаты и перестал демонстрировать усиленное разрушение при блокировке eIF5A. Важно, что несколько белков, связанных с заболеваниями — включая мутантный хантингтин (при болезни Гентингтона) и мутантный α‑синуклеин (при болезни Паркинсона) — также содержат амфифатические спирали и известны своим смещением локализации к митохондриям. В клеточных моделях, экспрессирующих эти белки, снижение активности eIF5A или иное нарушение митохондриальной сети приводило к их диссоциации от митохондрий и более эффективной очистке протеасомами, при этом меньше клеток содержали крупные агрегаты.
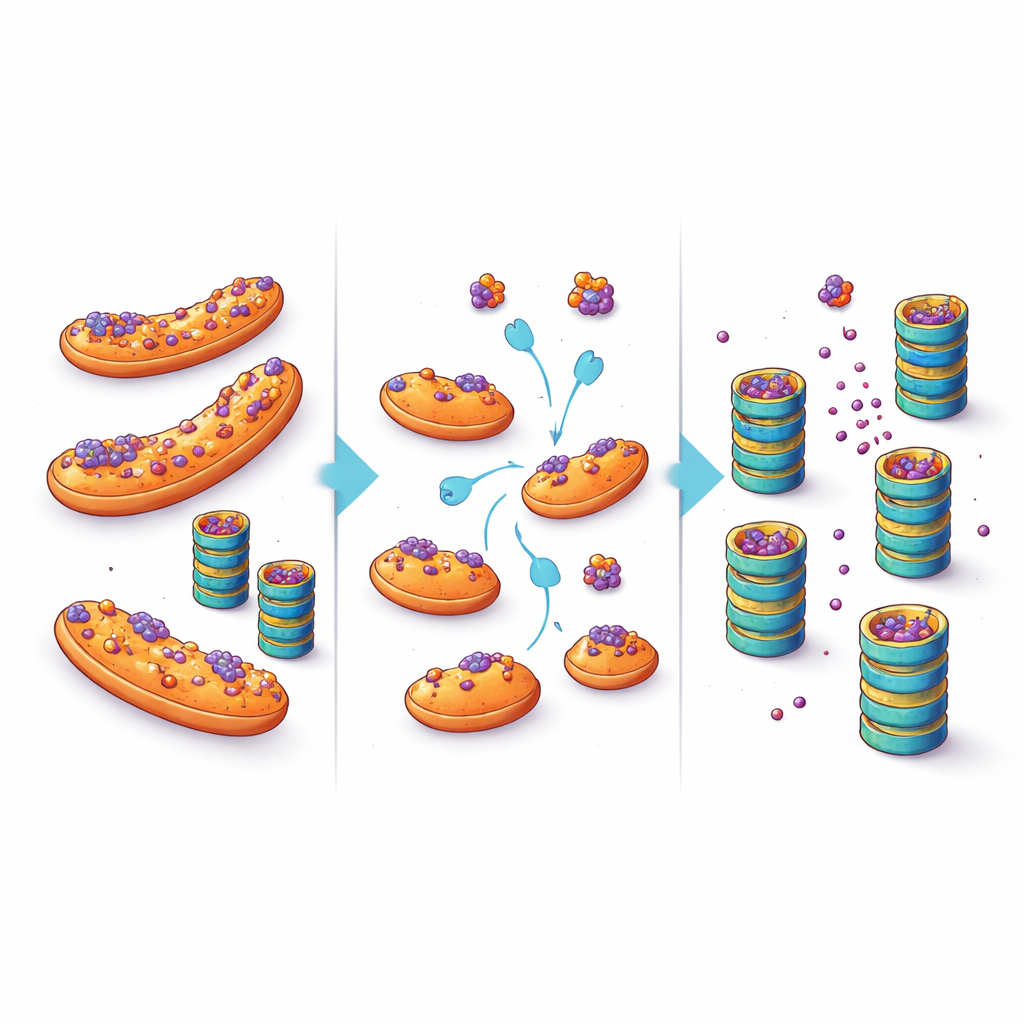
Преобразование клеточного убежища в терапевтическую возможность
Эти результаты предлагают смещение в понимании накопления белков при нейродегенеративных заболеваниях. Вместо того чтобы предполагать, что «шредеры» клетки просто перегружены или сломаны, работа подчёркивает местоположение как решающий фактор: когда склонные к агрегации белки «припаркованы» на митохондриях, они менее доступны для ферментов контроля качества и разрушаются медленнее. Сдвинув их с этого убежища — посредством целевых изменений факторов, таких как eIF5A, или прямо вмешиваясь в их способность прикрепляться к митохондриям — можно потенциально снизить уровни токсичных белков в уязвимых нейронах. Хотя любые будущие лечебные подходы должны будут взвесить такие вмешательства с учётом множества других ролей митохондрий и eIF5A, исследование открывает заманчивую терапевтическую дорогу: вместо того чтобы только усиливать «мощность» клеточного шредера, помочь неправильно свернутым белкам добраться до него.
Цитирование: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Ключевые слова: митохондрии, агрегация белков, протеасома, нейродегенерация, eIF5A