Clear Sky Science · sv
Mitokondrier fungerar som ett tillflyktsrum för aggregeringsbenägna proteiner som hindrar effektiv nedbrytning
Varför proteinklumpar spelar roll för hjärnhälsan
I många hjärnsjukdomar som Alzheimers, Parkinsons och Huntingtons sjukdom förlorar vissa proteiner sin korrekta form och klibbar ihop inuti nervceller. Dessa klibbiga klumpar kan störa viktiga processer och så småningom döda cellerna. Denna studie ställer en bedrägligt enkel fråga: om celler redan har kraftfulla sopsystem, varför blir de inte av med de här problemproteinerna mer effektivt? Svaret leder till en oväntad plats i cellen — mitokondrierna, ofta kallade cellens kraftverk.
Cellernas städpatruller och deras gränser
Våra celler tillverkar och bryter kontinuerligt ner proteiner. När proteiner felveckas är ett huvudsakligt avfallsspår ubiquitin–proteasomsystemet, som fungerar som ett märkt-sopor-och-kvarnband. Misskötta proteiner märks först med små molekyler (ubiquitin) och matas sedan in i tunnformade maskiner (proteasomer) som tuggar sönder dem till ofarliga bitar. Det här systemet är särskilt bra på att fånga skadade proteiner tidigt, innan de hårdnar till stora, olösliga klumpar. Ändå samlas klumpar i neurodegenerativa sjukdomar, trots att detta avfallssystem ofta förblir till stor del funktionellt. Denna gåta tyder på att problemet inte bara ligger i kvarnens styrka, utan också i om skräpet faktiskt når den.
Att hitta genetiska strömbrytare som ändrar proteinnedbrytning
För att undersöka vad som styr ödet för klumpbenägna proteiner skapade forskarna en specialiserad mänsklig cellinje med ett fluorescerande rapportprotein utformat för att lätt felvecka, men utan att vara omedelbart giftigt. De använde sedan en genombred CRISPR–Cas9-skärm och slog av tusentals gener en efter en och sorterade cellerna efter hur mycket av det defekta rapportproteinet de samlat på sig. Detta gjorde det möjligt att identifiera gener som antingen hjälpte cellen att förstöra rapporten eller, tvärtom, fick den att dröja kvar längre. Som förväntat var många träffar redan kända delar av proteinavfallsmaskineriet på ytan av det endoplasmatiska retiklet, ett membransystem som också fungerar som ett kvalitetskontrollcenter. Men en annan, mer överraskande grupp gener pekade på mitokondrierna och på en translationsfaktor kallad eIF5A, känd för att påverka mitokondriernas beteende.
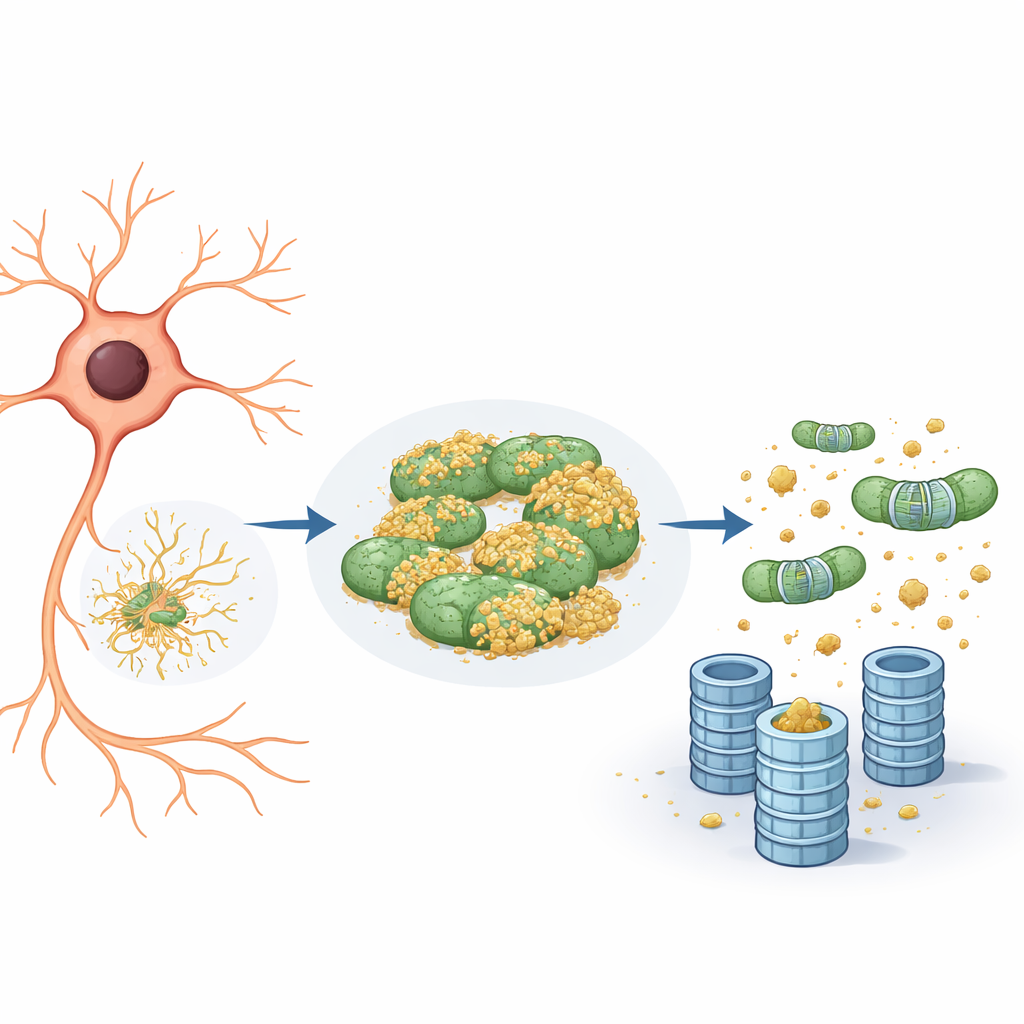
Mitokondrier som ett gömställe för skadliga proteiner
Närmare granskning visade att rapportproteinet tenderade att associera sig inte bara med det endoplasmatiska retiklet utan även med mitokondrier. På mitokondrierna förblev det till stor del omärkt och därmed osynligt för proteasomens kvarn. När teamet minskade aktiviteten hos eIF5A — antingen genom att sänka dess nivåer genetiskt eller genom att blockera en unik kemisk modifiering som det behöver för att fungera — hände två saker. För det första blev mitokondrienätverket mer fragmenterat och omorganiserat. För det andra lossnade rapportproteinet från mitokondrierna och dess nedbrytning gick snabbare, strikt genom ubiquitin–proteasomsystemet snarare än genom cellulära återvinningsvägar som autofagi. I praktiken fungerade mitokondrierna som ett "tillflyktsrum", en säker hamn där problematiska proteiner kunde undvika att bli märkta och förstörda.
Från konstgjorda rapporter till sjukdomsrelaterade proteiner
Nyckeln till detta beteende visade sig vara ett strukturellt motiv kallat en amphipatisk helix — en kort, delvis vattenälskande och delvis fettälskande sekvens som hjälper proteiner att fästa vid membraner. När forskarna försvagade denna helix i sin rapport var proteinet mindre benäget att binda till mitokondrier eller bilda aggregationer och visade inte längre ökad nedbrytning när eIF5A blockerades. Viktigt är att flera sjukdomsrelaterade proteiner, inklusive muterat huntingtin (i Huntingtons sjukdom) och muterat α‑synuklein (i Parkinsons sjukdom), också innehåller amphipatiska helixar och är kända för att fellokaliseras till mitokondrier. I cellmodeller som uttryckte dessa proteiner ledde sänkt eIF5A-aktivitet eller annan störning av mitokondrienätverket till att sjukdomsproteinerna dissocierade från mitokondrier och rensades mer effektivt av proteasomer, med färre celler som visade stora aggregationer.
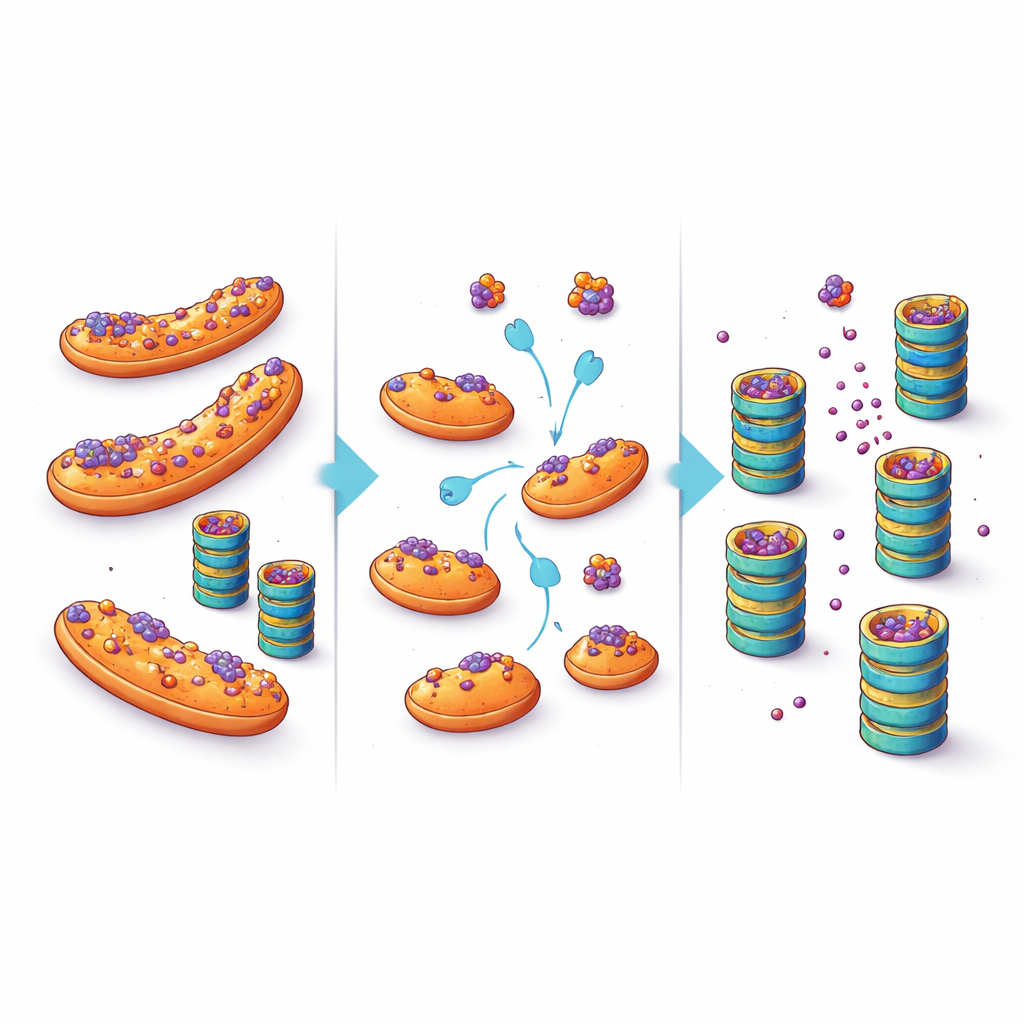
Att förvandla ett cellulärt tillflyktsrum till en terapeutisk möjlighet
Dessa fynd antyder ett skifte i hur vi tänker kring proteinansamling i neurodegenerativa sjukdomar. I stället för att anta att cellens kvarnar helt enkelt är överväldigade eller trasiga framhäver detta arbete platsen som en avgörande faktor: när aggregeringsbenägna proteiner parkerar på mitokondrier är de mindre åtkomliga för kvalitetskontrollenzymer och bryts ner långsammare. Genom att knuffa dem bort från detta tillflyktsrum — genom riktade förändringar i faktorer som eIF5A eller genom att direkt störa deras förmåga att docka vid mitokondrier — kan det vara möjligt att sänka nivåerna av giftiga proteiner i sårbara neuroner. Även om eventuell framtida behandling måste balansera sådana ingrepp mot mitokondriernas och eIF5A:s många andra roller öppnar studien en lockande terapeutisk väg: i stället för att bara öka kraften i den cellulära kvarnen, hjälp felveckade proteiner att hitta dit.
Citering: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Nyckelord: mitokondrier, proteinaggregation, proteasom, neurodegeneration, eIF5A