Clear Sky Science · pt
As mitocôndrias servem como compartimento de refúgio para proteínas propensas à agregação, dificultando a degradação eficiente
Por que os aglomerados de proteínas importam para a saúde do cérebro
Em muitos transtornos cerebrais, como Alzheimer, Parkinson e Huntington, certas proteínas perdem sua conformação adequada e se aglomeram dentro dos neurônios. Esses aglomerados pegajosos podem atrapalhar processos vitais e, eventualmente, matar as células. Este estudo faz uma pergunta aparentemente simples: se as células já dispõem de sistemas poderosos de descarte, por que não eliminam essas proteínas problemáticas com mais eficiência? A resposta aponta para um lugar inesperado dentro da célula — as mitocôndrias, frequentemente chamadas de usinas de energia celular.
As equipes de limpeza celular e seus limites
Nossas células estão constantemente sintetizando e degradando proteínas. Quando proteínas se dobram de forma incorreta, uma das principais rotas de descarte é o sistema ubiquitina–proteassoma, que funciona como um sistema de marcação de lixo seguido por um triturador. Proteínas com problemas são primeiro marcadas com pequenas moléculas (ubiquitina) e depois alimentadas em máquinas em forma de tambor (proteassomas) que as degradam em fragmentos inofensivos. Esse sistema é especialmente eficaz em detectar proteínas danificadas precocemente, antes que se solidifiquem em grandes aglomerados insolúveis. Ainda assim, em doenças neurodegenerativas, aglomerados se acumulam, mesmo quando esse sistema de descarte permanece em grande parte funcional. Esse enigma sugere que o problema pode não residir apenas na força do triturador, mas também em o lixo realmente chegar até ele.
Identificando chaves genéticas que alteram a degradação de proteínas
Para explorar o que controla o destino de proteínas propensas a aglomerar, os pesquisadores criaram uma linhagem celular humana especial com uma proteína repórter fluorescente projetada para se dobrar incorretamente com facilidade, mas sem ser imediatamente tóxica. Em seguida, usaram uma triagem genômica CRISPR–Cas9, desligando milhares de genes um a um e separando células de acordo com a quantidade do repórter defeituoso acumulada. Isso permitiu identificar genes que ou ajudavam a célula a destruir o repórter ou, ao contrário, faziam com que ele permanecesse por mais tempo. Como esperado, muitos alvos já eram partes conhecidas da maquinaria de descarte de proteínas na superfície do retículo endoplasmático, um sistema de membranas que funciona também como centro de controle de qualidade. Mas outro grupo, mais surpreendente, apontou para as mitocôndrias e para um fator de tradução chamado eIF5A, conhecido por influenciar o comportamento mitocondrial.
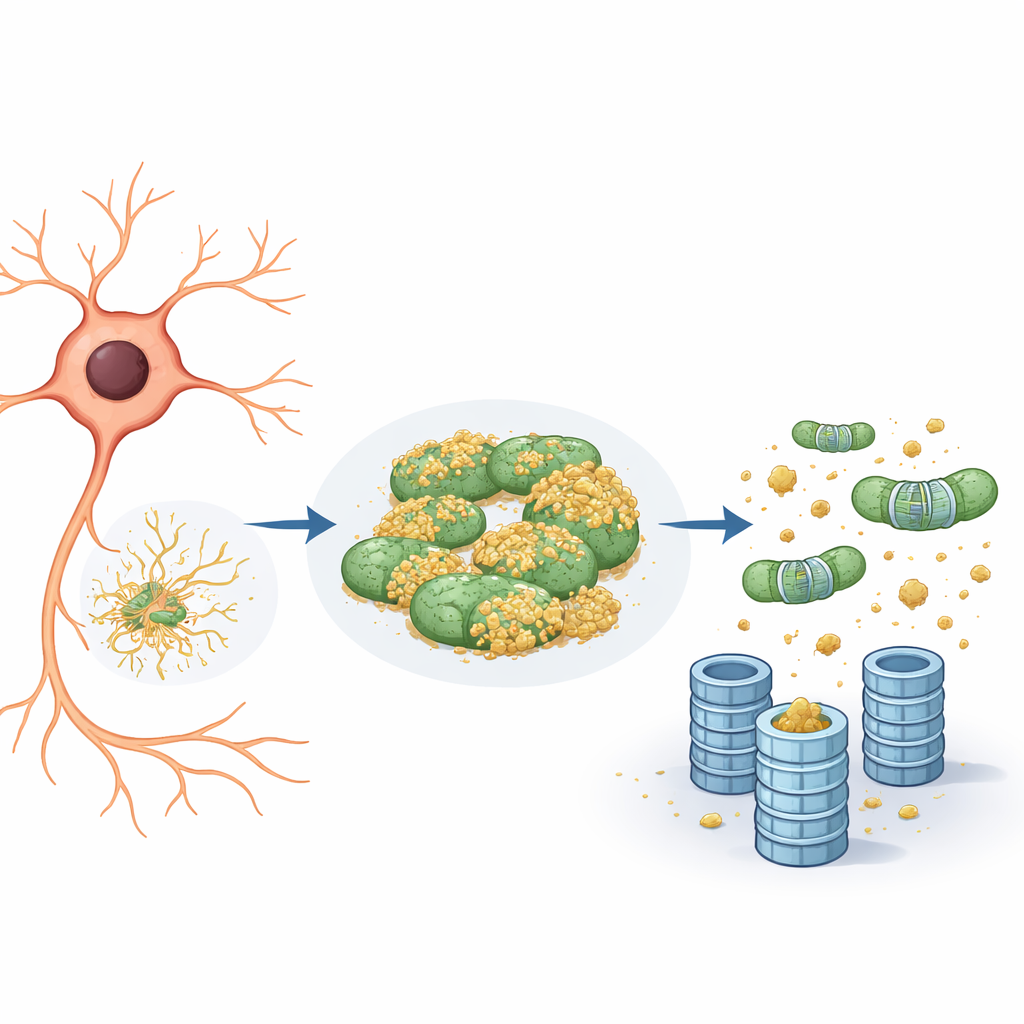
Mitocôndrias como esconderijo para proteínas problemáticas
Uma inspeção mais detalhada revelou que a proteína repórter tendia a se associar não apenas ao retículo endoplasmático, mas também às mitocôndrias. Nas mitocôndrias, ela permanecia em grande parte não marcada e, portanto, invisível ao triturador do proteassoma. Quando a equipe reduziu a atividade de eIF5A — seja diminuindo seus níveis geneticamente ou bloqueando uma modificação química única necessária para sua função — duas coisas aconteceram. Primeiro, a rede mitocondrial tornou-se mais fragmentada e reorganizada. Segundo, a proteína repórter se desprendeu das mitocôndrias e sua degradação acelerou, estritamente pela via ubiquitina–proteassoma em vez de por vias de reciclagem celular como a autofagia. Em essência, as mitocôndrias agiam como um “compartimento de refúgio”, um porto seguro onde proteínas problemáticas podiam evitar serem marcadas e destruídas.
De repórteres artificiais a proteínas ligadas a doenças
A chave desse comportamento revelou-se um motivo estrutural chamado hélice anfipática — um segmento curto, parcialmente hidrofílico e parcialmente hidrofóbico que ajuda proteínas a aderirem a membranas. Quando os pesquisadores suavizaram essa hélice em seu repórter, a proteína passou a ter menos probabilidade de se ligar às mitocôndrias ou formar agregados e deixou de apresentar maior degradação quando eIF5A era bloqueado. Importante, várias proteínas relacionadas a doenças, incluindo huntingtina mutante (na doença de Huntington) e α‑sinucleína mutante (na doença de Parkinson), também contêm hélices anfipáticas e são conhecidas por se deslocalizar para mitocôndrias. Em modelos celulares que expressam essas proteínas, reduzir a atividade de eIF5A ou perturbar a rede mitocondrial fez com que as proteínas associadas à doença se desassociasssem das mitocôndrias e fossem eliminadas mais eficientemente pelos proteassomas, com menos células exibindo grandes agregados.
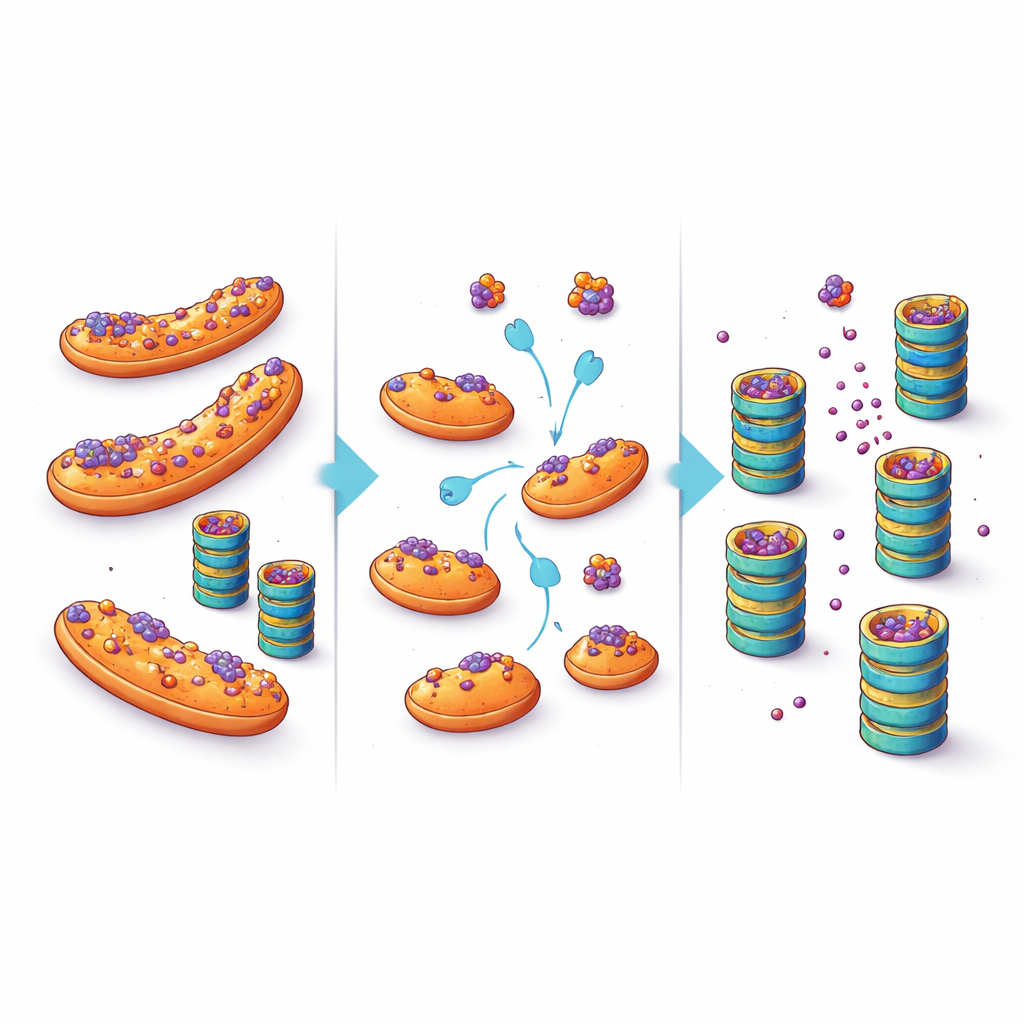
Transformando um refúgio celular em oportunidade terapêutica
Esses achados sugerem uma mudança na maneira de pensar sobre o acúmulo de proteínas em doenças neurodegenerativas. Em vez de supor que os trituradores da célula estão simplesmente sobrecarregados ou quebrados, este trabalho destaca a localização como fator crucial: quando proteínas propensas à agregação ficam ancoradas nas mitocôndrias, elas ficam menos acessíveis às enzimas de controle de qualidade e degradam-se mais lentamente. Ao deslocá‑las desse refúgio — por meio de alterações direcionadas em fatores como eIF5A ou interferindo diretamente em sua capacidade de se ligar às mitocôndrias — pode ser possível reduzir os níveis de proteínas tóxicas em neurônios vulneráveis. Embora qualquer tratamento futuro precise equilibrar tais intervenções com os muitos outros papéis das mitocôndrias e do eIF5A, o estudo abre uma via terapêutica atraente: em vez de apenas aumentar a potência do triturador celular, ajude as proteínas mal dobradas a encontrarem o caminho até ele.
Citação: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Palavras-chave: mitocôndrias, agregação de proteínas, proteassoma, neurodegeneração, eIF5A