Clear Sky Science · tr
Mitokondriler, verimli parçalanmayı engelleyen topaklanmaya meyilli proteinler için bir gizlenme bölmesi görevi görüyor
Protein kümelerinin beyin sağlığı açısından önemi
Alzheimer, Parkinson ve Huntington gibi birçok beyin hastalığında bazı proteinler doğru biçimlerini kaybeder ve sinir hücreleri içinde kümeler oluşturur. Bu yapışkan kümeler hayati süreçleri bozabilir ve sonunda hücreleri yok edebilir. Bu çalışma aldatıcı derecede basit bir soru soruyor: hücrelerin güçlü çöp imha sistemleri zaten varken, neden bu problemli proteinleri daha etkin şekilde yok edemiyorlar? Cevap hücrenin içinde beklenmedik bir yere — genellikle hücrenin enerji santralleri olarak anılan mitokondrilere — götürüyor.
Hücresel temizlik ekipleri ve sınırları
Hücrelerimiz sürekli proteinler üretiyor ve yıkıyor. Proteinler yanlış katlandığında, başlıca yok etme yollarından biri, işaretlenmiş çöpü şerit halinde öğüten bir sistem gibi çalışan ubikitin–proteazom yoludur. Problemli proteinler önce küçük moleküllerle (ubikitin) işaretlenir, sonra variller şeklindeki makineler (proteazomlar) içine beslenir ve zararsız parçalara ayrılır. Bu sistem, zarar görmüş proteinleri sert, çözünmez kümelere dönüşmeden önce yakalamada özellikle etkilidir. Yine de nörodejeneratif hastalıklarda kümeler birikir; üstelik bu yok etme sistemi çoğu zaman büyük ölçüde işlevsel kalır. Bu çelişki, sorunun yalnızca öğütücünün gücünde değil, çöpün gerçekten ona ulaşıp ulaşmadığında da olabileceğini düşündürür.
Protein yıkımını değiştiren genetik anahtarları bulmak
Topaklanmaya eğilimli proteinlerin akıbetini neyin kontrol ettiğini araştırmak için araştırmacılar, kolayca yanlış katlanan ama hemen toksik olmayan floresan bir raporlayıcı proteine sahip özel bir insan hücre hattı oluşturdu. Ardından genome çapında bir CRISPR–Cas9 taraması yaparak binlerce geni tek tek kapattılar ve hücreleri kusurlu raporlayıcıyı ne kadar biriktirdiklerine göre ayırdılar. Bu, hücrenin raporlayıcıyı yok etmesine yardımcı olan veya tersine onun daha uzun süre kalmasına neden olan genleri belirlemelerini sağladı. Beklendiği gibi, birçok vurgu zaten endoplazmik retikulum yüzeyindeki protein-yok etme makinesinin bilinen parçalarıydı; endoplazmik retikulum aynı zamanda kalite kontrol merkezi gibi davranan bir membran sistemidir. Ancak daha şaşırtıcı bir grup gen mitokondrilere ve mitokondri davranışını etkilediği bilinen bir çeviri faktörü olan eIF5A’ya işaret etti.
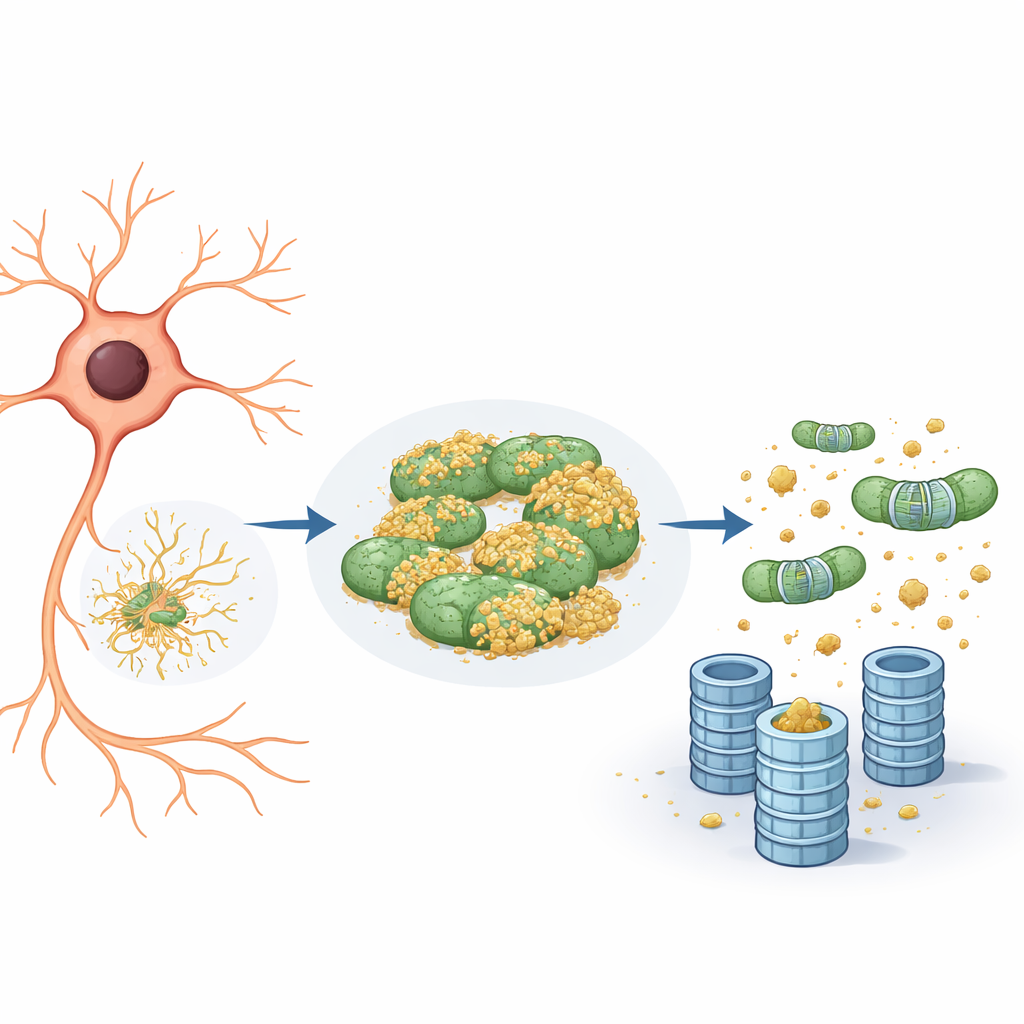
Kötü proteinler için saklanma yeri olarak mitokondriler
Daha ayrıntılı inceleme, raporlayıcı proteinin sadece endoplazmik retikulumla değil aynı zamanda mitokondrilerle de ilişki kurma eğiliminde olduğunu ortaya koydu. Mitokondrilerde, büyük ölçüde işaretlenmemiş kaldı ve dolayısıyla proteazom öğütücüsüne görünmez oldu. Araştırma ekibi eIF5A aktivitesini — ya genetik olarak düzeylerini düşürerek ya da işlevi için gerekli benzersiz bir kimyasal modifikasyonu engelleyerek — azalttığında iki şey oldu. Birincisi, mitokondri ağı daha parçalı hale geldi ve yeniden organize oldu. İkincisi, raporlayıcı protein mitokondrilerden ayrıldı ve yıkımı hızlandı; bu yıkım otofaji gibi hücresel geri dönüşüm yolları yerine kesin olarak ubikitin–proteazom sistemi aracılığıyla gerçekleşti. Özetle, mitokondriler “saklanma bölmesi” gibi davranıyor, sorunlu proteinlerin işaretlenip yok edilmekten kaçınabileceği güvenli bir liman sağlıyordu.
Yapay raporlayıcılardan hastalıkla ilişkili proteinlere
Bu davranışın anahtarı, amfipatik heliks adı verilen yapısal bir motif olduğu ortaya çıktı — kısmen suyu seven, kısmen yağı seven kısa bir segment ve proteinlerin membranlara yapışmasına yardımcı oluyor. Araştırmacılar raporlayıcılarındaki bu heliksi yumuşattıklarında, proteinin mitokondrilere bağlanma veya agregat oluşturma olasılığı azaldı ve eIF5A bloke edildiğinde artık artan yıkım göstermedi. Önemli olarak, mutant huntingtin (Huntington hastalığında) ve mutant α‑sinüklein (Parkinson hastalığında) de dahil olmak üzere birkaç hastalıkla ilişkili proteinin amfipatik heliksler içerdiği ve mitokondrilere yanlış lokalize olduğu biliniyor. Bu proteinleri ifade eden hücre modellerinde eIF5A aktivitesini düşürmek veya mitokondri ağını bozmak, hastalık proteinlerinin mitokondrilerden ayrılmasına ve proteazomlar tarafından daha etkin temizlenmesine yol açtu; daha az hücre büyük agregatlar gösterdi.
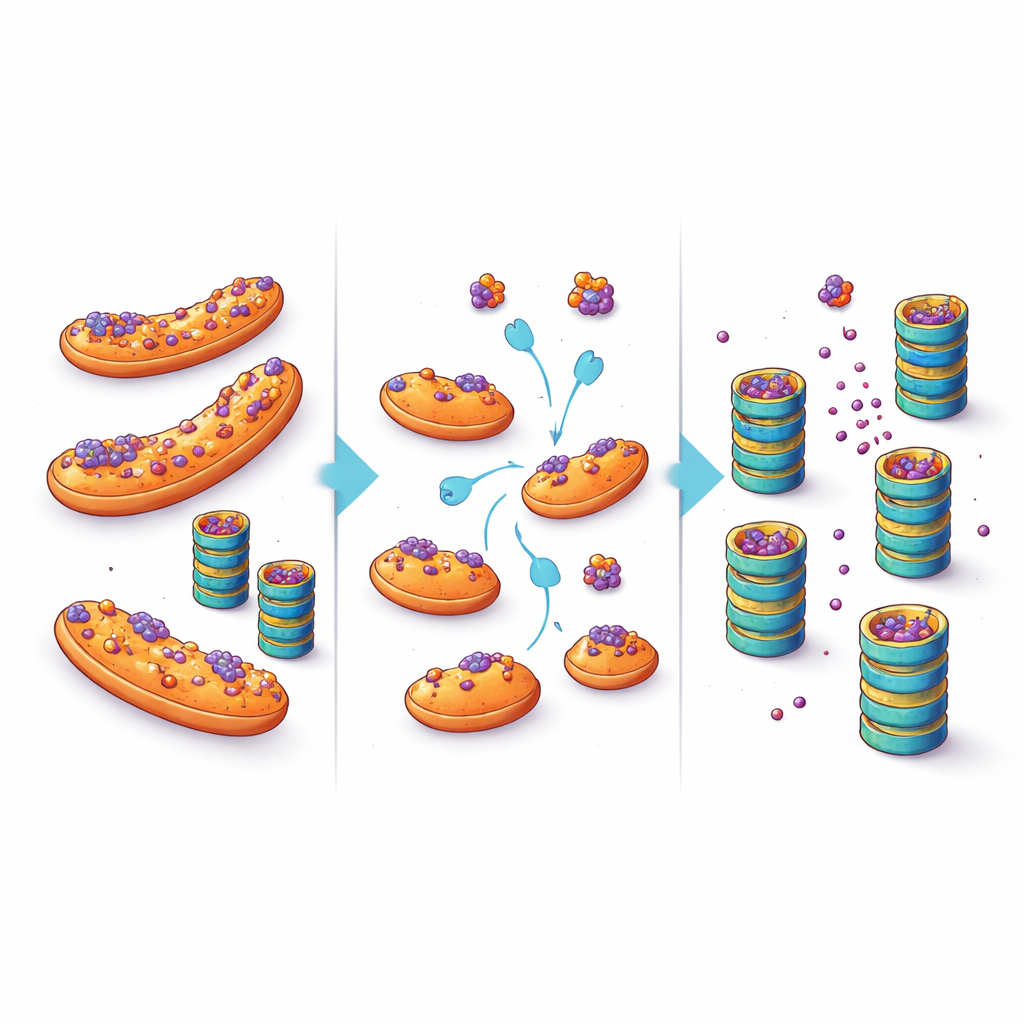
Hücresel bir sığınağı terapötik bir fırsata çevirmek
Bu bulgular, nörodejeneratif hastalıklarda protein birikimi hakkındaki düşünüşümüzü değiştirmeyi öneriyor. Hücrenin öğütücülerinin yalnızca aşırı yüklendiğini veya bozulduğunu varsaymak yerine, çalışma konumun kritik bir faktör olduğunu vurguluyor: topaklanmaya eğilimli proteinler mitokondrilerde park edildiğinde, kalite kontrol enzimleri için daha az erişilebilir oluyor ve daha yavaş parçalanıyor. Bu proteinleri eIF5A gibi faktörlerde hedeflenen değişiklikler yoluyla ya da doğrudan mitokondrilere bağlanma yeteneklerini bozarak bu sığınaktan uzaklaştırmak, hassas nöronlar içindeki toksik protein düzeylerini düşürme olasılığı sunuyor. Herhangi bir gelecekteki tedavi, mitokondrilerin ve eIF5A’nın birçok diğer rolü ile bu müdahaleler arasında bir denge kurmayı gerektirse de, çalışma cezbedici bir terapötik yol açıyor: hücresel öğütücünün gücünü sadece artırmak yerine, yanlış katlanmış proteinlerin ona ulaşmalarına yardımcı olmak.
Atıf: Gierisch, M.E., Barchi, E., Marogna, M. et al. Mitochondria serve as a holdout compartment for aggregation-prone proteins hindering efficient degradation. Nat Commun 17, 4195 (2026). https://doi.org/10.1038/s41467-026-72783-0
Anahtar kelimeler: mitokondri, protein topaklanması, proteazom, nörodejenerasyon, eIF5A