Clear Sky Science · zh
通过赖氨酸乙酰化重编程细菌毒力
细菌如何调节它们的攻击
许多有害细菌生活在我们细胞内,必须避免过快致死宿主。本研究揭示了一种此类微生物如何借助一种称为乙酰化的小型化学标签微调其攻击性的机制。通过在关键毒力蛋白上添加该标签,细菌可以改变该蛋白的构象、定位和活性,有效地根据宿主细胞的能量状态调整其进攻工具的强弱。
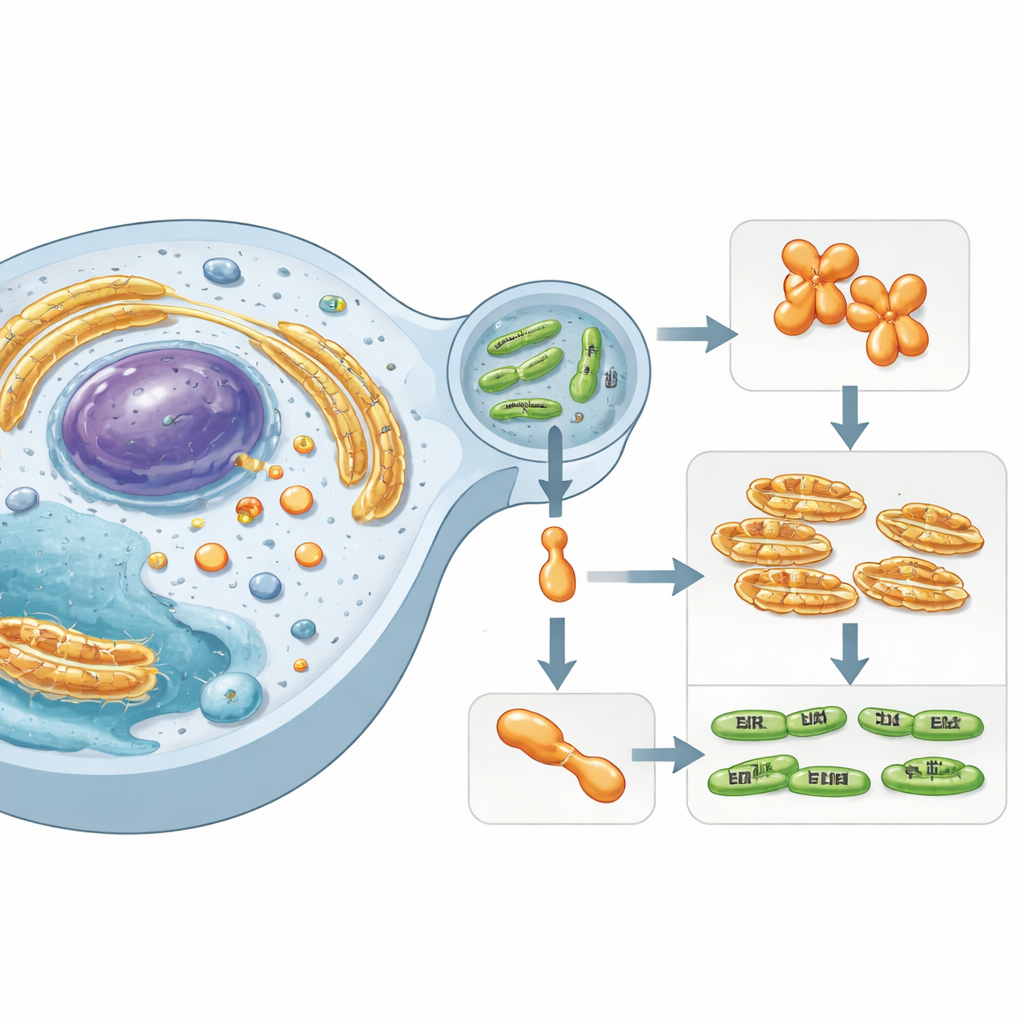
潜伏在人类细胞内的隐性参与者
这项工作聚焦于Simkania negevensis,这是一种类衣原体细菌,与长期呼吸道感染有关。这种微生物在人体细胞内的膜包泡中存活,并将专门的“效应蛋白”注入周围细胞质。其中一种效应蛋白称为 SnCE1,属于已知会干扰宿主蛋白标记系统的酶家族。这些标记——诸如泛素和 SUMO 的小蛋白——充当细胞内的交通信号,控制免疫、应激反应和细胞死亡。破坏 SUMO 和泛素链使细菌能够破坏宿主防御并营造更有利的生存环境。
具有双重功能的分子开关
研究人员表明 SnCE1 是真正的多功能分子。一方面,它是高效的“去SUMO酶”:与剪切泛素链相比,它更容易将 SUMO 链切割成单体。高分辨率晶体结构揭示了 SnCE1 如何在表面口袋中抓握 SUMO 分子,利用精确排列的带电和疏水区域使其优先识别 SUMO 而非泛素。另一方面,SnCE1 也具有自体乙酰转移酶活性:它从细胞燃料分子乙酰辅酶 A (acetyl‑CoA) 获取乙酰基并将其附着到自身若干赖氨酸残基上。令人惊讶的是,两种活性使用相同的催化中心,因此该酶在切割 SUMO 和自我修饰之间必须作出选择。
塑形、聚集与切割效应蛋白
乙酰化改变了 SnCE1 的组装方式。未修饰时,催化失活版本的蛋白倾向形成四聚体——由四个单元组成的簇。结构分析显示,亚基之间的界面阻塞了 SUMO 通常结合的位点,使这种聚集形式不利于去SUMO化。当特定赖氨酸,尤其是位于位置 231 的那一个被乙酰化时,这种基于盐桥的界面无法形成,SnCE1 以独立单体存在。这些单体具有开放的 SUMO 结合沟槽,并显示强烈的去SUMO酶活性。重要的是,在所有测试过的人类和细菌去乙酰化酶中,位于 Lys231 的乙酰化似乎都是不可逆的,一旦发生该修饰就将 SnCE1 锁定为活性单体状态。
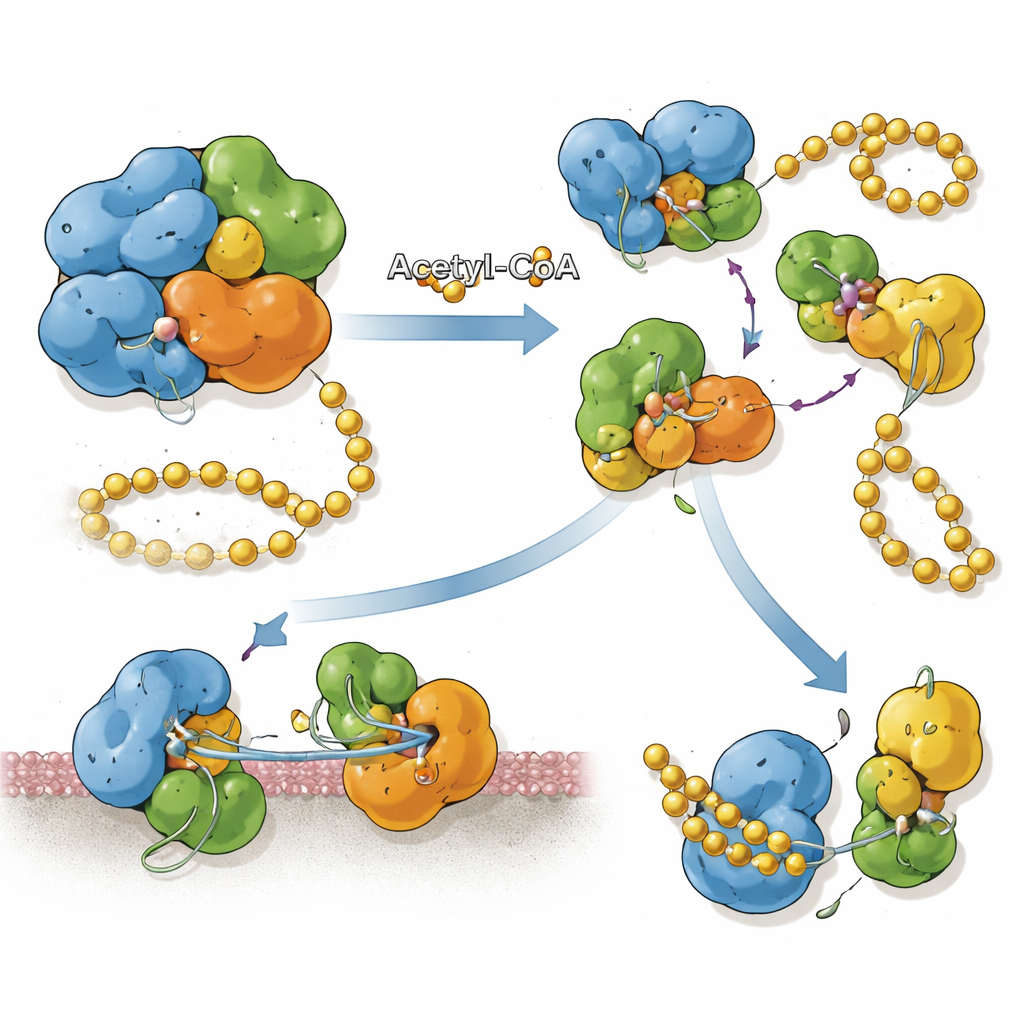
将化学标签与蛋白定位连接起来
SnCE1 在合成时带有一个表现为膜锚的 N 端片段,帮助其附着于细菌囊泡膜和邻近的内质网。研究小组发现,当 SnCE1 在该 N 端区域的若干赖氨酸上高度乙酰化时,蛋白保持完整且结合于膜。当宿主的去乙酰化酶——称为 sirtuin 的酶——去除部分这些乙酰标记时,SnCE1 会发生自切事件,从其 N 端切除约 10 千道尔顿的片段,包括膜锚。该自切加工将 SnCE1 释放到周围细胞质并导向线粒体。位点特异性乙酰化实验表明,没有单个赖氨酸能独自控制此步骤;相反,多处乙酰化位点共同作用以减缓或阻止该切割。
对线粒体与宿主代谢的影响
在人体细胞内,完整的 SnCE1 在内质网及其与线粒体的接触点富集,在这些区域可观察到线粒体形态发生显著改变。无论催化活性如何,SnCE1 的表达都会促进通常呈管状的线粒体网络发生碎裂,其中以易于被加工的非乙酰化单体突变体的效应最为明显。由于线粒体动力学与能量产生和细胞存活密切相关,这种重塑很可能影响宿主细胞对细菌生长的适宜性。作者提出,宿主细胞中乙酰‑CoA 与 NAD+ 的平衡——作为代谢状态的化学读数——调控 SnCE1 的乙酰化、去乙酰化和加工,从而在时间和空间上调整其活性与定位。
细菌毒力控制的新层面
通俗地说,这项研究表明 Simkania 使用乙酰化作为其关键武器之一的调光开关。当乙酰基充足时,SnCE1 成为稳定的活性单体,能够高效抹去 SUMO 标记,帮助细菌改写宿主信号传导,同时保持膜结合。当宿主去乙酰化酶发挥作用时,SnCE1 被剪切并释放,重新分布到线粒体附近,进一步重塑细胞内部结构。通过将毒力与反映细胞代谢的小型化学标签相连,细菌能够调整其操控宿主的激进程度,这一复杂策略可能为其他细胞内病原体共有。
引用: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
关键词: 细菌毒力调控, 蛋白质乙酰化, SUMO 去共轭, 宿主—病原体相互作用, 线粒体动力学