Clear Sky Science · es
Reprogramación de la virulencia bacteriana mediante acetilación de lisina
Cómo las bacterias ajustan su ataque
Muchas bacterias dañinas viven dentro de nuestras células y deben evitar matar al huésped demasiado rápido. Este estudio desvela cómo uno de esos microbios afina su agresividad usando una pequeña marca química llamada acetilación. Al decorar una proteína de virulencia clave con esta etiqueta, la bacteria puede cambiar la forma, la localización y la actividad de la proteína, regulando efectivamente sus herramientas ofensivas según el estado energético de la célula huésped.
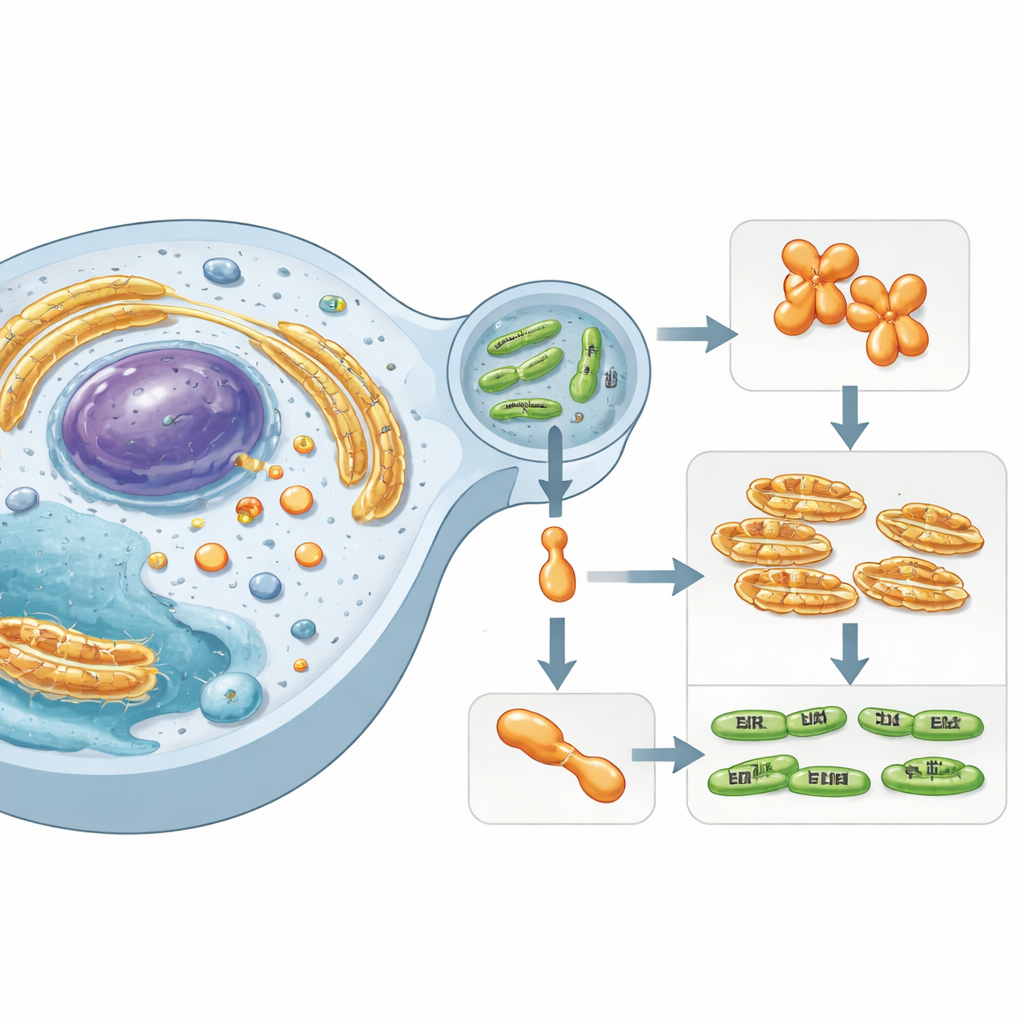
Un actor oculto dentro de las células humanas
El trabajo se centra en Simkania negevensis, una bacteria parecida a Chlamydia asociada a infecciones respiratorias persistentes. Este microbio sobrevive dentro de una burbuja delimitada por membrana en las células humanas e inyecta proteínas especializadas “efectoras” en el citoplasma circundante. Una de estas efectoras, llamada SnCE1, pertenece a una familia de enzimas conocidas por interferir con los sistemas de etiquetado proteico del huésped. Estas etiquetas —pequeñas proteínas como ubiquitina y SUMO— actúan como señales de tráfico celular, controlando la inmunidad, las respuestas al estrés y la muerte celular. Perturbar las cadenas de SUMO y ubiquitina permite a las bacterias sabotear las defensas del huésped y crear un nicho más hospitalario.
Un interruptor molecular de doble función
Los investigadores muestran que SnCE1 es una verdadera multitarea. Por un lado, es una eficiente “desSUMOilasa”: corta cadenas de SUMO en unidades simples mucho más fácilmente que las de ubiquitina. Estructuras cristalográficas de alta resolución revelan cómo SnCE1 sujeta una molécula de SUMO en un bolsillo superficial, usando regiones cargadas y hidrofóbicas colocadas con precisión para favorecer SUMO sobre ubiquitina. Por otro lado, SnCE1 también actúa como una auto‑acetiltransferasa: toma grupos acetilo de la molécula energética celular acetil‑CoA y los une a varias de sus propias lisinas. Sorprendentemente, ambas actividades utilizan el mismo centro catalítico, por lo que la enzima debe elegir entre cortar SUMO o modificarse a sí misma.
Modelar, agrupar y cortar la efectora
La acetilación resulta remodelar cómo se ensambla SnCE1. Cuando no está modificada, una versión catalíticamente inactiva de la proteína tiende a formar tetrámeros: agregados de cuatro unidades. El análisis estructural muestra que las interfaces entre subunidades bloquean el sitio donde normalmente se uniría SUMO, haciendo que esta forma agrupada sea poco adecuada para la desSUMOilación. Cuando lisinas específicas, especialmente la de la posición 231, están acetiladas, esta interfaz basada en puentes salinos ya no puede formarse y SnCE1 existe como monómeros separados. Estas unidades individuales tienen una ranura abierta de unión a SUMO y muestran fuerte actividad desSUMOilasa. Es importante que la acetilación en la Lys231 parece irreversible frente a todas las desacetilasas humanas y bacterianas probadas, fijando a SnCE1 en su estado activo y monomérico una vez que se produce esta modificación.
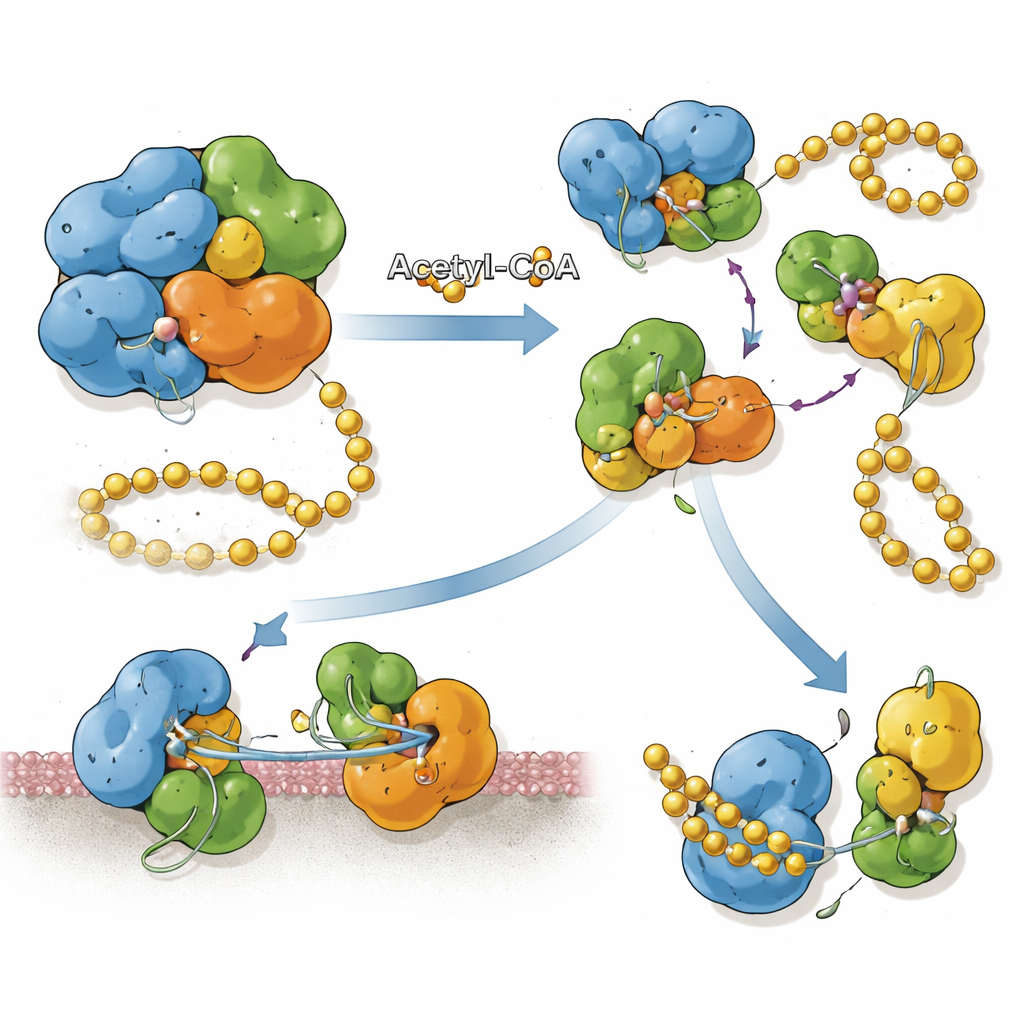
Vinculando etiquetas químicas con la posición de la proteína
SnCE1 se sintetiza con un segmento N‑terminal que funciona como ancla de membrana, ayudando a fijarla a la membrana de la vacuola bacteriana y al retículo endoplásmico cercano. El equipo encontró que cuando SnCE1 está fuertemente acetilada en varias lisinas de esta región N‑terminal, la proteína permanece íntegra y unida a la membrana. Cuando las enzimas del huésped llamadas sirtuinas eliminan algunas de estas marcas acetilo, SnCE1 sufre un evento de autocorte que recorta aproximadamente 10 kilodaltons de su extremo N, incluida el ancla de membrana. Este procesamiento autoproteolítico libera a SnCE1 hacia el citosol circundante y en dirección a las mitocondrias. Experimentos de acetilación sitio‑específica muestran que ninguna lisina única controla este paso; en su lugar, múltiples sitios acetilados actúan de forma colectiva para ralentizar o prevenir el corte.
Impacto en las mitocondrias y el metabolismo del huésped
Dentro de las células humanas, SnCE1 de longitud completa se concentra en el retículo endoplásmico y en puntos de contacto con las mitocondrias, donde coincide con cambios marcados en la morfología mitocondrial. Tanto si es catalíticamente activa como no, la expresión de SnCE1 promueve la fragmentación de la red mitocondrial, normalmente tubular, con el efecto más pronunciado observado en un mutante monomérico no acetilado que se procesa con facilidad. Dado que la dinámica mitocondrial está estrechamente ligada a la producción de energía y la supervivencia celular, este remodelado probablemente influye en lo acogedora que resulta la célula para el crecimiento bacteriano. Los autores proponen que el equilibrio de acetil‑CoA y NAD+ en la célula huésped —indicadores químicos del estado metabólico— gobierna la acetilación, desacetilación y el procesamiento de SnCE1, ajustando así su actividad y localización en espacio y tiempo.
Una nueva capa de control en la virulencia bacteriana
En términos cotidianos, este estudio muestra que Simkania usa la acetilación como un regulador de intensidad para una de sus armas clave. Cuando los grupos acetilo son abundantes, SnCE1 se convierte en un monómero estable y activo que borra eficientemente las etiquetas SUMO, ayudando a la bacteria a reconfigurar la señalización del huésped mientras permanece adherida a membranas. Cuando las desacetilasas del huésped actúan, SnCE1 se recorta y se libera, redistribuyéndose hacia las mitocondrias y remodelando aún más el paisaje interno de la célula. Al ligar la virulencia a pequeñas etiquetas químicas que reflejan el metabolismo celular, la bacteria puede modular cuán agresivamente manipula a su huésped, revelando una estrategia sofisticada que podría compartir con otros patógenos intracelulares.
Cita: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Palabras clave: regulación de la virulencia bacteriana, acetilación de proteínas, desconjugación de SUMO, interacciones huésped‑patógeno, dinámica mitocondrial