Clear Sky Science · fr
Reprogrammation de la virulence bactérienne par l’acétylation des lysines
Comment les bactéries ajustent leur attaque
Beaucoup de bactéries pathogènes vivent à l’intérieur de nos cellules et doivent éviter de tuer leur hôte trop rapidement. Cette étude révèle comment un microbe de ce type module son agressivité à l’aide d’une petite marque chimique appelée acétylation. En décorant une protéine clé de virulence avec cette marque, la bactérie peut modifier la conformation, la localisation et l’activité de la protéine, ajustant ainsi ses outils offensifs à l’état énergétique de la cellule hôte.
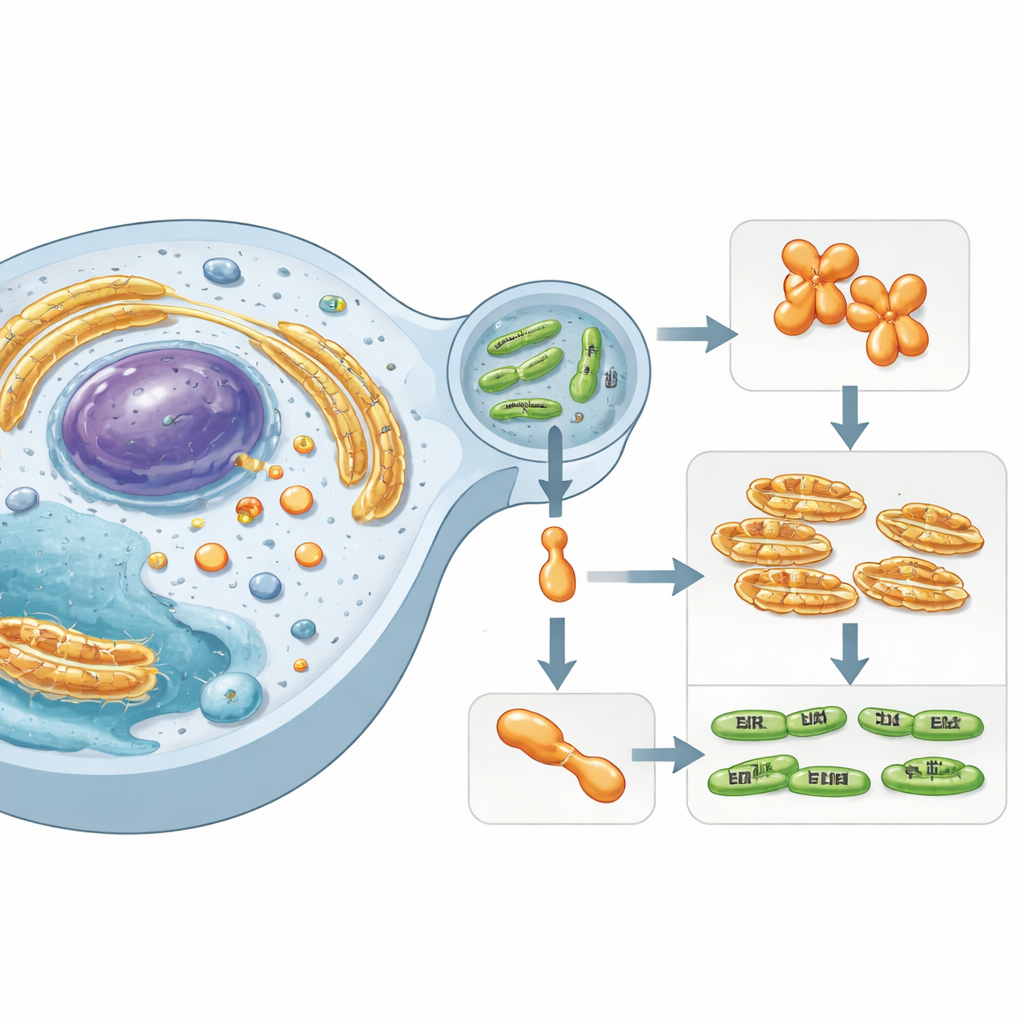
Un acteur caché à l’intérieur des cellules humaines
Le travail porte sur Simkania negevensis, une bactérie de type Chlamydia associée à des infections respiratoires prolongées. Ce microbe survit à l’intérieur d’une vésicule entourée d’une membrane dans les cellules humaines et injecte des protéines effectrices spécialisées dans le cytoplasme voisin. L’un de ces effecteurs, nommé SnCE1, appartient à une famille d’enzymes connues pour interférer avec les systèmes d’étiquetage des protéines de l’hôte. Ces étiquettes — de petits protéines telles que l’ubiquitine et le SUMO — agissent comme des signaux de circulation cellulaire, contrôlant l’immunité, les réponses au stress et la mort cellulaire. Perturber les chaînes de SUMO et d’ubiquitine permet aux bactéries de saboter les défenses de l’hôte et de créer un niche plus hospitalière.
Un commutateur moléculaire à double fonction
Les chercheurs montrent que SnCE1 est un véritable multitâche. D’une part, c’est une « déSUMOylase » efficace : elle coupe les chaînes de SUMO en unités simples beaucoup plus facilement qu’elle ne clive les chaînes d’ubiquitine. Des structures cristallographiques à haute résolution révèlent comment SnCE1 saisit une molécule de SUMO dans une poche de surface, utilisant des régions chargées et hydrophobes précisément positionnées pour favoriser le SUMO par rapport à l’ubiquitine. D’autre part, SnCE1 se comporte aussi comme une auto‑acétyltransférase : elle prélève des groupes acétyle de la molécule d’énergie cellulaire acétyl‑CoA et les attache à plusieurs de ses propres résidus lysine. De manière surprenante, les deux activités utilisent le même centre catalytique, si bien que l’enzyme doit choisir entre couper le SUMO et se modifier elle‑même.
Mise en forme, regroupement et clivage de l’effecteur
L’acétylation remodèle la façon dont SnCE1 s’assemble. Lorsqu’elle n’est pas modifiée, une version catalytiquement inactive de la protéine a tendance à former des tétramères — des agrégats de quatre unités. L’analyse structurale montre que les interfaces entre sous‑unités bloquent le site où le SUMO se lierait normalement, rendant cette forme en grappes peu adaptée à la déSUMOylation. Quand des lysines spécifiques, en particulier celle en position 231, sont acétylées, cette interface basée sur des ponts salins ne peut plus se former, et SnCE1 existe sous forme de monomères séparés. Ces unités isolées présentent un sillon de liaison au SUMO ouvert et affichent une forte activité déSUMOylase. Fait important, l’acétylation de la Lys231 semble irréversible avec tous les désacétylases humaines et bactériens testés, verrouillant SnCE1 dans son état actif et monomérique une fois cette modification survenue.
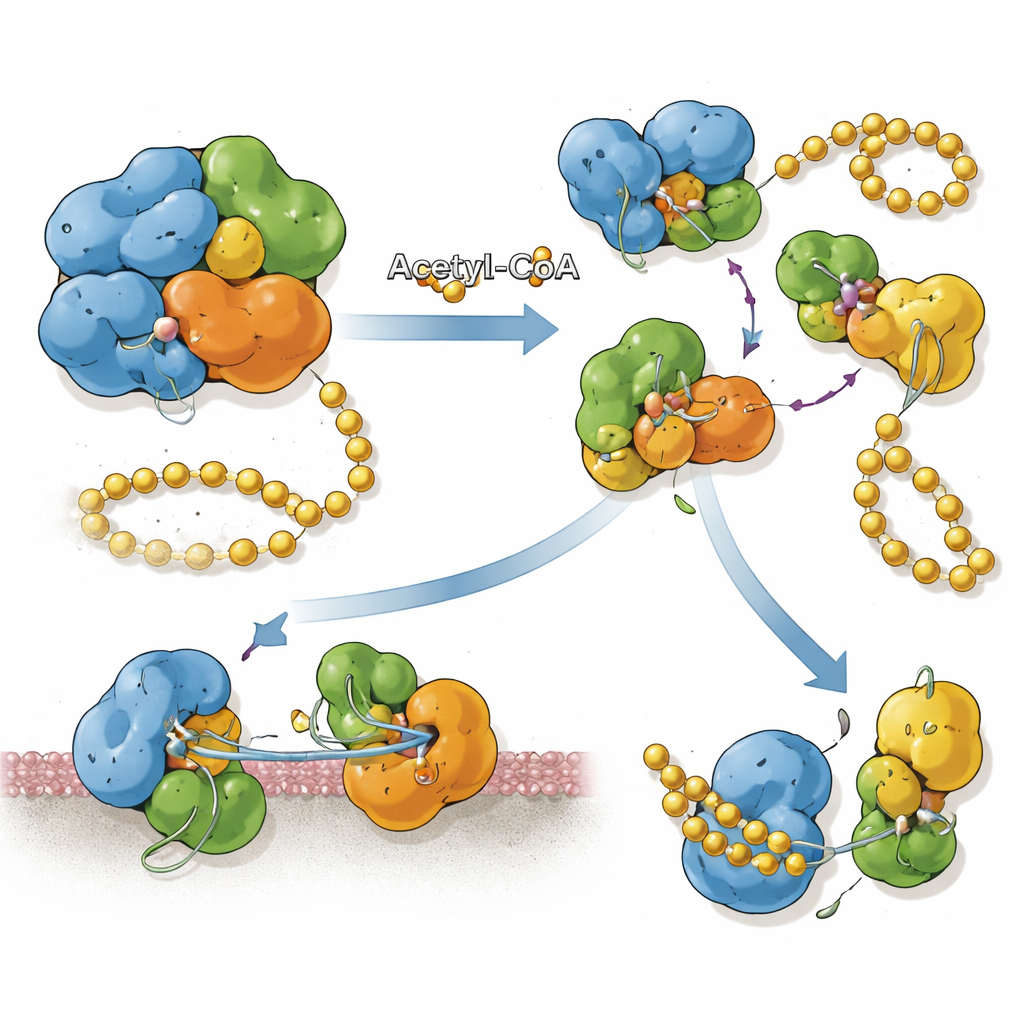
Relier les marques chimiques à la position de la protéine
SnCE1 est produite avec un segment N‑terminal qui se comporte comme une ancre membranaire, l’aidant à se fixer à la membrane de la vacuole bactérienne et au réticulum endoplasmique voisin. L’équipe a constaté que lorsque SnCE1 est fortement acétylée sur plusieurs lysines de cette région N‑terminale, la protéine reste pleine longueur et associée à la membrane. Lorsque des enzymes hôtes appelées sirtuines retirent certaines de ces marques acétyle, SnCE1 subit un événement d’auto‑clivage qui enlève environ 10 kilodaltons de son extrémité N‑terminale, y compris l’ancre membranaire. Ce traitement autoprotéolytique libère SnCE1 dans le cytosol environnant et vers les mitochondries. Des expériences d’acétylation site‑spécifique montrent qu’aucune lysine unique ne contrôle cette étape ; au contraire, plusieurs sites acétylés ralentissent ou empêchent collectivement le clivage.
Impact sur les mitochondries et le métabolisme de l’hôte
À l’intérieur des cellules humaines, la SnCE1 pleine longueur se concentre au niveau du réticulum endoplasmique et aux points de contact avec les mitochondries, où elle coïncide avec des changements saisissants de la morphologie mitochondriale. Qu’elle soit catalytiquement active ou non, l’expression de SnCE1 favorise la fragmentation du réseau mitochondrial normalement tubulaire, l’effet le plus marqué étant observé pour un mutant monomérique non acétylé qui est facilement traité. Comme la dynamique mitochondriale est étroitement liée à la production d’énergie et à la survie cellulaire, ce remodelage influence probablement l’hospitalité de la cellule pour la croissance bactérienne. Les auteurs proposent que l’équilibre entre l’acétyl‑CoA et le NAD+ dans la cellule hôte — indicateurs chimiques de l’état métabolique — régisse l’acétylation, la désacétylation et le traitement de SnCE1, ajustant ainsi son activité et sa localisation dans l’espace et le temps.
Une nouvelle couche de contrôle de la virulence bactérienne
En termes simples, cette étude montre que Simkania utilise l’acétylation comme un variateur sur l’un de ses principaux armes. Lorsque les groupes acétyle sont abondants, SnCE1 devient un monomère stable et actif qui efface efficacement les marques SUMO, aidant la bactérie à reprogrammer la signalisation de l’hôte tout en restant attachée aux membranes. Quand les désacétylases de l’hôte sont activées, SnCE1 est tronquée et libérée, se redistribuant vers les mitochondries et remodelant davantage le paysage interne de la cellule. En liant la virulence à de petites marques chimiques qui reflètent le métabolisme cellulaire, la bactérie peut ajuster l’intensité avec laquelle elle manipule son hôte, révélant une stratégie sophistiquée qui pourrait être partagée par d’autres pathogènes intracellulaires.
Citation: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Mots-clés: régulation de la virulence bactérienne, acétylation des protéines, déconjugation SUMO, interactions hôte–pathogène, dynamique mitochondriale