Clear Sky Science · nl
Hersturing van bacteriële virulentie door lysine-acetylatie
Hoe bacteriën hun aanval afstemmen
Veel schadelijke bacteriën leven binnen onze cellen en moeten voorkomen dat ze hun gastheer te snel doden. Deze studie onthult hoe één zo’n microbe zijn agressie fijn afstemt met behulp van een klein chemisch label dat acetylatie wordt genoemd. Door een sleutelproteïne voor virulentie met dit label te markeren, kan de bacterie de vorm, locatie en activiteit van dat eiwit wisselen en zo haar offensieve instrumenten op- of terugschakelen afhankelijk van de energietoestand van de gastheercel.
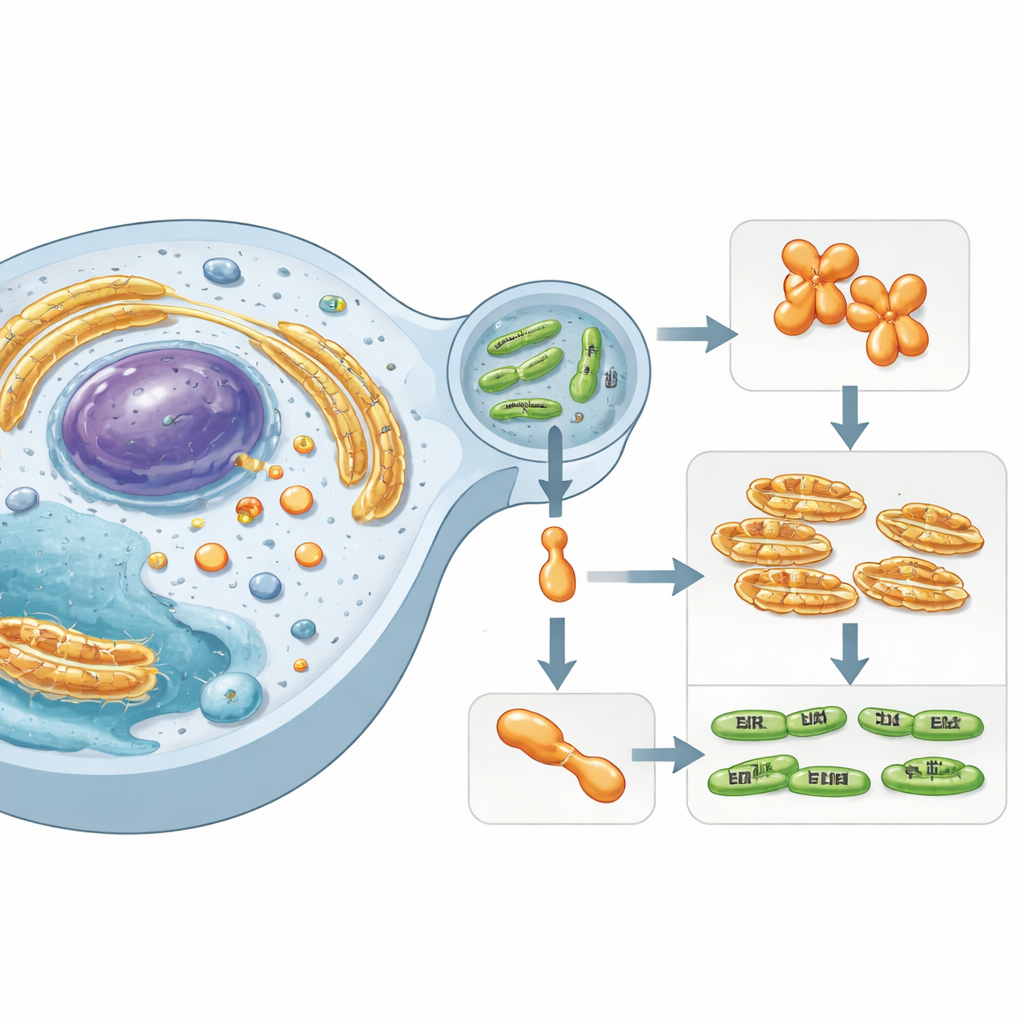
Een verborgen speler binnen menselijke cellen
Het werk richt zich op Simkania negevensis, een Chlamydia-achtig bacterie die in verband wordt gebracht met langdurige luchtweginfecties. Deze microbe overleeft binnen een membraan-omhulde blaar in menselijke cellen en injecteert gespecialiseerde “effector”-eiwitten in het omringende cytoplasma. Een van deze effectors, SnCE1 genoemd, behoort tot een familie enzymen die bekendstaan om hun vermogen de eiwit-labelsystemen van de gastheer te verstoren. Die labels — kleine eiwitten zoals ubiquitine en SUMO — functioneren als cellulaire verkeerslichten en regelen immuunreacties, stressantwoorden en celdood. Het ontregelen van SUMO- en ubiquitineketens stelt bacteriën in staat gastheerverdedigingen te saboteren en een meer gastvrije niche te creëren.
Een moleculaire schakel met dubbele functie
De onderzoekers tonen aan dat SnCE1 een echte alleskunner is. Enerzijds is het een efficiënte “deSUMOylase”: het knipt SUMO-ketens veel sneller in losse eenheden dan het ubiquitineketens doorneemt. Kristalstructuren met hoge resolutie laten zien hoe SnCE1 een SUMO-molecuul in een oppervlaktepocket vastgrijpt, waarbij nauwkeurig geplaatste geladen en hydrofobe gebieden SUMO boven ubiquitine bevoordelen. Anderzijds gedraagt SnCE1 zich ook als een auto-acetyltransferase: het neemt acetylgroepen van het cellulaire brandstofmolecuul acetyl-CoA en hecht die aan meerdere van zijn eigen lysineresiduen. Verrassend genoeg gebruiken beide activiteiten hetzelfde katalytische centrum, waardoor het enzym moet kiezen tussen het knippen van SUMO en het modificeren van zichzelf.
Vorming, clusteren en knippen van de effector
Acetylatie blijkt de wijze waarop SnCE1 is geassembleerd te herschikken. Wanneer het niet-gemodificeerd is, neigt een katalytisch inactieve versie van het eiwit tot het vormen van tetrameren — clustervormingen van vier subeenheden. Structurele analyse toont dat de interfaces tussen subeenheden de plaats blokkeren waar SUMO normaal zou binden, waardoor deze gecorreleerde vorm slecht geschikt is voor deSUMOylatie. Wanneer specifieke lysines, met name die op positie 231, worden geacetyleerd, kan deze op zoutbruggen gebaseerde interface niet langer vormen en bestaat SnCE1 als losse monomeren. Deze enkelvoudige eenheden hebben een open SUMO-bindingsgroeve en vertonen sterke deSUMOylase-activiteit. Belangrijk is dat acetylatie op Lys231 onder alle geteste humane en bacteriële deacetylases onomkeerbaar lijkt te zijn, waardoor SnCE1, eenmaal gemodificeerd, in zijn actieve, monomere staat vergrendeld raakt.
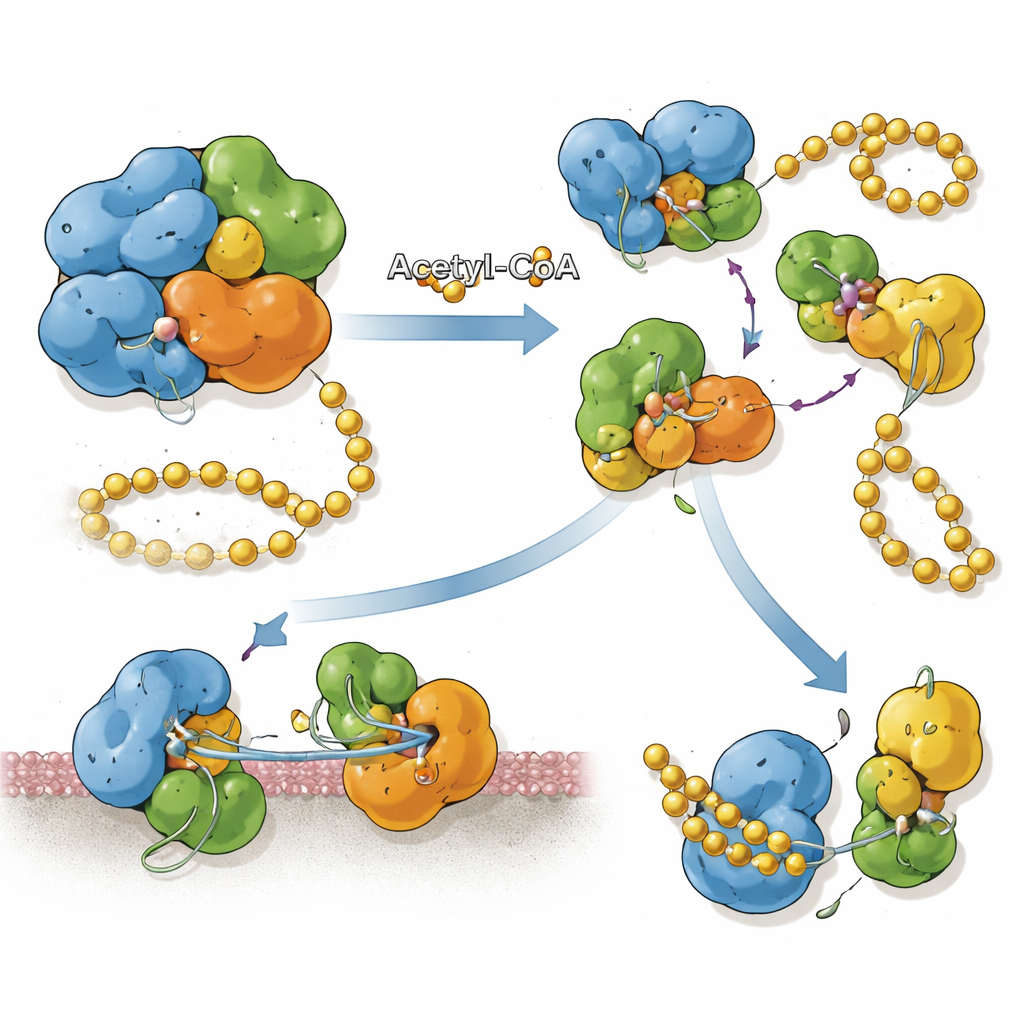
Het koppelen van chemische labels aan eiwitpositie
SnCE1 wordt geproduceerd met een N-terminaal segment dat zich gedraagt als een membraanaanhechting en helpt het te binden aan het membraan van de bacteriële vacuole en het nabijgelegen endoplasmatisch reticulum. Het team vond dat wanneer SnCE1 sterk geacetyleerd is op meerdere lysines in dit N-terminale gebied, het eiwit volledig intact blijft en membraangebonden is. Wanneer gastheer-enzymen genaamd sirtuïnes sommige van deze acetylmerken verwijderen, ondergaat SnCE1 een zelfknipgebeurtenis die ongeveer 10 kilodalton van zijn N-terminus afknipt, inclusief de membraanaanhechting. Deze autoproteolytische verwerking laat SnCE1 vrij in het omringende cytosol en richting mitochondriën. Plaats-specifieke acetylatie-experimenten tonen aan dat geen enkele lysine deze stap alleen controleert; in plaats daarvan vertragen of verhinderen meerdere geacetyleerde plaatsen gezamenlijk de knip.
Effecten op mitochondriën en gastheermetabolisme
Binnen menselijke cellen concentreert volledig intacte SnCE1 zich bij het endoplasmatisch reticulum en op contactpunten met mitochondriën, waar het samenvalt met opvallende veranderingen in de mitochondriale vorm. Of het nu katalytisch actief is of niet, expressie van SnCE1 bevordert fragmentatie van het normaal buisvormige mitochondriale netwerk, met het sterkste effect waargenomen bij een niet-geacetyleerde, monomere mutant die gemakkelijk wordt verwerkt. Omdat mitochondriale dynamiek nauw gekoppeld is aan energieproductie en celoverleving, beïnvloedt deze herstructurering waarschijnlijk hoe gastvrij de cel is voor bacteriële groei. De auteurs stellen dat de balans van acetyl-CoA en NAD+ in de gastheercel — chemische indicatoren van de metabole toestand — de acetylatie, deacetylatie en verwerking van SnCE1 regelt, waardoor de activiteit en lokalisatie ervan in ruimte en tijd worden afgestemd.
Een nieuwe controlelaag in bacteriële virulentie
In alledaagse termen laat deze studie zien dat Simkania acetylatie gebruikt als een dimmer op een van zijn belangrijkste wapens. Wanneer acetylgroepen overvloedig zijn, wordt SnCE1 een stabiel, actief monomeer dat efficiënt SUMO-labels wist en de bacterie helpt gastheersignalering te herbedraden terwijl het aan membranen blijft hangen. Wanneer gastheer-deacetylases geactiveerd worden, wordt SnCE1 afgesplitst en vrijgegeven, herverdeelt het zich richting mitochondriën en vormt het verder het interne landschap van de cel om. Door virulentie te koppelen aan kleine chemische labels die de cellulaire stofwisseling volgen, kan de bacterie afstemmen hoe agressief ze haar gastheer manipuleert, wat wijst op een verfijnde strategie die mogelijk gedeeld wordt door andere intracellulaire pathogenen.
Bronvermelding: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Trefwoorden: regulatie van bacteriële virulentie, eiwitacetylatie, SUMO-deconjugatie, gastheer–pathogeen interacties, mitochondriale dynamiek