Clear Sky Science · ru
Перепрограммирование вирулентности бактерий посредством ацетилирования лизина
Как бактерии регулируют свою атаку
Многие патогенные бактерии живут внутри наших клеток и должны избегать слишком быстрого уничтожения хозяина. В этом исследовании выясняется, как один такой микроорганизм тонко настраивает свою агрессию с помощью крошечного химического ярлыка — ацетилирования. Помечая этим ярлыком ключевой белок вирулентности, бактерия может менять его конформацию, локализацию и активность, фактически регулируя свои наступательные механизмы в зависимости от энергетического состояния клетки хозяина.
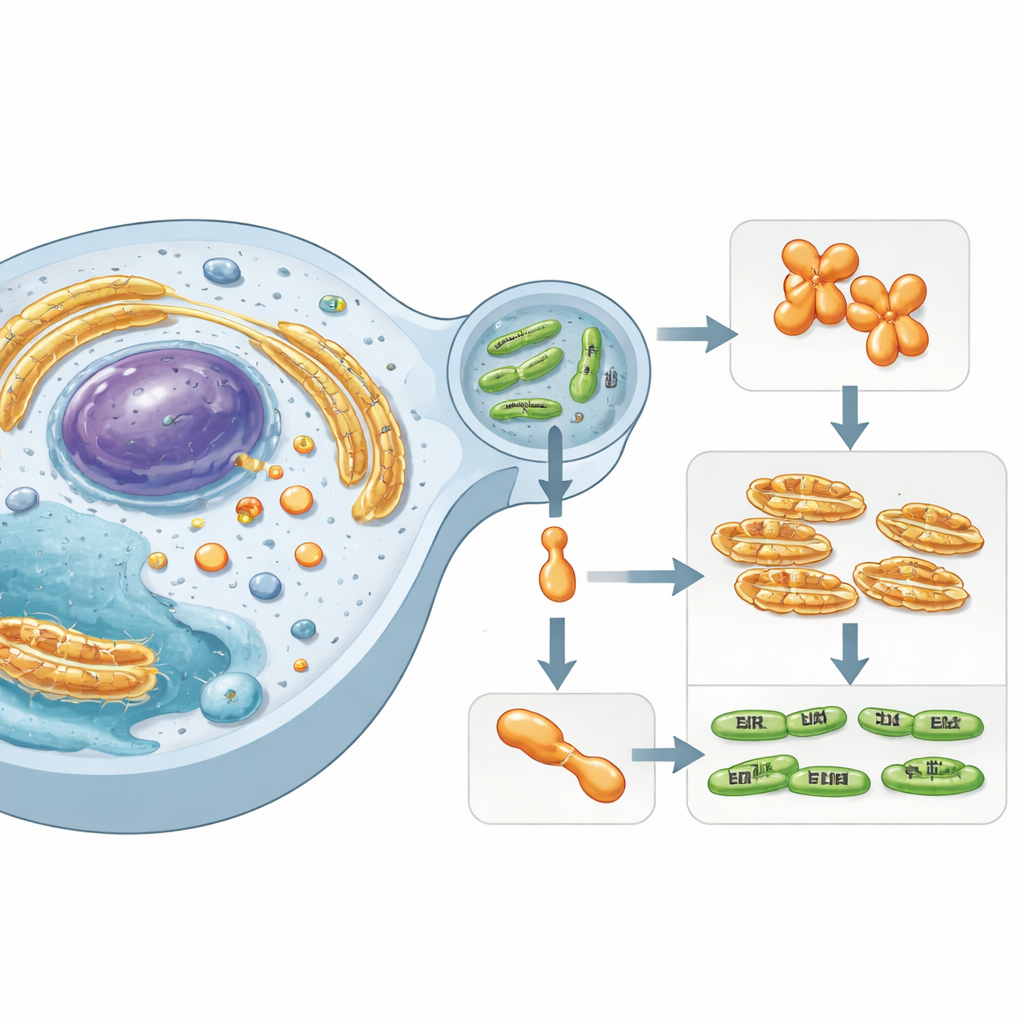
Скрытый игрок внутри человеческих клеток
Работа сосредоточена на Simkania negevensis, схожей с хламидиями бактерии, связанной с длительными респираторными инфекциями. Этот микроорганизм выживает внутри мембраносвязанного пузырька в человеческих клетках и вводит специализированные «эффекторные» белки в окружающий цитоплазматический объем. Один из таких эффекторов, названный SnCE1, относится к семейству ферментов, известных своим вмешательством в системы пометки белков хозяина. Эти пометки — маленькие белки, такие как убиквитин и SUMO — действуют как клеточные сигналы движения, контролируя иммунитет, стресс‑ответы и гибель клетки. Нарушение цепочек SUMO и убиквитина позволяет бактериям саботировать защиту хозяина и создавать более благоприятную нишу.
Молекулярный переключатель с двойной функцией
Исследователи показывают, что SnCE1 — настоящий универсал. С одной стороны, он является эффективным «деSUMOилазой»: он расщепляет цепочки SUMO до одиночных единиц гораздо охотнее, чем расщепляет цепочки убиквитина. Структуры высокого разрешения показывают, как SnCE1 захватывает молекулу SUMO в поверхностной ямке, используя точно расположенные заряженные и гидрофобные участки, чтобы предпочитать SUMO убиквитину. С другой стороны, SnCE1 также действует как авто‑ацетилтрансфераза: он берет ацетильные группы от клеточного энергетического молекулы ацетил‑КоА и присоединяет их к нескольким собственным остаткам лизина. Удивительно, что обе активности используют один и тот же каталитический центр, поэтому фермент вынужден выбирать между резкой SUMO и собственной модификацией.
Формирование, кластеризация и расщепление эффектора
Ацетилирование, как оказалось, перестраивает пространственную сборку SnCE1. В немодифицированном виде каталитически неактивная версия белка склонна образовывать тетрамеры — кластеры из четырех субъединиц. Структурный анализ показывает, что интерфейсы между субъединицами блокируют сайт, где обычно связывается SUMO, делая эту кластерную форму плохо пригодной для деSUMОylации. Когда определенные лизины, особенно на позиции 231, ацетилируются, этот интерфейс, основанный на солевом мостике, больше не может формироваться, и SnCE1 существует как отдельные мономеры. Эти одиночные субъединицы имеют открытую борозду для связывания SUMO и проявляют сильную деSUMOилазную активность. Важно, что ацетилирование Lys231 кажется необратимым при использовании всех протестированных человеческих и бактериальных деацетилаз, фиксируя SnCE1 в его активном мономерном состоянии после появления этой модификации.
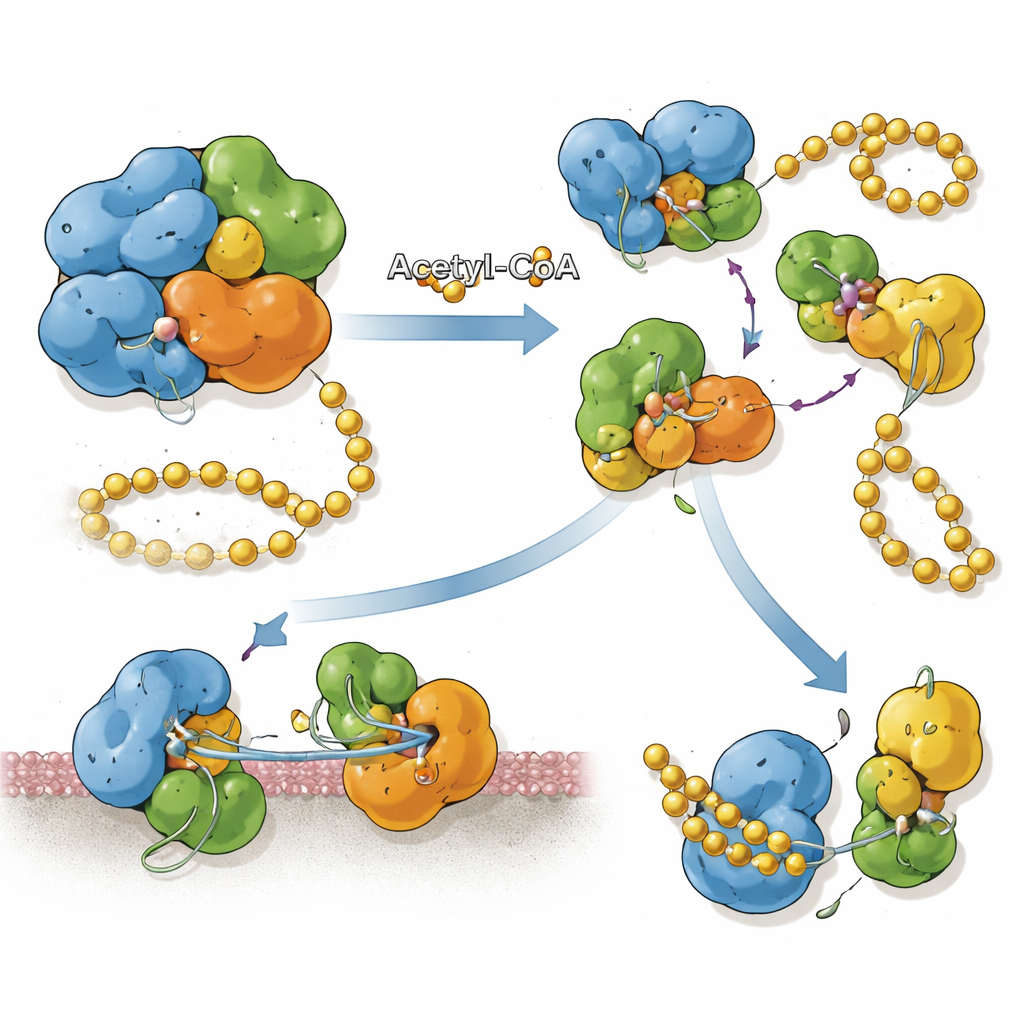
Связь химических меток с локализацией белка
SnCE1 синтезируется с N‑концевым сегментом, который ведет себя как мембранный якорь, помогая ему прикрепляться к мембране бактериальной вакуоли и соседнего эндоплазматического ретикулума. Группа обнаружила, что при интенсивном ацетилировании нескольких лизинов в этой N‑концевой области белок остаётся полноразмерным и связанным с мембраной. Когда ферменты хозяина, называемые сиртуинами, снимают часть этих ацетильных меток, SnCE1 подвергается саморасщеплению, при котором примерно 10 килодальтон отрезается от N‑конца, включая мембранный якорь. Это аутопротеолитическое расщепление высвобождает SnCE1 в окружающую цитозоль и направляет его к митохондриям. Эксперименты с сайто‑специфическим ацетилированием показывают, что ни один отдельный лизин не контролирует этот шаг; вместо этого несколько ацетилированных сайтов совместно замедляют или предотвращают расщепление.
Влияние на митохондрии и метаболизм хозяина
Внутри человеческих клеток полноразмерный SnCE1 концентрируется в эндоплазматическом ретикулуме и в точках контакта с митохондриями, где его появление совпадает с заметными изменениями формы митохондрий. Независимо от каталитической активности, экспрессия SnCE1 способствует фрагментации обычно трубчатой митохондриальной сети, причем наибольший эффект наблюдается для неацетилированного мономерного мутанта, который легко обрабатывается. Поскольку митохондриальная динамика тесно связана с выработкой энергии и выживанием клетки, такая перестройка, вероятно, влияет на пригодность клетки для роста бактерии. Авторы предлагают, что соотношение ацетил‑КоА и NAD+ в клетке хозяина — химические индикаторы метаболического состояния — управляет ацетилированием, деацетилированием и обработкой SnCE1, тем самым регулируя его активность и локализацию в пространстве и времени.
Новый уровень контроля вирулентности бактерий
Говоря простыми словами, это исследование показывает, что Simkania использует ацетилирование как регулятор‑диммер для одного из своих ключевых орудий. Когда ацетильные группы изобилуют, SnCE1 становится стабильным, активным мономером, который эффективно стирает SUMO‑метки, помогая бактерии перенастроить сигнальные пути хозяина, оставаясь при этом прикреплённым к мембранам. Когда включаются деацетилазы хозяина, SnCE1 отрезается и высвобождается, перераспределяясь к митохондриям и дополнительно изменяя внутренний ландшафт клетки. Привязывая вирулентность к маленьким химическим меткам, отражающим метаболизм клетки, бактерия может регулировать степень своей манипуляции хозяином — что демонстрирует сложную стратегию, которая, возможно, встречается и у других внутриклеточных патогенов.
Цитирование: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Ключевые слова: регуляция вирулентности бактерий, ацетилирование белков, де-конъюгация SUMO, взаимодействия хозяин–патоген, митохондриальная динамика