Clear Sky Science · ja
リジンのアセチル化による細菌毒性の再プログラミング
細菌はどのように攻撃を調整するか
多くの有害な細菌は宿主細胞内に生息し、宿主をあまりにも早く死に至らせないように振る舞う必要があります。本研究は、そうした微生物の一つがごく小さな化学的タグであるアセチル化を使って攻撃性を微調整する仕組みを明らかにします。主要な病原因子タンパク質にこのタグを付けることで、細菌はそのタンパク質の形状、局在、活性を切り替え、宿主細胞のエネルギー状態に合わせて攻撃手段を強めたり弱めたりできます。
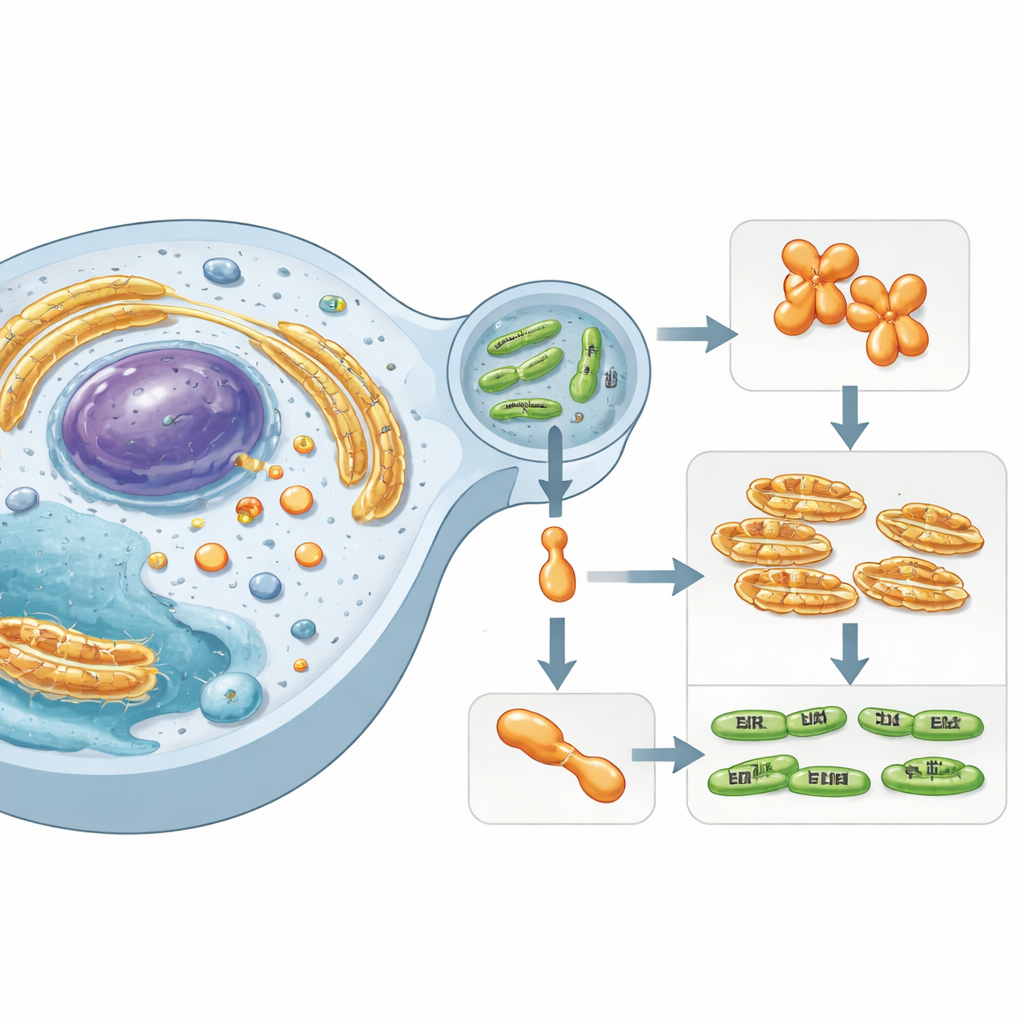
ヒト細胞内部の隠れた役者
研究は、慢性的な呼吸器感染と関連するクラミジア様細菌であるSimkania negevensisに焦点を当てています。この微生物はヒト細胞内の膜に囲まれた泡の中で生存し、周囲の細胞質に特殊な“エフェクター”タンパク質を注入します。これらのエフェクターのひとつ、SnCE1は宿主のタンパク質に付与されるタグ付けシステムに干渉することが知られた酵素群に属します。ユビキチンやSUMOのような小さなタンパク質タグは、免疫、ストレス応答、細胞死を制御する細胞内の交通信号のように働きます。SUMOやユビキチンの鎖を攪乱することで、細菌は宿主の防御を妨害し、より居心地のよいニッチを作り出せます。
二重機能の分子スイッチ
研究者らは、SnCE1が真のマルチタスク酵素であることを示しています。一方でそれは効率的な“脱SUMO化酵素”であり、ユビキチン鎖を切断するよりもはるかに容易にSUMO鎖を単位に切り分けます。高解像度の結晶構造は、SnCE1が表面のポケットでSUMO分子を把握し、適切に配置された帯電領域や疎水領域を使ってユビキチンよりもSUMOを優先する仕組みを示します。他方で、SnCE1は自己アセチルトランスフェラーゼとしても振る舞い、細胞の燃料分子であるアセチル‑CoAからアセチル基を取り、自身の複数のリジン残基に付与します。驚くべきことに、両方の活性は同じ触媒中心を共有するため、この酵素はSUMOを切るか自身を修飾するかの選択を迫られます。
エフェクターの形作り、クラスタ化、切断
アセチル化はSnCE1の組み立て方を再構築することが判明しました。修飾されていない触媒不活性型のタンパク質は四量体、すなわち四つのユニットのクラスタを形成する傾向があります。構造解析は、サブユニット間の界面がSUMOが通常結合する部位を塞いでおり、このクラスタ化した形は脱SUMO化に適さないことを示しています。特に位置231のリジンを含む特定のリジンがアセチル化されると、この塩橋に基づく界面は形成できなくなり、SnCE1は単独のモノマーとして存在します。これらの単量体はSUMO結合溝が開いており、強い脱SUMO化活性を示します。重要なのは、Lys231のアセチル化は、試験したヒトおよび細菌の脱アセチル化酵素の下でも不可逆的であるように見え、この修飾が起こるとSnCE1は活性な単量体状態に固定される点です。
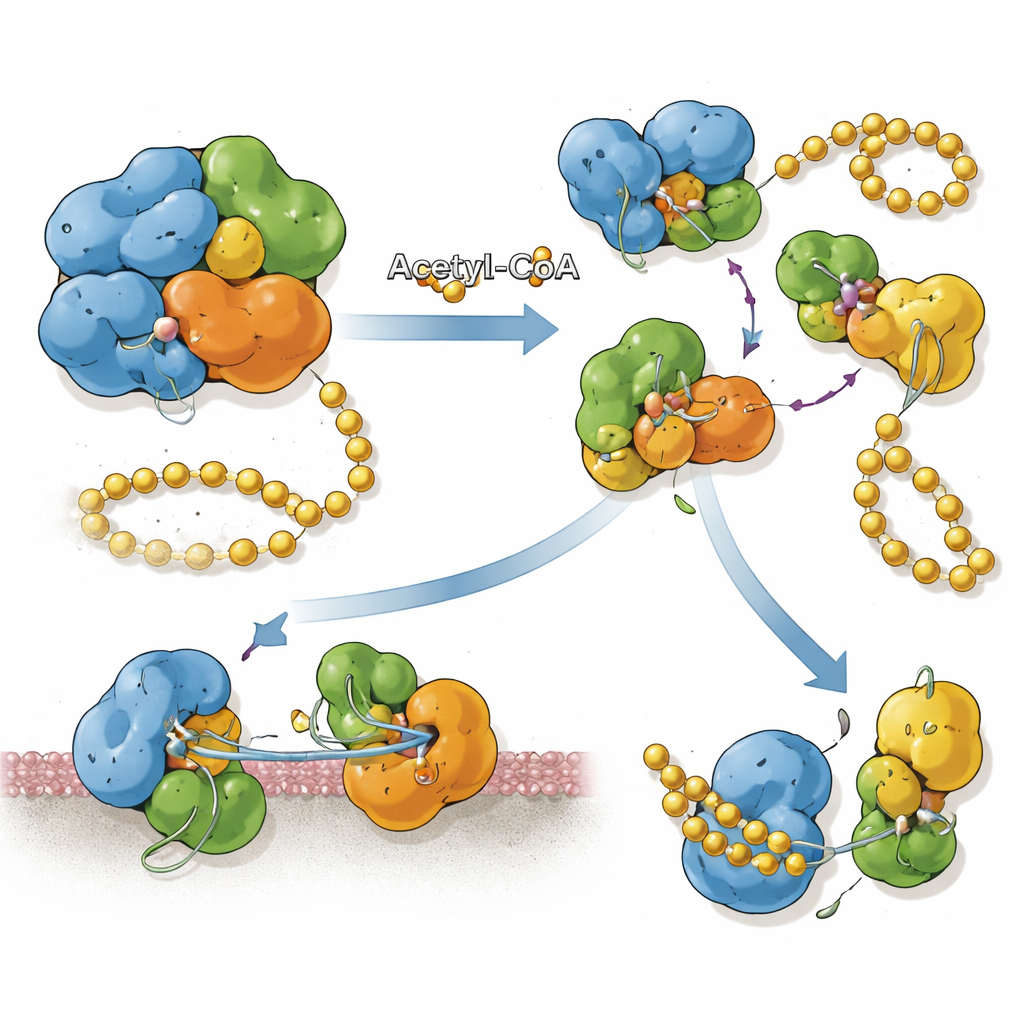
化学的タグとタンパク質局在の連結
SnCE1はN末端セグメントを持っており、これは膜アンカーのように振る舞って細菌の胞嚢膜や近傍の小胞体に付着するのを助けます。研究チームは、N末端領域の複数のリジンが強くアセチル化されていると、タンパク質は全長のままで膜結合した状態を保つことを見出しました。宿主のシルトゥインなどの酵素がこれらのアセチルマークの一部を除去すると、SnCE1は自己切断を起こし、N末端から約10キロダルトンが切り取られ、膜アンカーが失われます。この自己プロテオリティックな処理によりSnCE1は周囲の細胞質へと放出され、ミトコンドリアへ向かいます。部位特異的なアセチル化実験は、この段階を制御する単一のリジンは存在せず、むしろ複数のアセチル化部位が集合的に切断を遅らせるか阻止することを示しています。
ミトコンドリアと宿主代謝への影響
ヒト細胞内で全長のSnCE1は小胞体やミトコンドリアと接する接触点に集積し、そこではミトコンドリアの形状に顕著な変化が一致して観察されます。触媒活性の有無にかかわらず、SnCE1の発現は通常は管状のミトコンドリアネットワークの断片化を促進し、最も強い効果は非アセチル化の単量体変異体で見られ、これは容易に処理されます。ミトコンドリアのダイナミクスはエネルギー産生や細胞生存と密接に結びついているため、この再構築は細胞が細菌増殖にどれだけ好適かに影響を与えると考えられます。著者らは、宿主細胞内のアセチル‑CoAとNAD+のバランス(代謝状態の化学的指標)がSnCE1のアセチル化、脱アセチル化、処理を制御し、それによってその活性と局在を時空間的に調節すると提案しています。
細菌病原因性における新たな制御層
平たく言えば、この研究はSimkaniaが主要な武器の一つに対してアセチル化を調光器として利用していることを示しています。アセチル基が豊富なとき、SnCE1は安定した活性単量体となり効率的にSUMOタグを消去して宿主のシグナル伝達を書き換えつつ膜に付着したままでいられます。宿主の脱アセチル化酵素が作用すると、SnCE1は切断されて放出され、ミトコンドリアへ再分配して細胞の内部景観をさらに変化させます。病原因性を細胞代謝を反映する小さな化学タグに結び付けることで、細菌は宿主をどれだけ積極的に操作するかを調整できるようになり、この精巧な戦略は他の細胞内病原体にも共通している可能性があります。
引用: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
キーワード: 細菌の病原因性制御, タンパク質のアセチル化, SUMOの脱結合, 宿主–病原体相互作用, ミトコンドリアのダイナミクス