Clear Sky Science · ar
إعادة برمجة ضراوة البكتيريا عبر أستلة اللايزين
كيف تضبط البكتيريا هجومها
تعيش العديد من البكتيريا الضارة داخل خلايانا ويجب أن تتجنّب قتل العائل بسرعة مفرطة. تكشف هذه الدراسة كيف يضبط أحد هذه الميكروبات عدوانيته باستخدام وسم كيميائي صغير يُسمى الأستلة. عن طريق تزيين بروتين ضراوة رئيسي بهذا الوسم، تستطيع البكتيريا تغيير شكل البروتين وموقعه ونشاطه، لتقوم فعليًا بزيادة أو تقليل أدواتها الهجومية لتتماشى مع حالة طاقة خلية العائل.
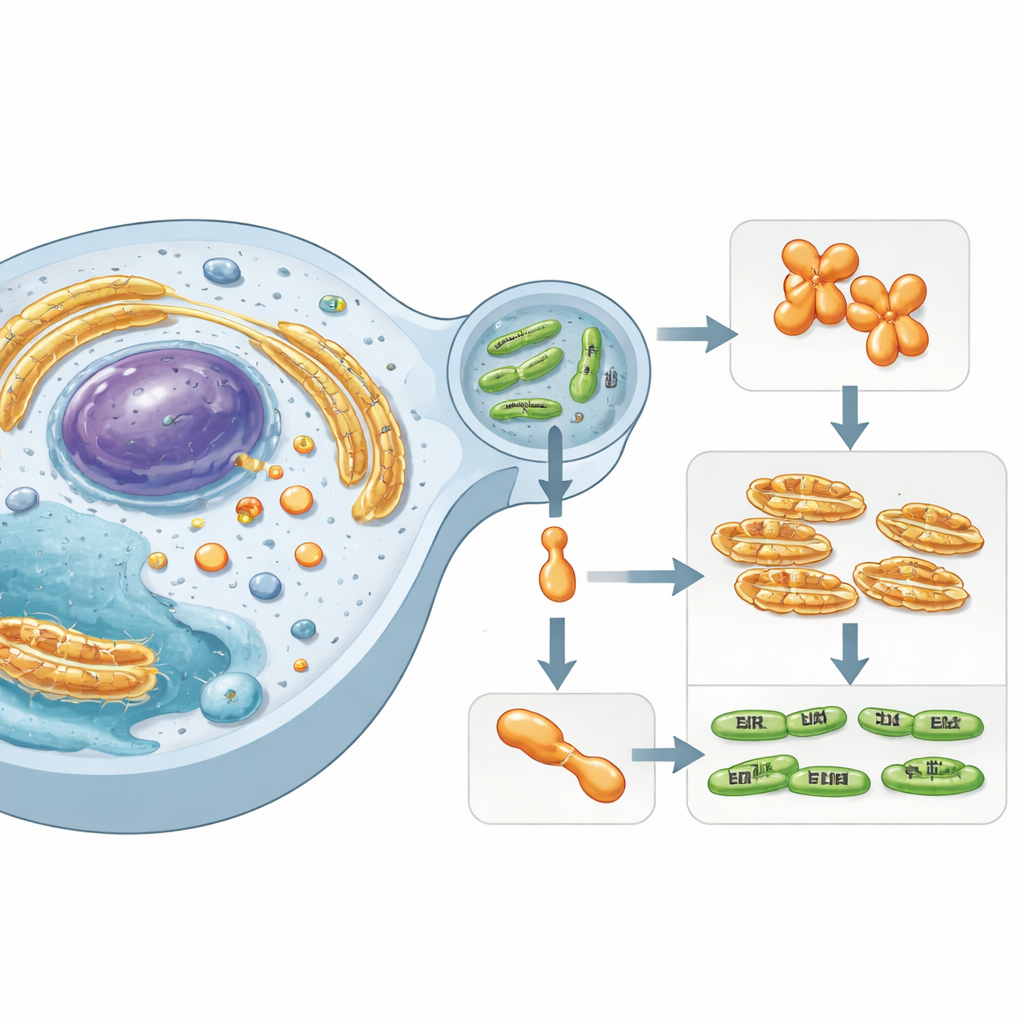
لاعب خفي داخل الخلايا البشرية
تركز هذه الدراسة على Simkania negevensis، بكتيريا شبيهة بالكلاميديا مرتبطة بالتهابات تنفُّسية مستمرة. تعيش هذه الميكروب داخل حويصلة محاطة بغشاء داخل الخلايا البشرية وتحقن بروتينات متخصِّصة تسمى «عوامل فاعلة» إلى السيتوبلازم المحيط. أحد هذه العوامل، المسمى SnCE1، ينتمي إلى عائلة من الإنزيمات المعروفة بتعطيل أنظمة وسم البروتين لدى العائل. تعمل هذه الوسوم — وهي بروتينات صغيرة مثل يوبيةوتين وSUMO — كإشارات مرورية خلوية تتحكم بالمناعة واستجابات الإجهاد وموت الخلية. يتيح تعطيل سلاسل SUMO ويوبيةوتين للبكتيريا تخريب دفاعات العائل وتهيئة بيئة أكثر ملاءمة لبقائها.
مفتاح جزيئي ذو وظيفتين
يُظهر الباحثون أن SnCE1 متعدد المهام بالفعل. من جهة، هو «مزيل SUMO» فعال: يجزّء سلاسل SUMO إلى وحدات مفردة بسهولة أكبر بكثير من قدرته على قص سلاسل اليوبيةوتين. تكشف هياكل بلورية عالية الدقة كيف يمسك SnCE1 بجزيء SUMO في جيب سطحي، مستخدمًا مناطق مشحونة وهيدروفوبية موضوعة بدقة لتفضيل SUMO على اليوبيةوتين. من جهة أخرى، يعمل SnCE1 أيضًا كناقل أستيل ذاتي: يأخذ مجموعات أستيل من جزيء الوقود الخلوي أسيتيل‑CoA ويلصقها بعدة بقايا لايزين خاصة به. والمفاجئ أن كلا النشاطين تستخدمان نفس المركز الحفازي، لذا على الإنزيم أن يختار بين قص SUMO وتعديل نفسه.
تشكيل العامل وتجمعه وقطعه
تبيّن الأستلة أنها تعيد تشكيل كيفية تجميع SnCE1. عندما يكون غير مُعدّل، يميل نسخة غير فعالة حفازيًا من البروتين لتشكيل رباعيات — تجمعات من أربع وحدات. تُظهر التحليلات التركيبية أن الواجهات بين الوحدات تسد الموقع الذي سيرتبط به SUMO عادةً، مما يجعل هذا الشكل المُجمّع غير مناسب لإزالة SUMO. عندما تُستَلَّ بعض اللايزينات المحددة، وخصوصًا واحدة عند الموضع 231، لا يستطيع هذا التداخل المبني على جسور ملحية أن يتكوّن، ويصبح SnCE1 كائنات مفردة منفصلة. تملك هذه الوحدات المفردة شقًا مفتوحًا لالتقاط SUMO وتظهر نشاطًا قويًا كمزيل SUMO. والأهم أن أستلة لايزين 231 تبدو غير قابلة للعكس أمام جميع الديازيلات البشرية والبكتيرية المختبرة، مما يقفل SnCE1 في حالته النشطة المفردة بمجرد حصول هذا التعديل.
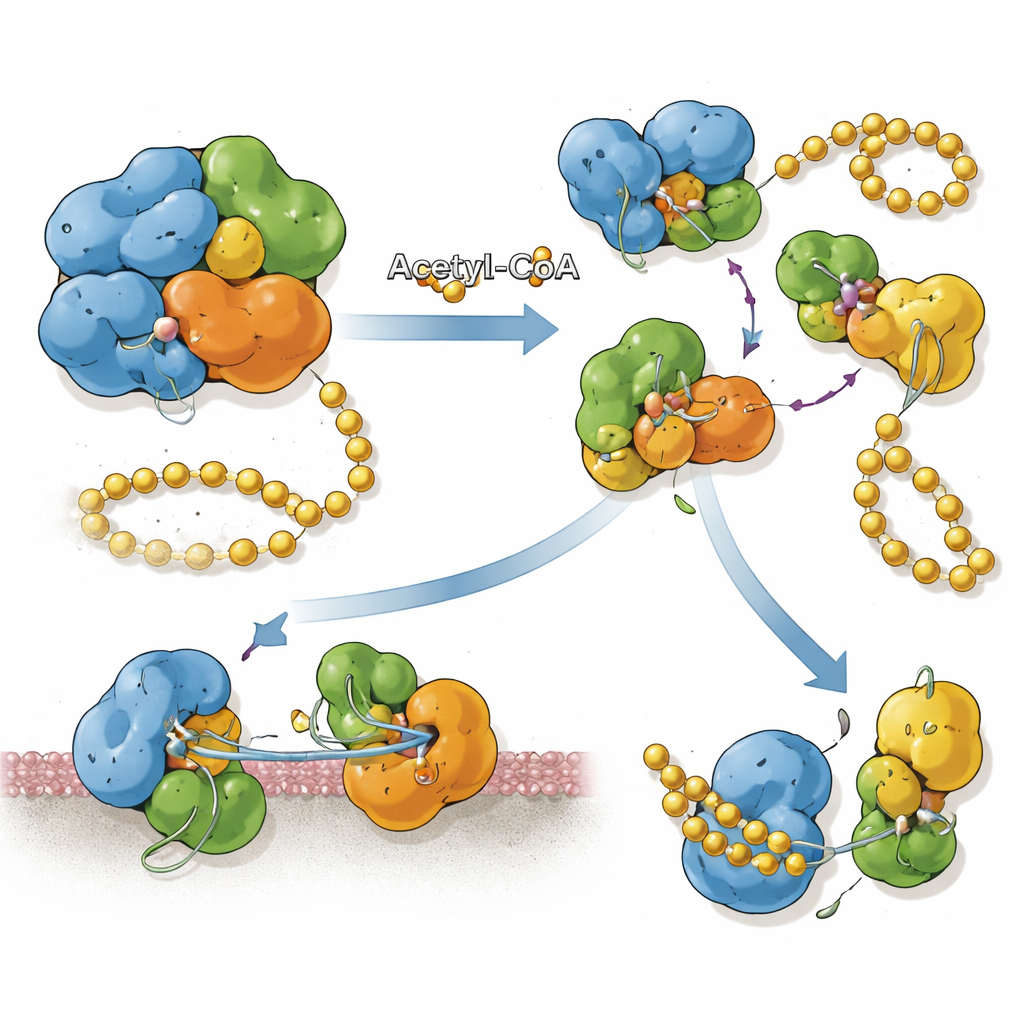
ربط الوسوم الكيميائية بموقع البروتين
يُنتَج SnCE1 مزوَّدًا بمقطع طرفي N يتصرف كمرساة غشائية، مما يساعده على الارتباط بغشاء الحويصلة البكتيرية والشبكة الإندوبلازمية المجاورة. وجد الفريق أنه عندما يكون SnCE1 مُستَلًا بكثافة على عدة لايزينات في هذا المقطع الطرفي N، يبقى البروتين كامل الطول ومرتبطًا بالغشاء. عندما تزيل إنزيمات العائل المسماة سيرتوينات بعض هذه العلامات الأستيلية، يخضع SnCE1 لحدث قص ذاتي يقطع نحو عشرة كيلودالتون تقريبًا من طرفه N، بما في ذلك مرساة الغشاء. هذا المعالجة البروتيزية الذاتية تُطلق SnCE1 إلى السيتوبلازم المحيط وتعيد توزيعه نحو الميتوكوندريا. تُظهر تجارب أستلة موقعية أن لايزينًا واحدًا منفردًا لا يتحكم بهذه الخطوة؛ بل تعدد المواقع المؤستلة يبطئ أو يمنع القطع بصورة جماعية.
التأثير على الميتوكوندريا وأيض العائل
داخل الخلايا البشرية، يتركز SnCE1 كامل الطول عند الشبكة الإندوبلازمية ونقاط التماس مع الميتوكوندريا، حيث يتزامن مع تغيّرات واضحة في شكل الميتوكوندريا. سواء كان نشطًا حفازيًا أم لا، فإن تعبیر SnCE1 يعزز تجزؤ الشبكة الميتوكوندرية الأنبوبية الاعتيادية، مع أقوى تأثير لدى طفرة مفردة غير مُستَلَّة ومفردة تُعالَج بسرعة. ونظرًا لأن ديناميكيات الميتوكوندريا مرتبطة ارتباطًا وثيقًا بإنتاج الطاقة وبقاء الخلية، فمن المرجح أن يؤثر هذا إعادة التشكيل على مدى ملاءمة الخلية لنمو البكتيريا. يقترح المؤلفون أن توازن أسيتيل‑CoA وNAD+ داخل خلية العائل — قراءات كيميائية للحالة الأيضية — يتحكم في أستلة SnCE1 وإزالة أستلاته ومعالجته، وبالتالي يضبط نشاطه وموقعه مكانيًا وزمنيًا.
طبقة جديدة من التحكم في ضراوة البكتيريا
بعبارة مبسطة، تُظهر هذه الدراسة أن Simkania تستخدم الأستلة كمفتاح خافِت لأسلحتها الرئيسية. عندما تكون مجموعات الأستيل متوفرة بكثرة، يصبح SnCE1 مونو ميرًا مستقرًا ونشطًا يمحو علامات SUMO بكفاءة، مما يساعد البكتيرية على إعادة برمجة إشارات العائل بينما تبقى مرتبطة بالغشاء. عندما تنشط نازعات الأستلة لدى العائل، يُقصّ SnCE1 ويُحرر، فيتجه نحو الميتوكوندريا ويعيد تشكيل المشهد الداخلي للخلية. بربط الضراوة بوسوم كيميائية صغيرة تعكس الأيض الخلوي، تستطيع البكتيريا تعديل مدى تلاعبها بالعائل، ما يكشف عن استراتيجية متطورة قد تشترك فيها مسببات مرض داخلية أخرى.
الاستشهاد: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
الكلمات المفتاحية: تنظيم ضراوة البكتيريا, أستلة البروتين, فك اقتران SUMO, تفاعلات العائل ـ الممرض, ديناميكيات الميتوكوندريا