Clear Sky Science · de
Umschaltung bakterieller Virulenz durch Lysin‑Acetylierung
Wie Bakterien ihren Angriff abstimmen
Viele schädliche Bakterien leben in unseren Zellen und müssen verhindern, ihren Wirt zu schnell zu töten. Diese Studie zeigt, wie ein solcher Erreger seine Angriffslust über einen winzigen chemischen Marker namens Acetylierung feinjustiert. Indem das Bakterium ein zentrales Virulenzprotein mit diesem Marker versieht, kann es dessen Form, Lokalisation und Aktivität verändern und so seine Angriffsmechanismen je nach Energielage der Wirtszelle hoch- oder herunterregeln.
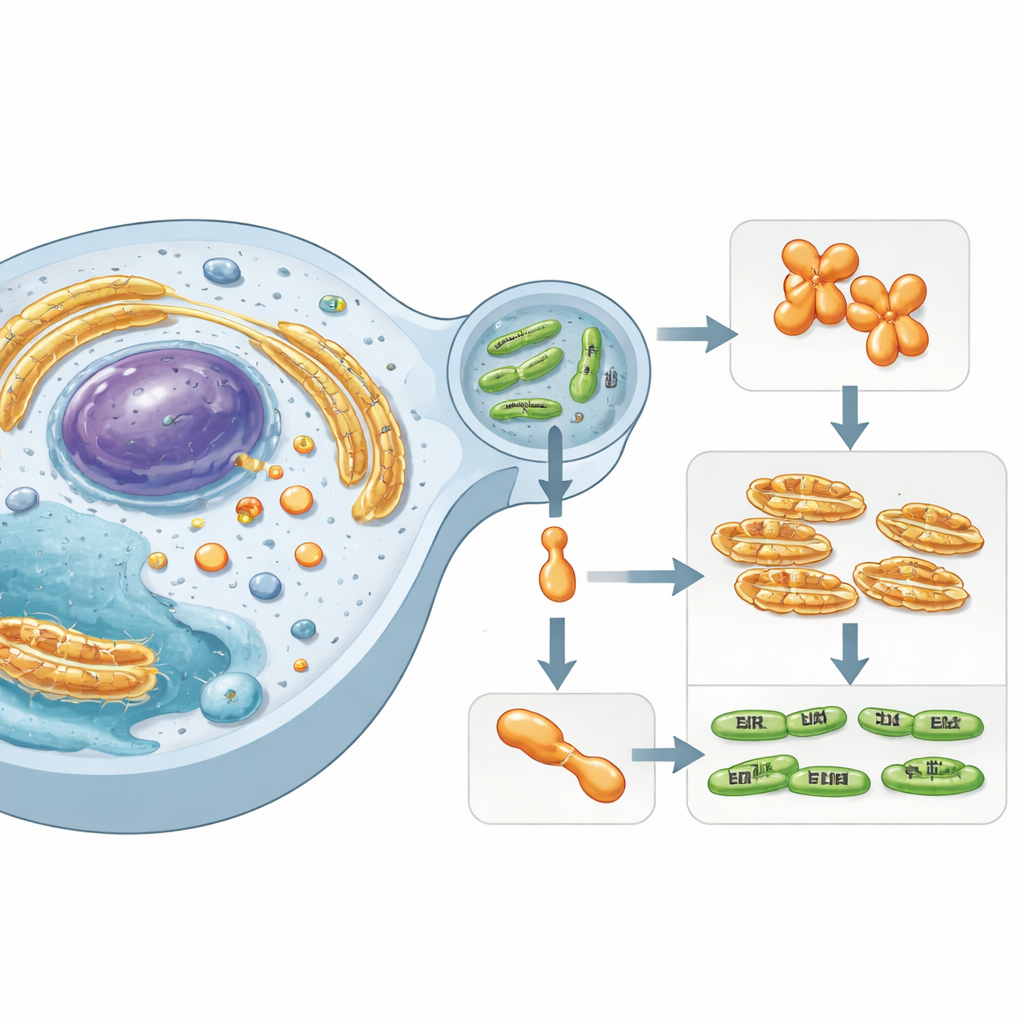
Ein verborgener Akteur in menschlichen Zellen
Die Arbeit konzentriert sich auf Simkania negevensis, ein chlamydienähnliches Bakterium, das mit langanhaltenden Atemwegsinfektionen in Verbindung gebracht wird. Dieser Keim überlebt innerhalb einer membranumgrenzten Blase in menschlichen Zellen und schleust spezialisierte „Effektor“-Proteine in das umgebende Zytoplasma. Einer dieser Effektoren, SnCE1 genannt, gehört zu einer Enzymfamilie, die dafür bekannt ist, in die Protein‑Markierungssysteme des Wirts einzugreifen. Diese Marker — kleine Proteine wie Ubiquitin und SUMO — fungieren als zelluläre Verkehrssignale und steuern Immunantworten, Stressreaktionen und den Zelltod. Durch das Stören von SUMO‑ und Ubiquitin‑Ketten können Bakterien die Abwehr des Wirts sabotieren und ein günstigeres Nischenmilieu schaffen.
Ein molekularer Schalter mit Doppelrolle
Die Forschenden zeigen, dass SnCE1 ein echtes Multitalent ist. Einerseits ist es ein effizientes „DeSUMOylase“: Es spaltet SUMO‑Ketten in einzelne Einheiten deutlich leichter als Ubiquitin‑Ketten. Hochaufgelöste Kristallstrukturen legen dar, wie SnCE1 ein SUMO‑Molekül in einer Oberflächentasche hält und über präzise angeordnete geladene und hydrophobe Bereiche SUMO gegenüber Ubiquitin bevorzugt. Andererseits agiert SnCE1 auch als Auto‑Acetyltransferase: Es nimmt Acetylgruppen vom zellulären Brennstoffmolekül Acetyl‑CoA auf und hängt sie an mehrere seiner eigenen Lysinreste. Überraschenderweise nutzen beide Aktivitäten dasselbe katalytische Zentrum, sodass das Enzym zwischen dem Schneiden von SUMO und der Modifikation seiner selbst wählen muss.
Formung, Clusterbildung und Spaltung des Effektors
Acetylierung verändert offenbar die Assemblierung von SnCE1. Unmodifiziert neigt eine katalytisch inaktive Form dazu, Tetramere zu bilden — Vierer‑Cluster. Strukturanalysen zeigen, dass die Schnittstellen zwischen Untereinheiten die Stelle blockieren, an der SUMO normalerweise binden würde, sodass diese geclusterte Form für die DeSUMOylierung ungeeignet ist. Werden bestimmte Lysinreste, insbesondere der an Position 231, acetylierter, kann diese Salzbrücken‑basierte Schnittstelle nicht mehr ausgebildet werden, und SnCE1 liegt als einzelne Monomere vor. Diese Einzelteile besitzen eine offene SUMO‑Bindungsrinne und zeigen starke DeSUMOylase‑Aktivität. Wichtig ist, dass die Acetylierung an Lys231 unter allen getesteten menschlichen und bakteriellen Deacetylasen offenbar irreversibel ist, wodurch SnCE1 nach Eintritt dieser Modifikation dauerhaft in seinem aktiven, monomeren Zustand verharrt.
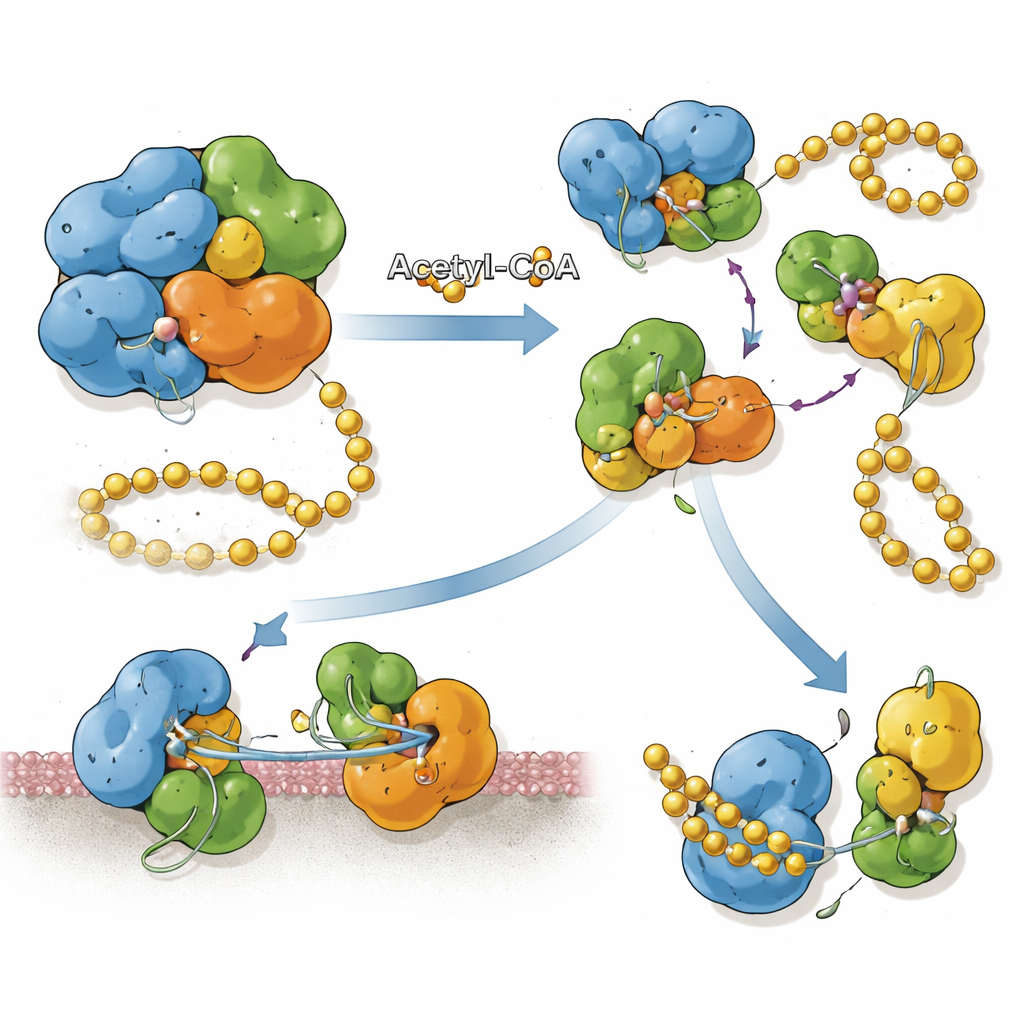
Verknüpfung chemischer Marker mit Proteinposition
SnCE1 wird mit einem N‑terminalen Abschnitt produziert, der wie ein Membrananker wirkt und ihm hilft, an die Membran der bakteriellen Vakuole und an das nahe gelegene endoplasmatische Retikulum zu binden. Die Forscher fanden heraus, dass bei starker Acetylierung mehrerer Lysinreste in diesem N‑terminalen Bereich das Protein als volle Länge membrangebunden bleibt. Entfernen Wirt‑Enzyme, sogenannte Sirtuine, einige dieser Acetylmarken, so durchläuft SnCE1 ein selbstvermitteltes Spaltungsereignis, bei dem etwa 10 Kilodalton vom N‑Termin abgeschnitten werden, einschließlich des Membranankers. Diese autoproteolytische Verarbeitung setzt SnCE1 ins umliegende Zytosol frei und richtet es auf die Mitochondrien aus. Standortspezifische Acetylierungsversuche zeigen, dass kein einzelnes Lysin diesen Schritt allein steuert; vielmehr bremsen oder verhindern mehrere acetylierte Stellen zusammen das Schneiden.
Auswirkung auf Mitochondrien und Wirtsstoffwechsel
In menschlichen Zellen sammelt sich das voll‑längige SnCE1 am endoplasmatischen Retikulum und an Kontaktstellen zu Mitochondrien, wo es mit markanten Veränderungen der Mitochondrienform einhergeht. Unabhängig von katalytischer Aktivität fördert die Expression von SnCE1 die Fragmentierung des normalerweise röhrenförmigen Mitochondriennetzwerks, am stärksten ausgeprägt bei einem nicht‑acetylierten, monomeren Mutanten, der leicht verarbeitet wird. Da die mitochondriale Dynamik eng mit Energieproduktion und Zellüberleben verknüpft ist, beeinflusst diese Umgestaltung wahrscheinlich, wie gastlich die Zelle für bakterielles Wachstum ist. Die Autoren schlagen vor, dass das Verhältnis von Acetyl‑CoA zu NAD+ in der Wirtszelle — chemische Indikatoren des Stoffwechselzustands — die Acetylierung, Deacetylierung und Verarbeitung von SnCE1 steuert und damit seine Aktivität und Lokalisation räumlich und zeitlich reguliert.
Eine neue Kontrollschicht bakterieller Virulenz
Alltäglich gesprochen zeigt diese Studie, dass Simkania Acetylierung als Dimmer für eine seiner Schlüsselwaffen nutzt. Sind Acetylgruppen reichlich vorhanden, wird SnCE1 zu einem stabilen, aktiven Monomer, das SUMO‑Marker effizient entfernt und dem Bakterium hilft, die Signalwege des Wirts umzuprogrammieren, während es an Membranen gebunden bleibt. Aktivieren wirtsseitige Deacetylasen, so wird SnCE1 beschnitten und freigesetzt, wandert zu den Mitochondrien und verändert weiter die innere Zellarchitektur. Indem das Pathogen Virulenz an kleine chemische Marker bindet, die den zellulären Stoffwechsel abbilden, kann es seine Manipulationsstrategie fein abstimmen — eine ausgeklügelte Taktik, die möglicherweise auch von anderen intrazellulären Erregern genutzt wird.
Zitation: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Schlüsselwörter: Regulation bakterieller Virulenz, Proteinacetylierung, SUMO‑Dekonjugation, Wirt–Pathogen‑Interaktionen, mitochondriale Dynamik