Clear Sky Science · he
תכנות מחדש של זיהומיות חיידקית על‑ידי אצטילציה של ליזין
איך חיידקים מווסתים את התקפתם
רבים מהחיידקים המזיקים מתקיימים בתוך תאי המארח וחייבים להימנע מלגרום למותו מהר מדי. מחקר זה מגלה כיצד מיקרואורגניזם כזה מווסת בעדינות את הפגיעה שלו באמצעות תג כימי קטן שנקרא אצטילציה. על‑ידי קישוט חלבון זיהומיות מפתח בתג זה, החיידק יכול לשנות את צורתו, מיקומו ופעילותו של החלבון — ובאופן יעיל להעלות או להוריד את כלי ההתקפה שלו בהתאם למצב האנרגיה של תא המארח.
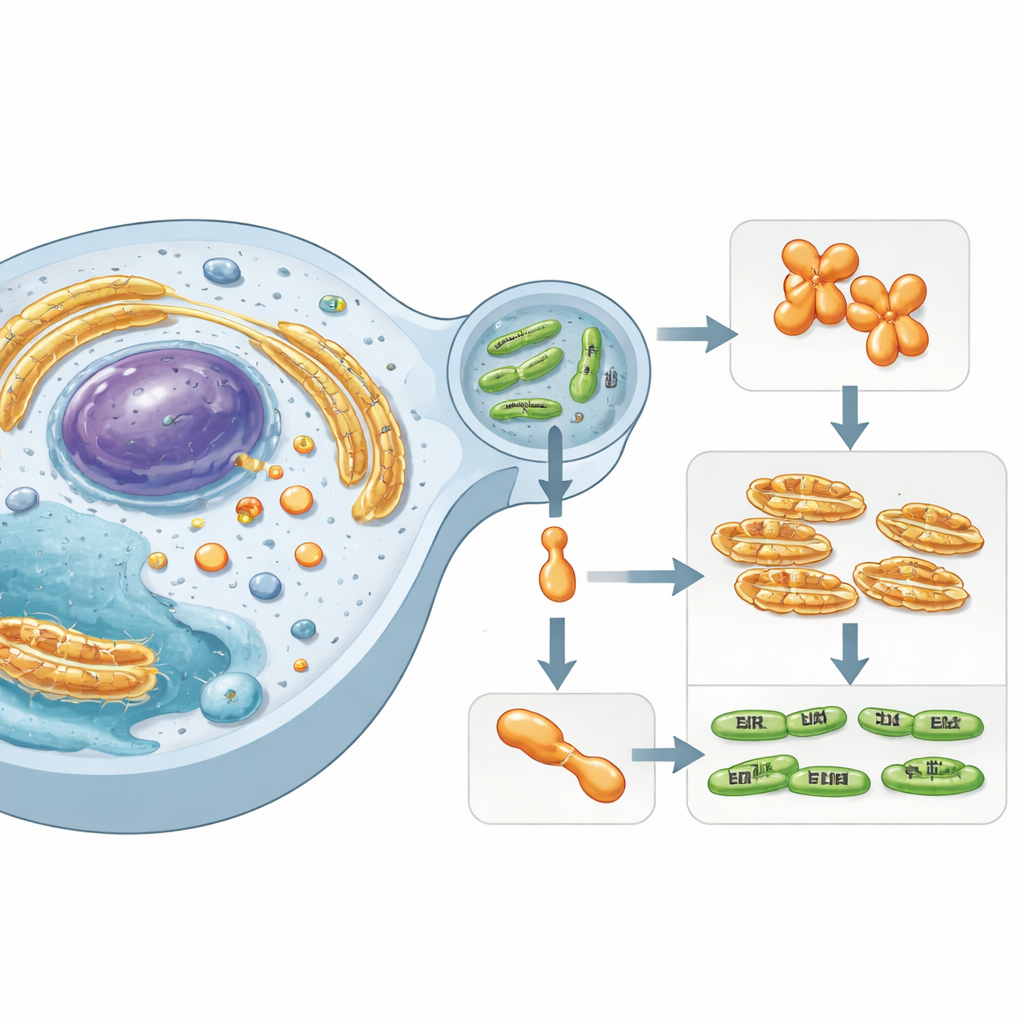
שחקן חבוי בתוך תאים אנושיים
העבודה מתמקדת ב‑Simkania negevensis, חיידק דמוי כלמידיה המקושר לזיהומי נשימה ממושכים. המיקרוב הזה שורד בתוך בועה עטופה ממברנה בתוך תאי האדם ומזריק חלבוני “אפקטור” מיוחדים לציטופלזמה שמסביב. אחד מהאפקטורים הללו, הנקרא SnCE1, שייך למשפחת אנזימים הידועה בהתערבותה במערכות תגי־החלבון של המארח. תגיות אלה — חלבונים קטנים כמו יוביקוויטין ו‑SUMO — פועלות כסימני תנועה תאיים, ומווסתות חיסון, תגובות למתח ומוות תאי. פגיעה בשרשראות SUMO ויוביקוויטין מאפשרת לחיידקים לסכל הגנות המארח וליצור משכן ידידותי יותר.
מתג מולקולרי בעל שתי פונקציות
החוקרים מראים ש‑SnCE1 הוא רב משימתי אמיתי. מצד אחד, הוא “דיא‑SUMOילאז” יעיל: הוא חותך שרשראות SUMO ליחידות בודדות ביתר קלות מאשר חותך שרשראות יוביקוויטין. מבני קריסטל ברזולוציה גבוהה חושפים כיצד SnCE1 אוחז מולקולת SUMO בכיס פני שטח, תוך שימוש באזורים טעונים והידרופוביים ממוקמים בדיוק שמעדיפים SUMO על פני יוביקוויטין. מצד שני, SnCE1 גם מתפקד כאצטיל‑טרנספרז אוטו־קטלי: הוא לוקח קבוצות אצטיל מהמולקולה הדלקתית תיאצטיל‑CoA ומצמיד אותן למספר שיירי ליזין שלו עצמו. באופן מפתיע, שתי הפעילויות משתמשות במרכז קטליטי זהה, ולכן האנזים חייב לבחור בין חיתוך SUMO לבין שינוי עצמי.
עיצוב, אשכולות וחיתוך האפקטור
ניתן לראות כי האצטילציה משנה את אופן ההרכבה של SnCE1. כשהוא לא מומתן, גרסה קטליטית לא פעילה של החלבון נוטה ליצור טטראמרים — אשכולות של ארבע יחידות. ניתוח מבני מראה שהממשקים בין תת‑היחידות חוסמים את האתר שבו SUMO היה נקשר בדרך כלל, מה שהופך את הצורה המאוחדת הזו ללא מתאימה לפעולת דיא‑SUMOילציה. כאשר ליזינים ספציפיים, ובמיוחד זה במיקום 231, עוברים אצטילציה, ממשק המבוסס על גשרים מלחים אינו יכול עוד להיווצר, ו‑SnCE1 קיים כחד־יחידות נפרדות. יחידות בודדות אלה מציגות חריץ קיבוע SUMO פתוח ומראות פעילות דיא‑SUMOילאז חזקה. חשוב לציין שאצטילציה בליזין 231 נראית כבלתי הפיכה תחת כל הדיא‑אצטילאזות האנושיות והחיידקיות שנבדקו, ולכן מנעילה את SnCE1 למצבו הפעיל והמונומרי ברגע שהשינוי מתרחש.
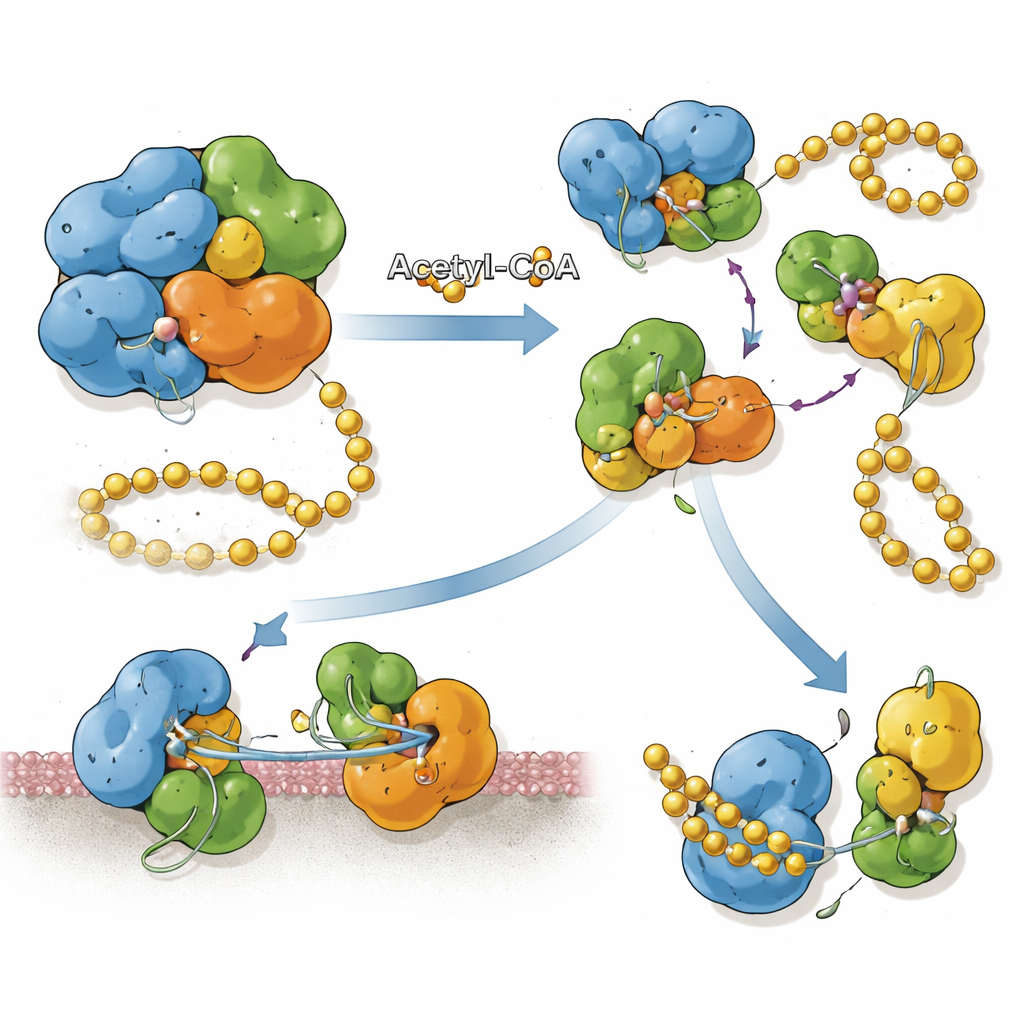
קישור תגיות כימיות למיקום החלבון
SnCE1 מיוצר עם מקטע N‑טרמינלי המתנהג כעוגן ממברנאלי, המסייע לו להתחבר לממברנת הוויקולה החיידקית ולרשת האנדופלסמית הקרובה. הקבוצה מצאה שכאשר SnCE1 מאוסטל בכבדות על מספר ליזינים באזור ה‑N‑טרמינלי הזה, החלבון נשאר באורכו המלא וקשור לממברנה. כאשר אנזימים של המארח שנקראים סירטואינים מסירים חלק מסימני האצטיל, SnCE1 עובר אירוע חיתוך עצמי שמקצר ממנו בערך 10 קילו‑דלטון מהקצה ה‑N, כולל עוגן הממברנה. עיבוד אוטופרו־טאוליטי זה משחרר את SnCE1 לציטוזול ושולח אותו לעבר המיטוכונדריה. ניסויים של אצטילציה מיקודנית מראים שאין ליזין יחיד השולט בצעד זה; במקום זאת, אתרי אצטילציה מרובים פועלים יחד ומאטו או מונעים את החיתוך.
השפעה על מיטוכונדריה ומטבוליזם המארח
בתאים אנושיים, SnCE1 באורכו המלא מרוכז ברשת האנדופלסמית ובנקודות מגע עם מיטוכונדריה, שם הוא מתיישב עם שינויים בולטים בצורת המיטוכונדריה. בין אם פעיל קטליטית ובין אם לאו, ביטוי של SnCE1 מקדם פירוק של הרשת המיטוכונדריאלית הצינורית הנורמלית, כאשר ההשפעה החזקה ביותר נראית במוטנט מונומרי שאינו אצטילציה ועמיד לחיתוך. מכיוון שדינמיקת המיטוכונדריה קשורה בקשר הדוק לייצור אנרגיה ולהישרדות התא, שינויים אלה ככל הנראה משפיעים על מידת הנכונות של התא לגידול החיידק. המחברים מציעים שאיזון בין תיאצטיל‑CoA ל‑NAD+ בתא המארח — מדדי המצב המטבולי — מכתיב את אצטילציית, דיא־אצטילציית ועיבוד SnCE1, ובכך מווסת את פעילותו ומיקומו במרחב ובזמן.
שכבה חדשה של שליטה בזיהומיות חיידקית
במילים פשוטות, המחקר מראה ש‑Simkania משתמשת באצטילציה כמתג דימור על אחד מנשקיה המרכזיים. כאשר קבוצות אצטיל בשפע, SnCE1 הופך למונומר יציב ופעיל שמוחק ביעילות תגי SUMO, מסייע לחיידק לשכתב איתותי מארח בעודו נשאר מחובר לממברנות. כאשר דיא‑אצטילאזות המארח מופעלות, SnCE1 נחתך ומשתחרר, מתפזר לעבר מיטוכונדריה ומשנה עוד יותר את הנוף התאי הפנימי. על‑ידי קשירת הזיהומיות לתגיות כימיות קטנות שעוקבות אחר מטבוליזם תאי, החיידק יכול להתאים עד כמה באגרסיביות הוא מנצל את המארח — אסטרטגיה מתוחכמת שעשויה להיות משותפת לפתוגנים תוך‑תאיים אחרים.
ציטוט: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
מילות מפתח: ויסות זיהומיות חיידקית, אצטילציה של חלבונים, התנתקות SUMO, אינטראקציות בין מארח לפתוגן, דינמיקה מיטוכונדריאלית