Clear Sky Science · pl
Przeprogramowanie wirulencji bakterii przez acetylację lizyny
Jak bakterie regulują swój atak
Wiele chorobotwórczych bakterii żyje wewnątrz naszych komórek i musi unikać zabicia gospodarza zbyt szybko. To badanie ujawnia, jak jeden z takich mikrobów dopasowuje swoją agresję przy pomocy niewielkiej chemicznej etykiety zwanej acetylacją. Poprzez oznaczanie kluczowego białka wirulencji tym znacznikiem bakteria może zmieniać kształt, lokalizację i aktywność tego białka, skutecznie regulując swoje narzędzia ofensywne w górę lub w dół w zależności od stanu energetycznego komórki gospodarza.
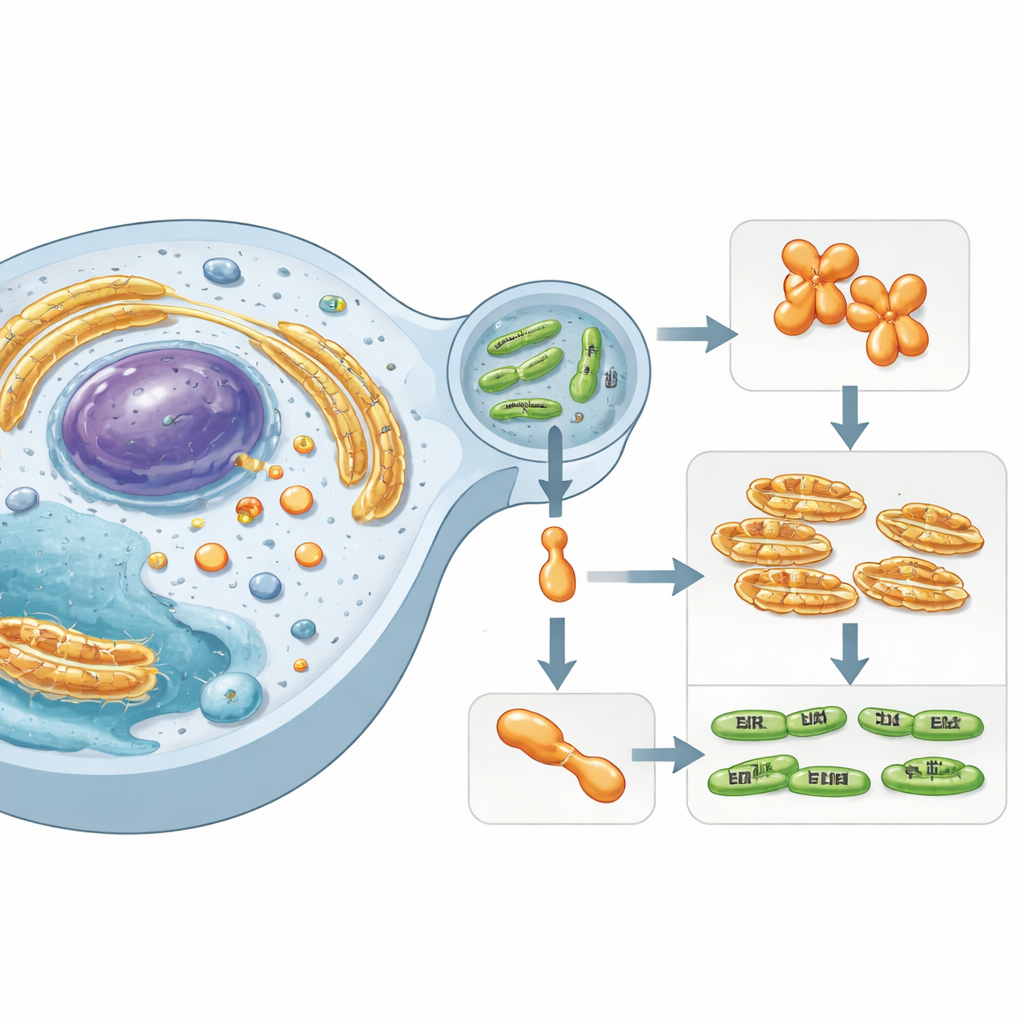
Ukryty gracz wewnątrz komórek ludzkich
Praca skupia się na Simkania negevensis, bakterii podobnej do Chlamydii związanej z przewlekłymi zakażeniami dróg oddechowych. Ten mikrob przeżywa wewnątrz otoczonego błoną pęcherzyka w komórkach ludzkich i wstrzykuje wyspecjalizowane „efektory” do otaczającego cytoplazmy. Jeden z tych efektorów, nazwany SnCE1, należy do rodziny enzymów znanych z ingerencji w systemy znakowania białek gospodarza. Te znaczniki — małe białka takie jak ubikwityna i SUMO — działają jak komórkowe sygnały drogowe, kontrolując odporność, odpowiedzi na stres i śmierć komórkową. Zakłócanie łańcuchów SUMO i ubikwityny pozwala bakteriom sabotować obronę gospodarza i tworzyć bardziej sprzyjające środowisko.
Dwufunkcyjny molekularny przełącznik
Naukowcy wykazali, że SnCE1 to prawdziwy multitasker. Z jednej strony jest wydajną „deSUMOylazą”: rozcina łańcuchy SUMO na pojedyncze jednostki znacznie chętniej niż przecina łańcuchy ubikwityny. Struktury krystaliczne o wysokiej rozdzielczości ujawniają, jak SnCE1 chwyta cząsteczkę SUMO w powierzchniowej kieszeni, wykorzystując precyzyjnie rozmieszczone regiony naładowane i hydrofobowe, by faworyzować SUMO ponad ubikwitynę. Z drugiej strony SnCE1 zachowuje się także jako autoacetylotransferaza: pobiera grupy acetylowe z komórkowej paliwowej cząsteczki acetyl‑CoA i przyłącza je do kilku własnych reszt lizynowych. Co zaskakujące, obie aktywności wykorzystują to samo centrum katalityczne, więc enzym musi wybierać między cięciem SUMO a modyfikowaniem samego siebie.
Formowanie, grupowanie i cięcie efektora
Okazuje się, że acetylacja przebudowuje sposób, w jaki SnCE1 się składa. Gdy jest niezmodyfikowany, katalitycznie nieaktywny wariant białka ma skłonność do tworzenia tetramerów — klastrów złożonych z czterech jednostek. Analiza strukturalna pokazuje, że interfejsy między podjednostkami blokują miejsce, do którego normalnie wiązałby się SUMO, czyniąc tę postać w postaci klastra nieodpowiednią do deSUMOylacji. Gdy określone lizyny, zwłaszcza ta na pozycji 231, zostają acetylowane, ten interfejs oparty na mostkach solnych nie może się już tworzyć i SnCE1 występuje jako oddzielne monomery. Te pojedyncze jednostki mają otwartą szczelinę wiążącą SUMO i wykazują silną aktywność deSUMOylazy. Co ważne, acetylacja Lys231 wydaje się być nieodwracalna przy zastosowaniu wszystkich przetestowanych ludzkich i bakteryjnych deacetylaz, blokując SnCE1 w jego aktywnym, monomerycznym stanie po zajściu tej modyfikacji.
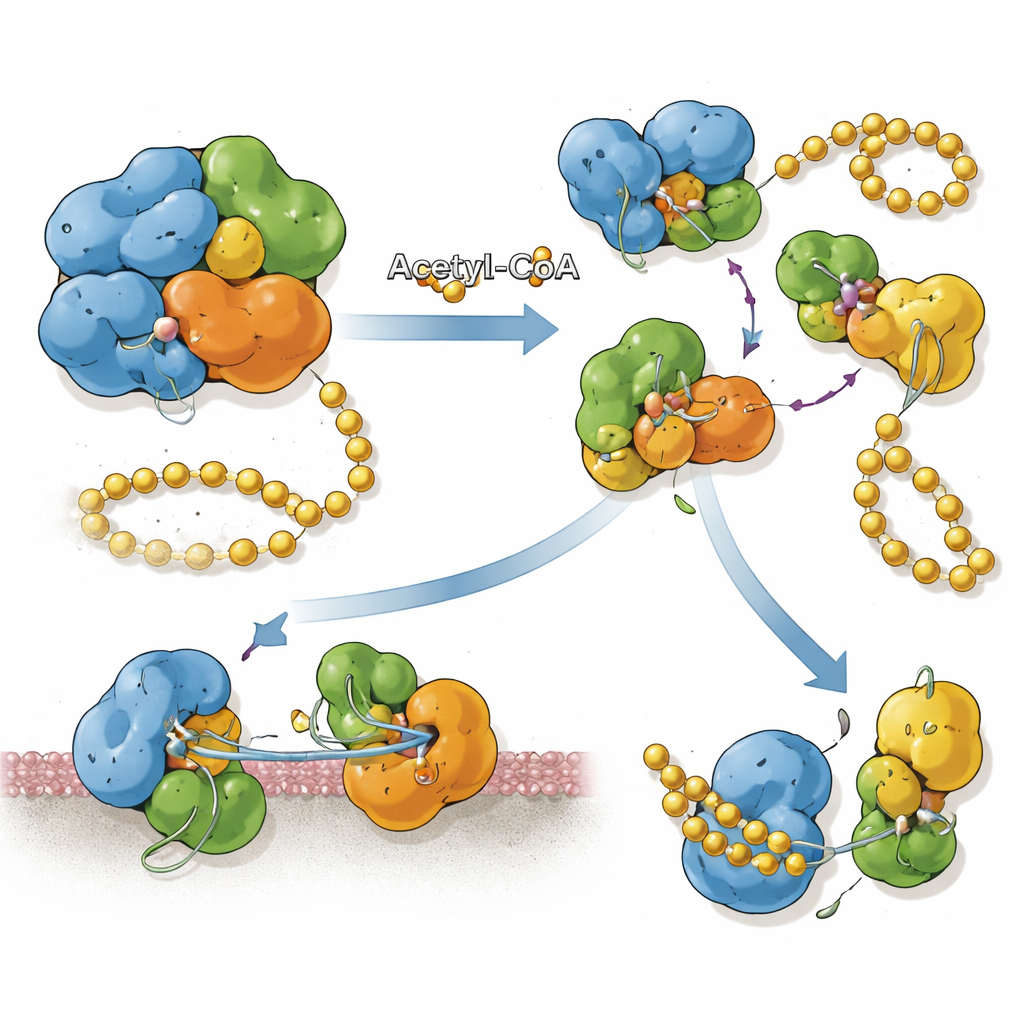
Powiązanie chemicznych znaczników z pozycją białka
SnCE1 jest produkowany z N‑terminalnym fragmentem zachowującym się jak kotwica błonowa, pomagającym mu przyłączać się do błony pęcherzyka bakteryjnego i pobliskiego retikulum endoplazmatycznego. Zespół odkrył, że gdy SnCE1 jest silnie acetylowany na kilku lizynach w tej N‑terminalnej części, białko pozostaje pełnej długości i związane z błoną. Gdy enzymy gospodarza zwane sirtuinami usuwają część tych znaków acetylowych, SnCE1 ulega autokatalitycznemu przecięciu, które odcina w przybliżeniu 10 kilodaltonów z jego N‑końca, włącznie z kotwicą błonową. To autoproteolityczne przetworzenie uwalnia SnCE1 do otaczającej cytosolu i w kierunku mitochondriów. Eksperymenty z miejscowo‑specyficzną acetylacją pokazują, że żaden pojedynczy lizyn nie kontroluje tego kroku; zamiast tego wiele zacetylowanych miejsc kolektywnie spowalnia lub zapobiega cięciu.
Wpływ na mitochondria i metabolizm gospodarza
W komórkach ludzkich pełnej długości SnCE1 koncentruje się przy retikulum endoplazmatycznym i w punktach kontaktu z mitochondriami, gdzie pokrywa się z uderzającymi zmianami kształtu mitochondriów. Niezależnie od tego, czy jest katalitycznie aktywny, czy nie, ekspresja SnCE1 sprzyja fragmentacji normalnie tubularnej sieci mitochondrialnej, przy najsilniejszym efekcie obserwowanym w nieacetylowanym, monomerycznym mutantcie, który jest łatwo przetwarzany. Ponieważ dynamika mitochondriów jest ściśle powiązana z produkcją energii i przeżyciem komórki, ta przebudowa prawdopodobnie wpływa na to, jak sprzyjające środowisko dla wzrostu bakterii jest w danej komórce. Autorzy proponują, że bilans acetyl‑CoA i NAD+ w komórce gospodarza — chemiczne wskaźniki stanu metabolicznego — reguluje acetylację, deacetylację i przetwarzanie SnCE1, tym samym dostrajając jego aktywność i lokalizację w przestrzeni i czasie.
Nowa warstwa kontroli wirulencji bakteryjnej
Mówiąc prościej, badanie pokazuje, że Simkania wykorzystuje acetylację jak ściemniacz jednego ze swoich kluczowych oręży. Gdy grupy acetylowe są obfite, SnCE1 staje się stabilnym, aktywnym monomerem, który skutecznie usuwa znaczniki SUMO, pomagając bakterii przeprogramować sygnalizację gospodarza, pozostając przy tym związanym z błonami. Gdy zaangażowane są deacetylazy gospodarza, SnCE1 jest przycinany i uwalniany, przemieszcza się w kierunku mitochondriów i dalej przebudowuje wewnętrzny krajobraz komórki. Wiążąc wirulencję z małymi chemicznymi znacznikami odzwierciedlającymi metabolizm komórki, bakteria może dostosować, jak agresywnie manipuluje gospodarzem, ujawniając wyszukaną strategię, która może być wspólna dla innych wewnątrzkomórkowych patogenów.
Cytowanie: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Słowa kluczowe: regulacja wirulencji bakterii, acetylacja białek, dekonjugacja SUMO, interakcje gospodarza i patogenu, dynamika mitochondriów