Clear Sky Science · sv
Omprogrammering av bakteriell virulens genom lysin‑acetylation
Hur bakterier finjusterar sitt angrepp
Många skadliga bakterier lever inne i våra celler och måste undvika att döda värden för snabbt. Denna studie avslöjar hur en sådan mikroorganism finjusterar sin aggression med hjälp av en liten kemisk markör kallad acetylation. Genom att klä ett nyckelprotein för virulens med denna etikett kan bakterien växla proteinets form, placering och aktivitet och därmed effektivt skruva upp eller ner sina offensiva verktyg för att matcha värdcellens energitillstånd.
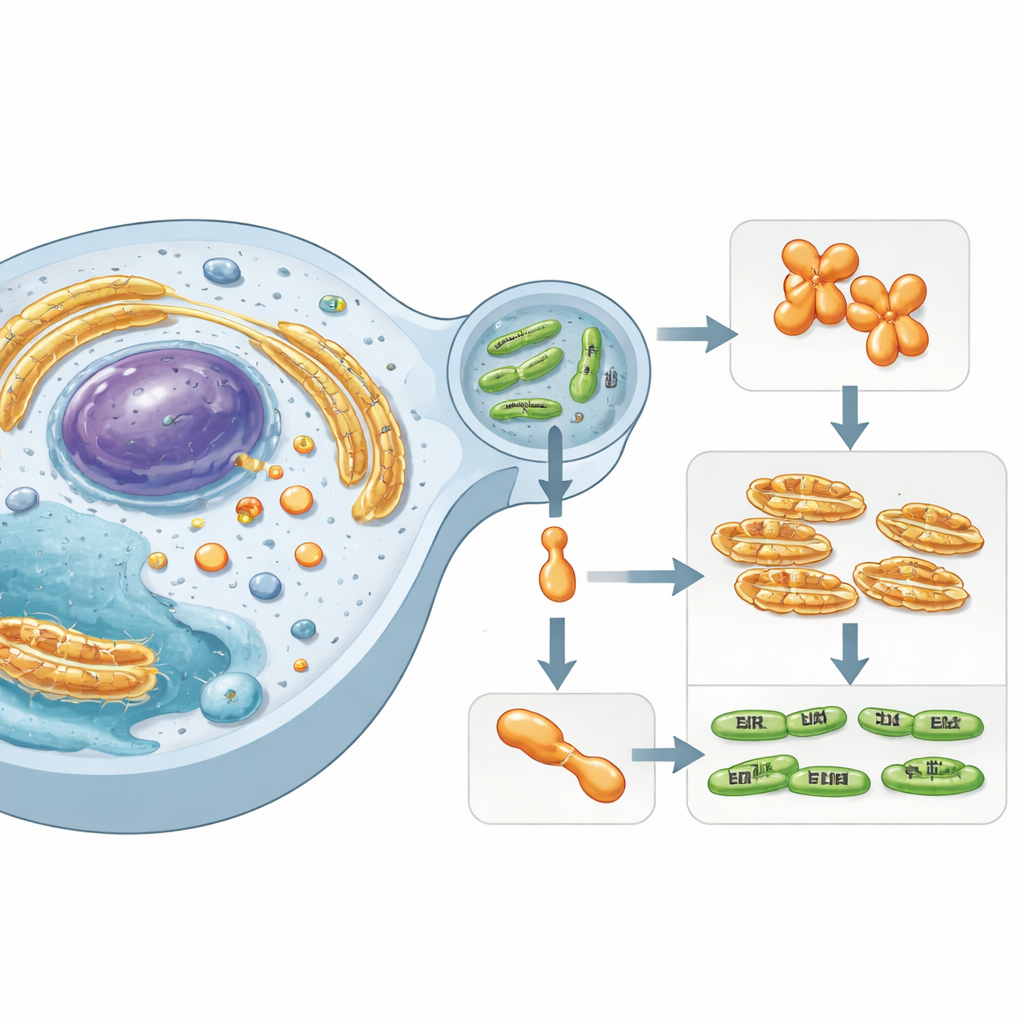
En dold aktör inne i mänskliga celler
Arbetet fokuserar på Simkania negevensis, en Chlamydia‑liknande bakterie kopplad till långvariga luftvägsinfektioner. Denna mikroorganism överlever inne i en membranomsluten bubbla i mänskliga celler och sprutar in specialiserade ”effektor”-proteiner i den omgivande cytoplasman. En av dessa effektorer, kallad SnCE1, tillhör en familj av enzymer som är kända för att störa värdcellens system för proteinetikettering. Dessa etiketter — små proteiner såsom ubiquitin och SUMO — fungerar som cellulära trafiksignaler och kontrollerar immunitet, stressrespons och celldöd. Genom att störa SUMO‑ och ubiquitinkedjor kan bakterier sabotera värdens försvar och skapa en mer gästvänlig nisch.
En tvåfunktioners molekylär strömbrytare
Forskarna visar att SnCE1 är en verklig mångsysslare. Å ena sidan är det en effektiv ”deSUMOylas”: det klyver SUMO‑kedjor till enheter mycket lättare än det klyver ubiquitinkedjor. Högupplösta kristallstrukturer avslöjar hur SnCE1 griper en SUMO‑molekyl i en ytficka och använder precist placerade laddade och hydrofoba regioner för att favorisera SUMO framför ubiquitin. Å andra sidan fungerar SnCE1 också som en auto‑acetyltransferas: det tar acetylgrupper från den cellulära bränslemolekylen acetyl‑CoA och fäster dem vid flera av sina egna lysinrester. Överraskande nog använder båda aktiviteterna samma katalytiska centrum, så enzymet måste välja mellan att klippa SUMO och att modifiera sig självt.
Formning, klustring och klyvning av effektorn
Acetylation visar sig omforma hur SnCE1 är sammansatt. När det är omodifierat tenderar en katalytiskt inaktiv version av proteinet att bilda tetramerer — kluster av fyra enheter. Strukturell analys visar att gränssnitten mellan subenheterna blockerar den plats där SUMO normalt skulle binda, vilket gör denna klustrade form olämplig för deSUMOylation. När specifika lysiner, framför allt en på position 231, är acetylade kan inte detta saltkraftsbaserade gränssnitt längre bildas, och SnCE1 förekommer som separata monomerer. Dessa enstaka enheter har en öppen SUMO‑bindande fåra och uppvisar stark deSUMOylasaktivitet. Viktigt är att acetylation på Lys231 verkar irreversibel för alla testade mänskliga och bakteriella deacetylaser, vilket låser SnCE1 i dess aktiva, monomera tillstånd när denna modifiering väl har inträffat.
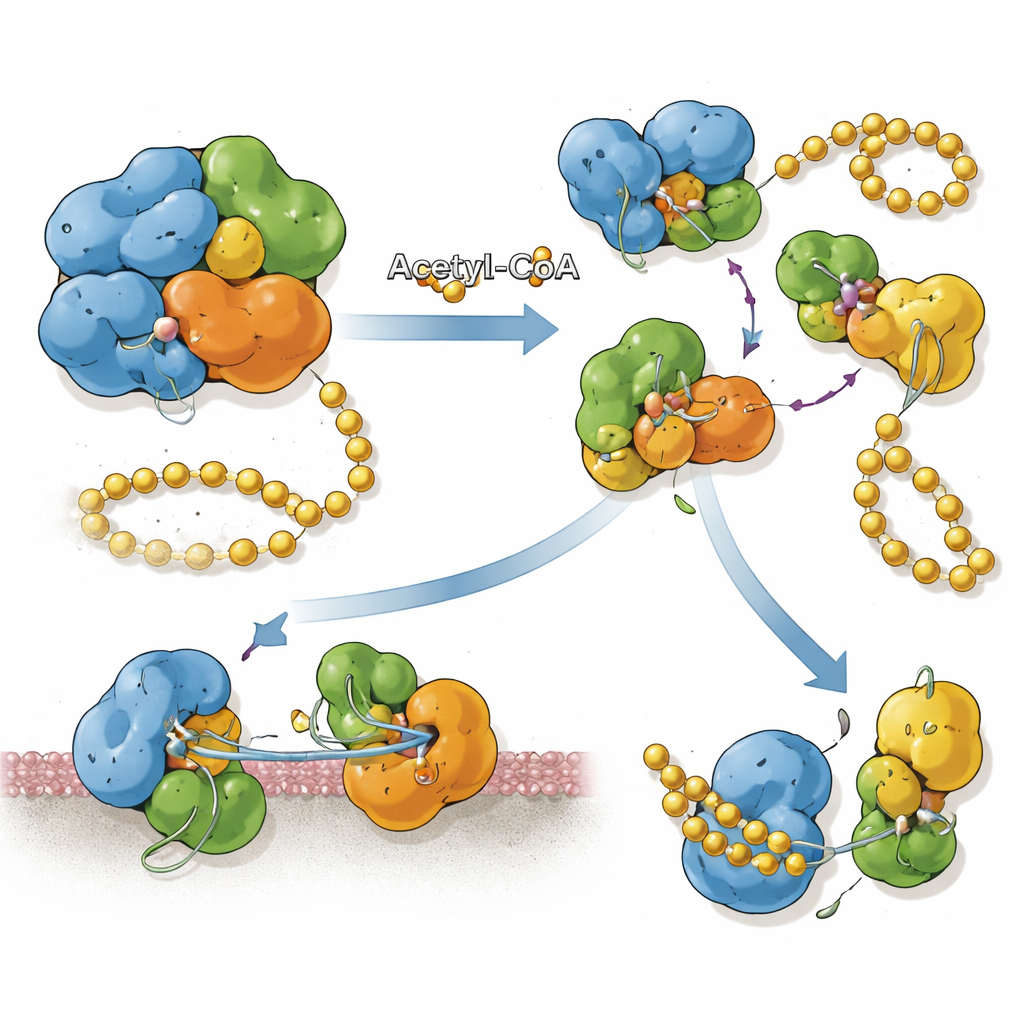
Koppla kemiska märken till proteinets position
SnCE1 produceras med ett N-terminalt segment som beter sig som ett membrankotare, vilket hjälper det att fästa vid membranet i den bakteriella vakuolen och vid intilliggande endoplasmatiska nätverket. Forskarna fann att när SnCE1 är kraftigt acetylat på flera lysiner i denna N‑terminala region förblir proteinet fullängds och membranbundet. När värdens enzymer, kallade sirtuiner, tar bort några av dessa acetylmärken genomgår SnCE1 en själv‑klyvningshändelse som trimmar av ungefär 10 kilodalton från dess N‑terminal, inklusive membrankotaren. Denna autoproteolytiska bearbetning frigör SnCE1 till den omgivande cytosolen och mot mitokondrierna. Site‑specifika acetylationsexperiment visar att ingen enskild lysin styr detta steg; istället bromsar eller förhindrar flera acetylade platser tillsammans klyvningen.
Påverkan på mitokondrier och värdmetabolism
Inne i mänskliga celler koncentreras fullängds‑SnCE1 vid det endoplasmatiska nätverket och vid kontaktpunkter med mitokondrier, där det sammanfaller med markanta förändringar i mitokondriernas form. Oavsett om det är katalytiskt aktivt eller inte främjar uttryck av SnCE1 fragmentering av det normalt tubulära mitokondriella nätverket, med starkast effekt i en icke‑acetylad, monomerisk mutant som lätt genomgår bearbetning. Eftersom mitokondriell dynamik är tätt kopplad till energiproduktion och cells överlevnad, påverkar denna omformning sannolikt hur gästvänlig cellen är för bakteriell tillväxt. Författarna föreslår att balansen mellan acetyl‑CoA och NAD+ i värdcellen — kemiska avläsningar av det metaboliska tillståndet — styr SnCE1‑acetylation, deacetylation och bearbetning, och därigenom finjusterar dess aktivitet och lokalisering i rum och tid.
Ett nytt kontrolllager i bakteriell virulens
I praktiska termer visar denna studie att Simkania använder acetylation som en dimmer på ett av sina nyckelvapen. När acetylgrupper är rikliga blir SnCE1 en stabil, aktiv monomer som effektivt suddar ut SUMO‑märken och hjälper bakterien att omkoppla värdens signalering samtidigt som den förblir membranbunden. När värdens deacetylaser aktiveras trimmas och frigörs SnCE1, omfördelas mot mitokondrier och omformar cellens inre landskap ytterligare. Genom att knyta virulens till små kemiska etiketter som speglar cellens metabolism kan bakterien justera hur aggressivt den manipulerar sin värd — en sofistikerad strategi som kan vara vanlig även bland andra intracellulära patogener.
Citering: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Nyckelord: reglering av bakteriell virulens, proteinacetylation, SUMO‑dekonjugering, värd–patogen‑interaktioner, mitokondriell dynamik