Clear Sky Science · it
Riprogrammazione della virulenza batterica tramite acetilazione della lisina
Come i batteri regolano il loro attacco
Molti batteri dannosi vivono all’interno delle nostre cellule e devono evitare di uccidere l’ospite troppo in fretta. Questo studio svela come uno di questi microbi modula la sua aggressività utilizzando un piccolo segnale chimico chiamato acetilazione. Decorando una proteina chiave della virulenza con questo segno, il batterio può cambiare la forma, la localizzazione e l’attività della proteina, regolando di fatto i suoi strumenti offensivi in base allo stato energetico della cellula ospite.
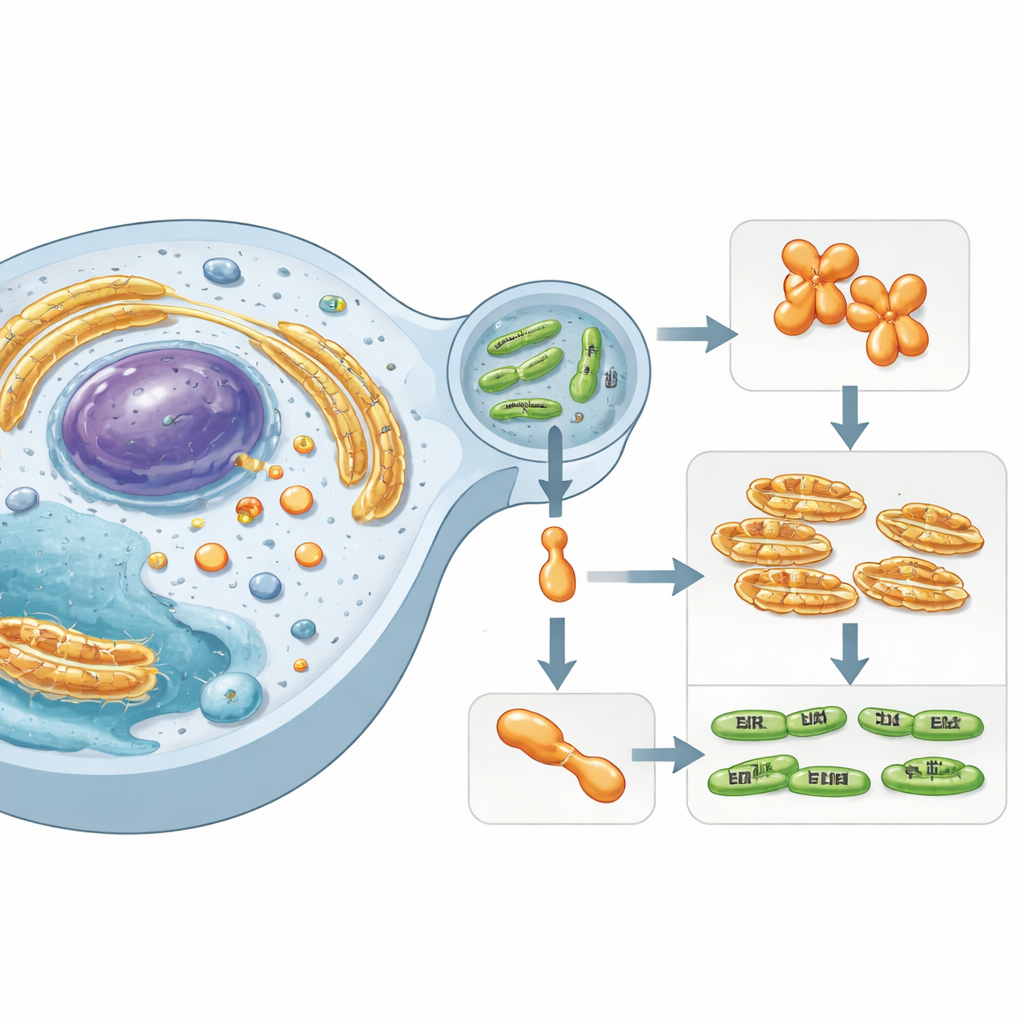
Un attore nascosto all’interno delle cellule umane
Il lavoro si concentra su Simkania negevensis, un batterio simile a Chlamydia associato a infezioni respiratorie di lunga durata. Questo microbo sopravvive all’interno di una bolla delimitata da membrana nelle cellule umane e inietta “effettori” specializzati nel citoplasma circostante. Uno di questi effettori, chiamato SnCE1, appartiene a una famiglia di enzimi noti per interferire con i sistemi di marcatura proteica dell’ospite. Queste etichette — piccole proteine come ubiquitina e SUMO — funzionano come segnali del traffico cellulare, controllando l’immunità, le risposte allo stress e la morte cellulare. Sconvolgere le catene di SUMO e ubiquitina permette ai batteri di sabotare le difese dell’ospite e creare un ambiente più favorevole per la loro sopravvivenza.
Un interruttore molecolare a doppia funzione
I ricercatori mostrano che SnCE1 è un vero e proprio multitasker. Da un lato è un efficiente “deSUMOilasi”: spezza le catene di SUMO in unità singole molto più facilmente di quanto non faccia con le catene di ubiquitina. Strutture cristallografiche ad alta risoluzione rivelano come SnCE1 afferra una molecola di SUMO in una tasca superficiale, usando regioni cariche e idrofobiche posizionate con precisione per favorire SUMO rispetto all’ubiquitina. Dall’altro lato, SnCE1 si comporta anche come un auto‑acetiltransferasi: prende gruppi acetile dalla molecola cellulare carburante acetil‑CoA e li attacca a diverse lisine proprie. Sorprendentemente, entrambe le attività utilizzano lo stesso centro catalitico, quindi l’enzima deve scegliere tra tagliare SUMO o modificare se stesso.
Forma, aggregazione e scissione dell’effettore
L’acetilazione risulta rimodellare l’assemblaggio di SnCE1. Quando non modificata, una versione cataliticamente inattiva della proteina tende a formare tetrameri — ammassi di quattro unità. L’analisi strutturale mostra che le interfacce tra le subunità bloccano il sito dove SUMO si legherebbe normalmente, rendendo questa forma aggregata poco adatta alla deSUMOilazione. Quando specifiche lisine, in particolare quella in posizione 231, sono acetilate, questa interfaccia basata su ponti salini non può più formarsi e SnCE1 esiste come monomeri separati. Queste unità singole presentano una gola di legame per SUMO aperta e mostrano forte attività deSUMOilasica. È importante notare che l’acetilazione della Lys231 sembra irreversibile nei confronti di tutti i deacetilasi umani e batterici testati, bloccando SnCE1 nello stato attivo e monomerico una volta che questa modifica si è verificata.
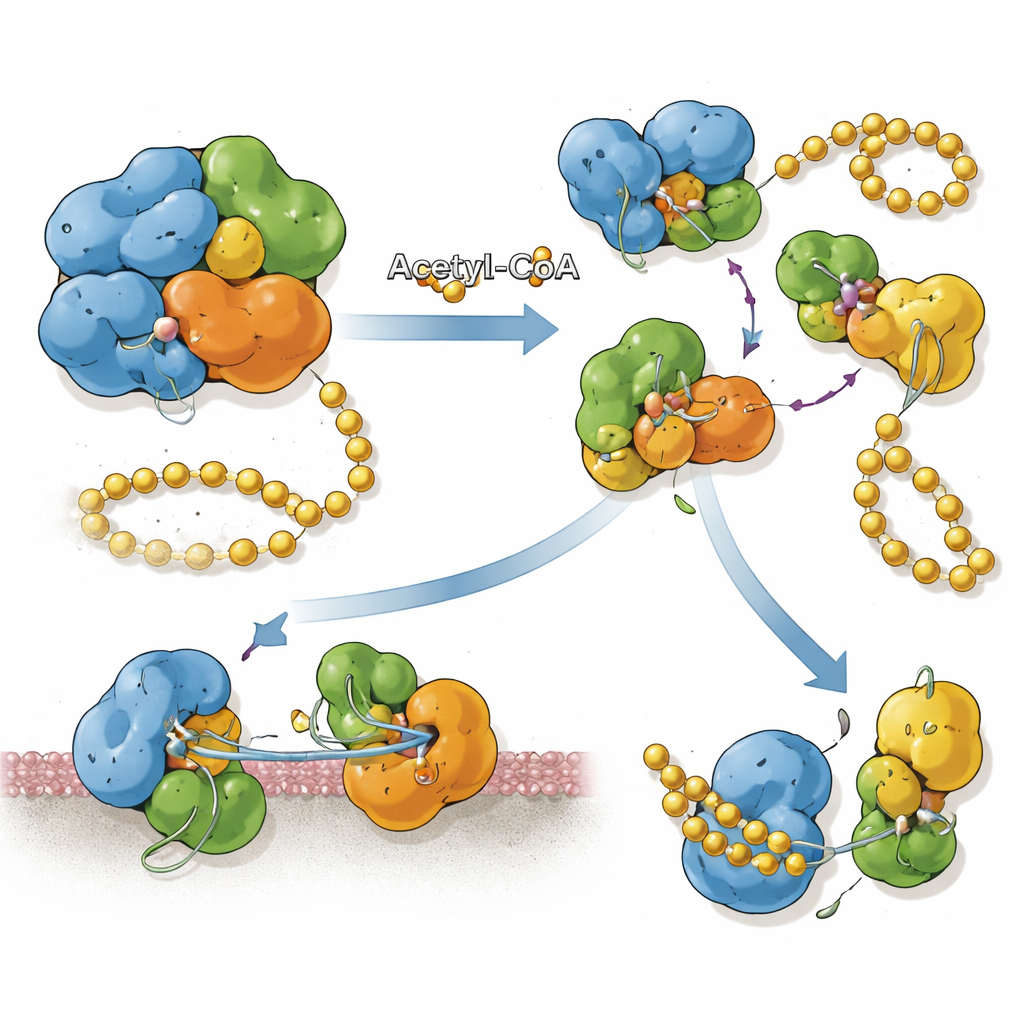
Collegare i segni chimici alla posizione della proteina
SnCE1 è prodotta con un segmento N‑terminale che si comporta come un ancora di membrana, aiutandola ad attaccarsi alla membrana della vacuola batterica e al reticolo endoplasmatico vicino. Il gruppo ha scoperto che quando SnCE1 è fortemente acetilata su diverse lisine in questa regione N‑terminal, la proteina rimane a lunghezza intera e legata alla membrana. Quando enzimi ospiti chiamati sirtuine rimuovono alcuni di questi segni acetilici, SnCE1 subisce un evento di autocleavage che taglia via all’incirca 10 kilodalton dal suo N‑termine, incluso l’ancora di membrana. Questo processamento autoproteolitico rilascia SnCE1 nel citosol circostante e la indirizza verso i mitocondri. Esperimenti di acetilazione sito‑specifica mostrano che nessuna singola lisina controlla questo passaggio; piuttosto, più siti acetilati collettivamente rallentano o impediscono il taglio.
Impatto sui mitocondri e sul metabolismo dell’ospite
All’interno delle cellule umane, SnCE1 a lunghezza intera si concentra nel reticolo endoplasmatico e nei punti di contatto con i mitocondri, dove coincide con marcati cambiamenti nella morfologia mitocondriale. Sia che sia cataliticamente attiva o meno, l’espressione di SnCE1 favorisce la frammentazione della rete mitocondriale normalmente tubulare, con l’effetto più pronunciato osservato in un mutante monomerico non acetilato che viene facilmente processato. Poiché la dinamica mitocondriale è strettamente legata alla produzione energetica e alla sopravvivenza cellulare, questo rimodellamento probabilmente influisce su quanto la cellula sia favorevole alla crescita batterica. Gli autori propongono che l’equilibrio tra acetil‑CoA e NAD+ nella cellula ospite — segnali chimici dello stato metabolico — governi l’acetilazione, la deacetilazione e il processamento di SnCE1, regolando così la sua attività e localizzazione nello spazio e nel tempo.
Un nuovo livello di controllo nella virulenza batterica
In termini pratici, questo studio mostra che Simkania usa l’acetilazione come un dimmer su una delle sue armi chiave. Quando i gruppi acetile sono abbondanti, SnCE1 diventa un monomero stabile e attivo che cancella efficacemente le etichette SUMO, aiutando il batterio a riorientare la segnalazione dell’ospite rimanendo attaccato alle membrane. Quando i deacetilasi dell’ospite sono attivi, SnCE1 viene tagliata e rilasciata, ridistribuendosi verso i mitocondri e rimodellando ulteriormente il panorama interno della cellula. Legando la virulenza a piccoli segni chimici che riflettono il metabolismo cellulare, il batterio può regolare quanto aggressivamente manipola il suo ospite, rivelando una strategia sofisticata che potrebbe essere condivisa da altri patogeni intracellulari.
Citazione: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Parole chiave: regolazione della virulenza batterica, acetilazione delle proteine, deconiugazione SUMO, interazioni ospite‑patogeno, dinamica mitocondriale