Clear Sky Science · tr
Lizinde asetilasyonla bakteriyel virülansın yeniden programlanması
Bakteriler Saldırıyı Nasıl Ayarlar
Birçok zararlı bakteri hücrelerimizin içinde yaşar ve konakçıyı çok çabuk öldürmekten kaçınmak zorundadır. Bu çalışma, bu tür mikroplardan birinin saldırganlığını küçük bir kimyasal işaret olan asetilasyonla nasıl ince ayar yaptığına ışık tutuyor. Anahtar bir virülans proteinini bu işaretle ‘‘süsleyerek’’, bakteri proteinin şekli, konumu ve aktivitesini değiştirerek hücresel enerji durumuna uygun biçimde saldırı araçlarını yükseltip alçaltabiliyor.
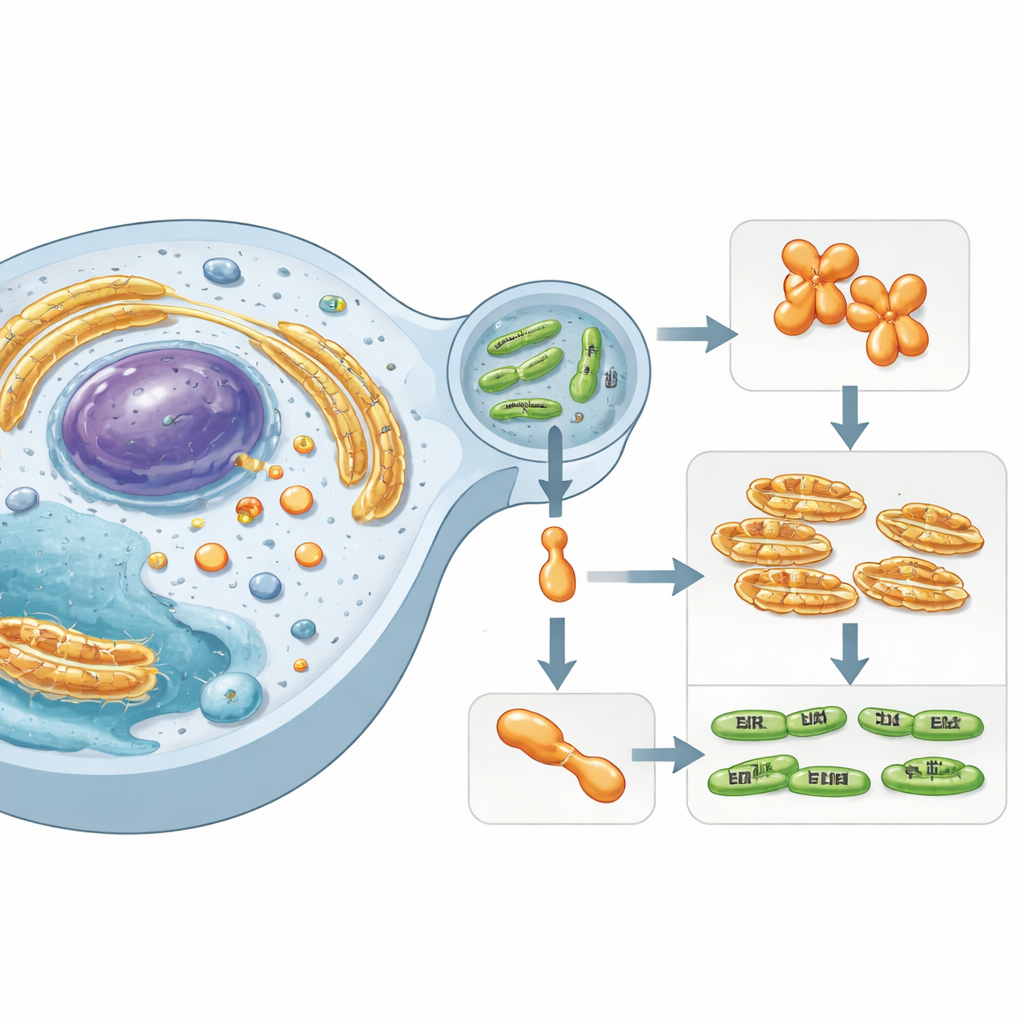
İnsan Hücreleri İçindeki Gizli Bir Aktör
Çalışma, uzun süreli solunum yolu enfeksiyonlarıyla ilişkilendirilen Chlamydia benzeri Simkania negevensis üzerinde yoğunlaşıyor. Bu mikroorganizma insan hücreleri içinde zarla çevrili bir kesecikte hayatta kalır ve çevreleyen sitoplazmaya özel “efektör” proteinleri enjekte eder. Bu efektörlerden biri olan SnCE1, konakçının protein etiketleme sistemlerini bozmasıyla bilinen enzim ailesine aittir. Bu etiketler—ubikitin ve SUMO gibi küçük proteinler—hücresel trafik sinalleri gibi davranır, bağışıklık, stres tepkileri ve hücre ölümü gibi süreçleri kontrol eder. SUMO ve ubikitin zincirlerini bozmak, bakterilerin konak savunmalarını sabote etmesine ve daha elverişli bir yaşam alanı oluşturmasına olanak tanır.
Çift İşlevli Moleküler Bir Anahtar
Araştırmacılar SnCE1’in gerçek bir çok görevli olduğunu gösteriyor. Bir yandan, etkili bir “deSUMOylaz”dır: SUMO zincirlerini tek tek birimlere kesmede, ubikitin zincirlerini kesmeye kıyasla çok daha hızlıdır. Yüksek çözünürlüklü kristal yapılar, SnCE1’in bir SUMO molekülünü bir yüzey ceplerinde nasıl kavradığını ve SUMO’yu ubikitine tercih eden doğru yerleşimli yüklü ve hidrofobik bölgeler kullandığını ortaya koyuyor. Öte yandan, SnCE1 aynı zamanda oto‑asetiltransferaz olarak da davranır: hücresel yakıt molekülü asetil‑CoA’dan asetil gruplarını alıp kendi lizin kalıntılarının birkaçına ekler. Şaşırtıcı biçimde her iki aktivite aynı katalitik merkez tarafından yürütüldüğünden, enzim SUMO’yu kesme ile kendini modifiye etme arasında bir seçim yapmak zorundadır.
Efektörün Şekillenmesi, Kümeleşmesi ve Kesilmesi
Asetilasyon, SnCE1’in bir araya geliş biçimini yeniden düzenliyor. Değişmemiş durumda, katalitik olarak inaktif bir versiyon proteinin dörtlüler—dört birimden oluşan kümeler—halinde toplanma eğilimindedir. Yapısal analizler, alt birimler arasındaki yüzeylerin SUMO’nun normalde bağlanacağı yeri kapattığını gösteriyor; bu nedenle kümeleşmiş biçim deSUMOylasyon için uygun değildir. Özellikle 231 konumundaki lizin olmak üzere belirli lizinlerin asetilasyonunda, bu tuz köprüsü temelli ara yüz artık oluşamaz ve SnCE1 ayrı monomerler halinde bulunur. Bu tek birimler açık bir SUMO‑bağlayıcı oluğa sahiptir ve güçlü deSUMOylaz aktivitesi gösterir. Önemli olarak, Lys231’deki asetilasyon insan ve bakteri deasetilazlarının test edildiği tüm koşullarda geri dönüşümsüz görünmüş; bu değişiklik oluştuğunda SnCE1’i aktif, monomerik durumda kilitliyor.
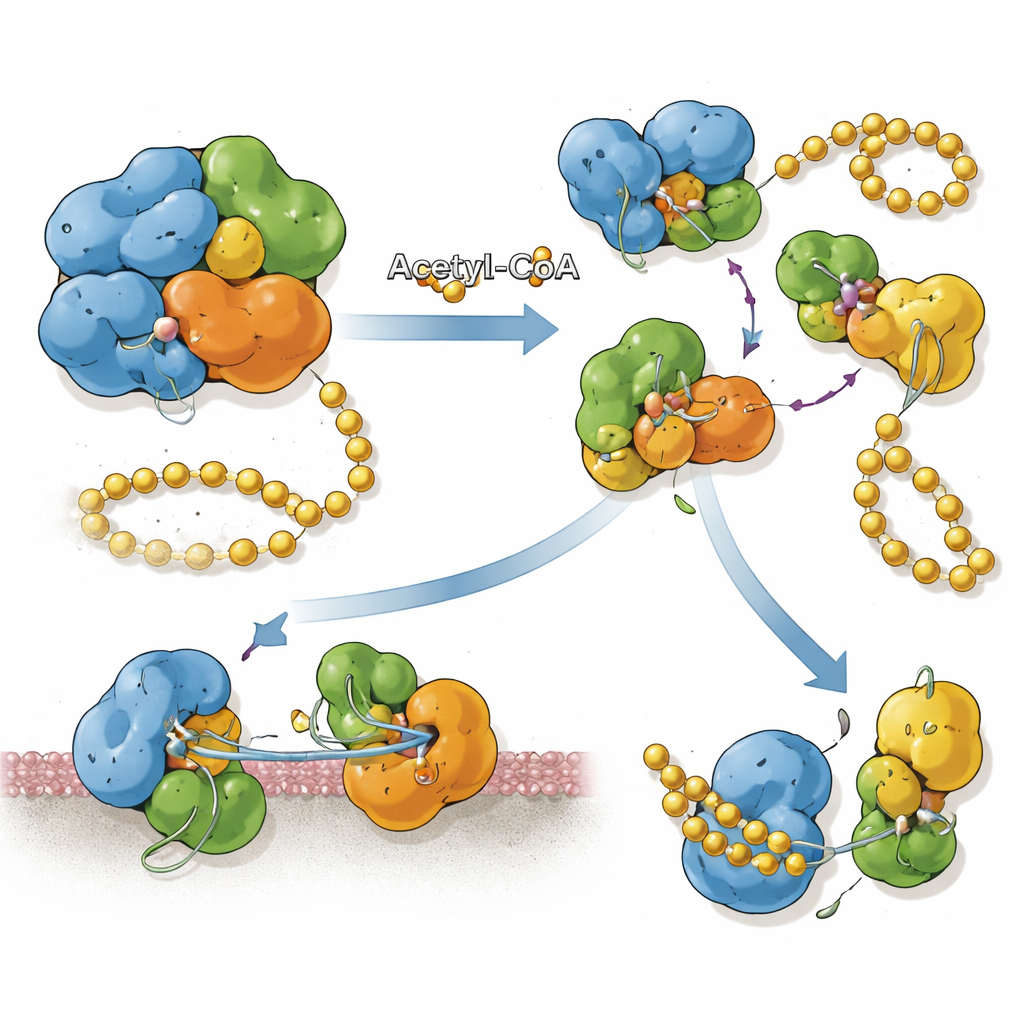
Kimyasal İşaretleri Protein Konumuna Bağlamak
SnCE1, bakteriyel vakuolün ve yakınındaki endoplazmik retikulumun zarına bağlanmasına yardımcı olan N‑terminal bir segmentle üretilir; bu bölüm bir membran çapa gibi davranır. Ekip, SnCE1’in N‑terminal bölgesindeki birkaç lizinde güçlü biçimde asetilendiğinde proteinin tam uzunlukta ve membrana bağlı kaldığını buldu. Konakçı enzimleri olan sirtuinler bazı bu asetil işaretlerini kaldırdığında, SnCE1 yaklaşık 10 kilodalton civarında bir N‑terminal parça kaybına yol açan bir oto‑yarmalanma geçirir; bu kesilme membran çapasını da içerir. Bu oto‑proteolitik işlem SnCE1’i çevreleyen sitozole ve mitokondrilere doğru serbest bırakır. Bölge‑özgü asetilasyon deneyleri bu adımı tek bir lizin kontrol etmediğini; bunun yerine birden çok asetillenmiş bölgenin birlikte kesilmeyi yavaşlattığını veya engellediğini gösteriyor.
Mitokondrilere ve Konak Metabolizmasına Etkisi
İnsan hücreleri içinde tam uzunluklu SnCE1 endoplazmik retikulumda ve mitokondrilerle temas noktalarında yoğunlaşır; burada mitokondriyal şekillerde çarpıcı değişikliklerle örtüşür. Katalitik olarak aktif olsun veya olmasın, SnCE1 ifadesi normalde tübüler olan mitokondri ağının parçalanmasını teşvik eder; en güçlü etki, kolayca işlenen, aşırı asetillenmemiş monomerik mutantta görülür. Mitokondriyal dinamikler enerji üretimi ve hücre hayatta kalmasıyla sıkı bağlantılı olduğundan bu yeniden şekillenme, hücrenin bakteriyel büyüme için ne kadar elverişli olduğunu etkiliyor olabilir. Yazarlar, konak hücresindeki asetil‑CoA ve NAD+ dengesi—metabolik durumu gösteren kimyasal değerler—in SnCE1 asetilasyonu, deasetilasyonu ve işlemeye hükmettiğini; böylece aktivitesini ve lokalizasyonunu zaman ve mekânda ayarladığını öne sürüyorlar.
Bakteriyel Virülansta Yeni Bir Kontrol Katmanı
Gündelik ifadeyle, bu çalışma Simkanianın asetilasyonu ana silahlarından birinde bir dimmer anahtarı olarak kullandığını gösteriyor. Asetil grupları bol olduğunda, SnCE1 istikrarlı, aktif bir monomer haline gelir ve SUMO işaretlerini verimli biçimde siler; bu durum bakterinin sinyallemeyi yeniden yapılandırmasına yardımcı olurken membrana bağlı kalmasını sağlar. Konak deasetilazları etkin olduğunda SnCE1 kesilir ve serbest bırakılır, mitokondrilere doğru yeniden dağılarak hücrenin iç manzarasını daha da yeniden şekillendirir. Virülansı hücresel metabolizmayı izleyen küçük kimyasal işaretlere bağlayarak bakteri, konakçıyı ne kadar agresifçe manipüle edeceğini ayarlayabiliyor; bu, diğer hücre içi patojenler tarafından da paylaşılabilecek ileri düzeyde bir stratejiyi açığa çıkarıyor.
Atıf: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Anahtar kelimeler: bakteriyel virülans düzenlemesi, protein asetilasyonu, SUMO dekonjugasyonu, konak–patojen etkileşimleri, mitokondriyal dinamikler