Clear Sky Science · pt
Reprogramação da virulência bacteriana por acetilação de lisina
Como as bactérias ajustam seu ataque
Muitas bactérias nocivas vivem dentro de nossas células e precisam evitar matar o hospedeiro rápido demais. Este estudo revela como um desses microrganismos ajusta sua agressividade usando uma pequena marca química chamada acetilação. Ao decorar uma proteína de virulência crucial com essa marca, a bactéria pode alternar a forma, a localização e a atividade da proteína, efetivamente regulando suas ferramentas ofensivas para combinar com o estado energético da célula hospedeira.
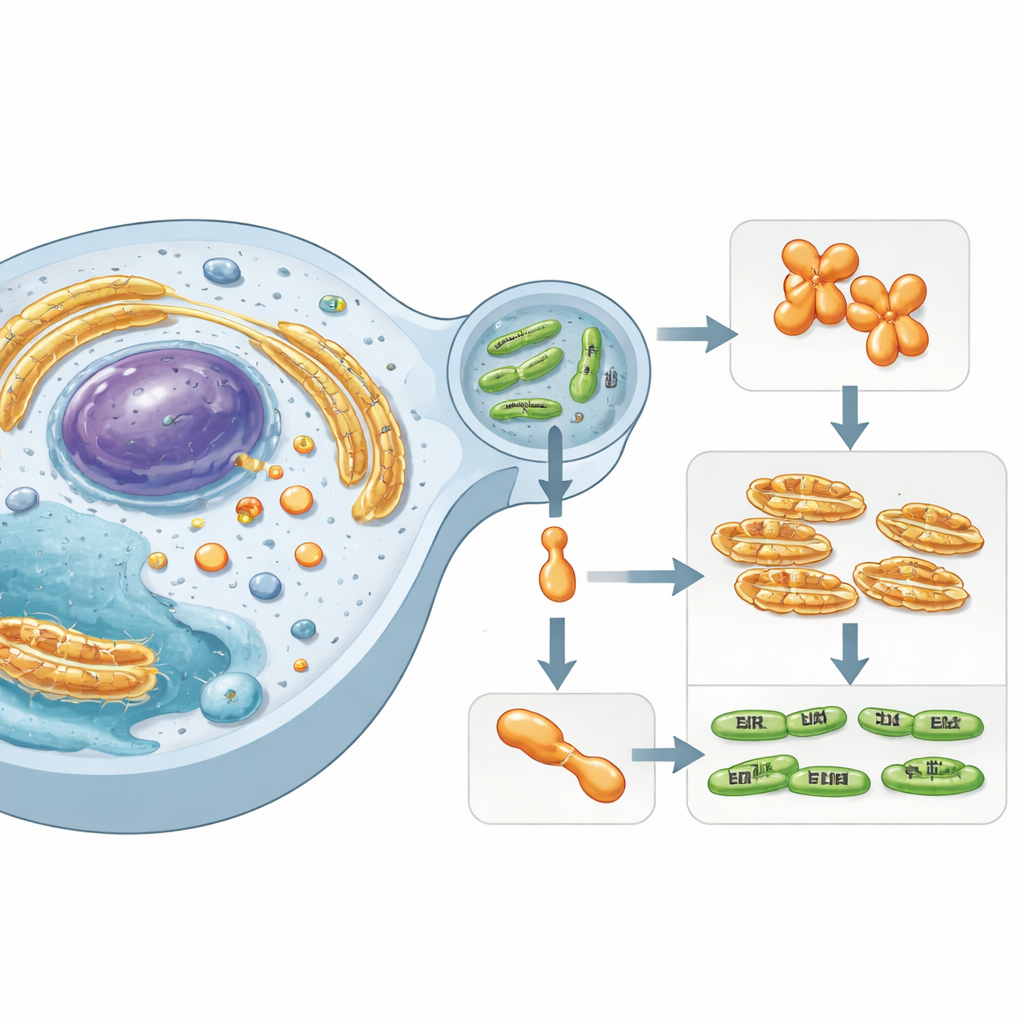
Um ator oculto dentro de células humanas
O trabalho foca em Simkania negevensis, uma bactéria semelhante à Chlamydia associada a infecções respiratórias persistentes. Esse microrganismo sobrevive dentro de uma bolha delimitada por membrana nas células humanas e injeta proteínas “efetoras” especializadas no citoplasma circundante. Uma dessas efetoras, chamada SnCE1, pertence a uma família de enzimas conhecidas por interferir nos sistemas de marcação de proteínas do hospedeiro. Essas marcas — pequenas proteínas como ubiquitina e SUMO — atuam como sinalizadores celulares, controlando imunidade, respostas ao estresse e morte celular. A interrupção de cadeias de SUMO e ubiquitina permite que as bactérias saboteiem as defesas do hospedeiro e criem um nicho mais favorável.
Um interruptor molecular com dupla função
Os pesquisadores mostram que SnCE1 é um verdadeiro multitarefas. Por um lado, é uma eficiente “deSUMOilase”: corta cadeias de SUMO em unidades individuais muito mais prontamente do que cliva cadeias de ubiquitina. Estruturas cristalinas de alta resolução revelam como SnCE1 acomoda uma molécula de SUMO em um bolso de superfície, usando regiões carregadas e hidrofóbicas precisamente posicionadas para favorecer SUMO em vez de ubiquitina. Por outro lado, SnCE1 também age como uma auto‑acetiltransferase: toma grupos acetil da molécula energética acetil‑CoA e os liga a vários de seus próprios resíduos de lisina. Surpreendentemente, ambas as atividades usam o mesmo centro catalítico, de modo que a enzima precisa escolher entre cortar SUMO e modificar a si própria.
Modelando, agrupando e clivando a efetora
A acetilação remodela a montagem de SnCE1. Quando não modificada, uma versão cataliticamente inativa da proteína tende a formar tetrâmeros — aglomerados de quatro unidades. Análises estruturais mostram que as interfaces entre subunidades bloqueiam o sítio onde SUMO normalmente se ligaria, tornando essa forma agrupada pouco adequada para a deSUMOilação. Quando lisinas específicas, especialmente a da posição 231, são acetiladas, essa interface baseada em pontes salinas não pode mais se formar, e SnCE1 passa a existir como monômeros separados. Essas unidades individuais têm um sulco de ligação a SUMO aberto e exibem forte atividade de deSUMOilase. Importante, a acetilação em Lis231 parece irreversível perante todas as desacetilases humanas e bacterianas testadas, bloqueando SnCE1 em seu estado ativo monomérico uma vez que essa modificação ocorre.
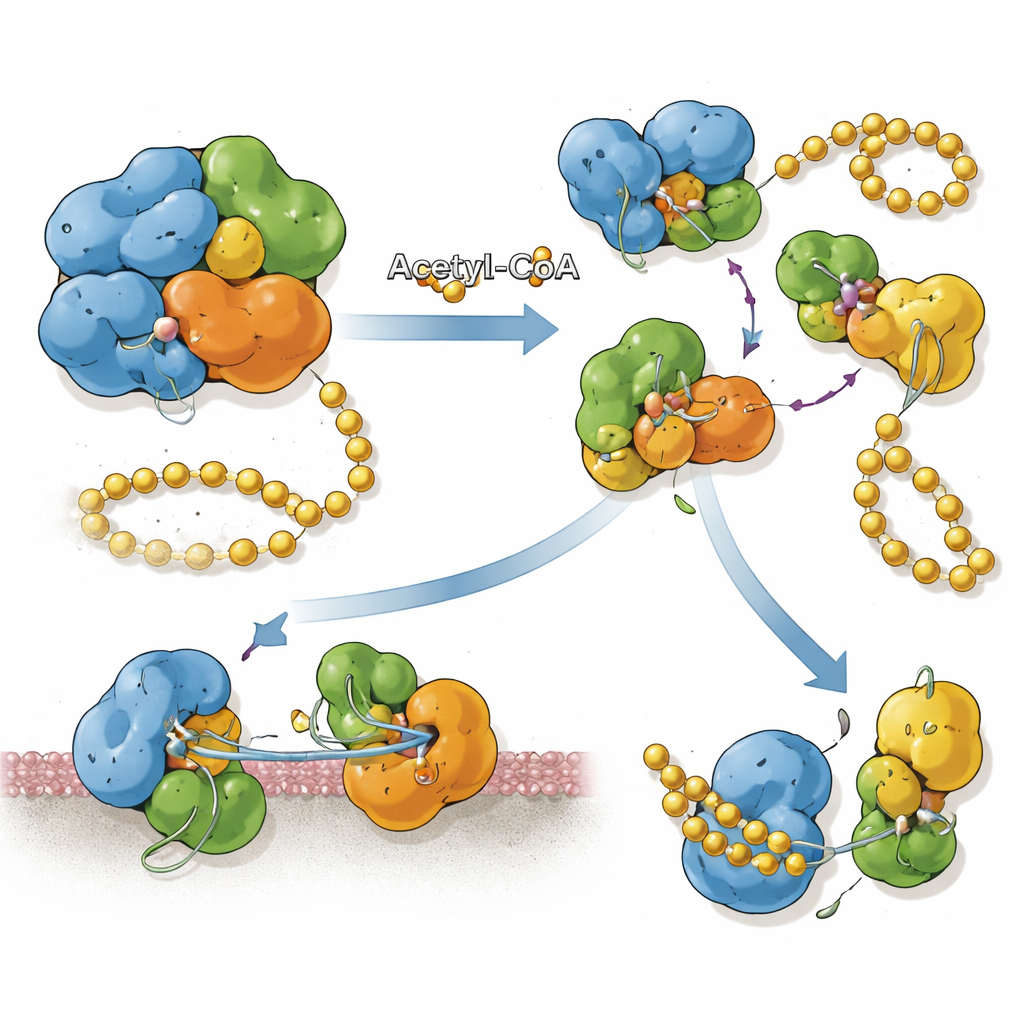
Ligando marcas químicas à posição da proteína
SnCE1 é produzida com um segmento N‑terminal que se comporta como uma âncora de membrana, ajudando-a a se ligar à membrana da vacúola bacteriana e ao retículo endoplasmático adjacente. A equipe descobriu que quando SnCE1 está fortemente acetilada em várias lisinas nessa região N‑terminal, a proteína permanece em comprimento total e ligada à membrana. Quando enzimas do hospedeiro chamadas sirtuínas removem algumas dessas marcas acetil, SnCE1 sofre um evento de autocleavage que remove cerca de 10 quilodaltons de sua extremidade N, incluindo a âncora de membrana. Esse processamento autoprotolítico libera SnCE1 para o citosol circundante e em direção às mitocôndrias. Experimentos de acetilação sítio‑específica mostram que nenhuma lisina isolada controla essa etapa; em vez disso, múltiplos sítios acetilados, coletivamente, retardam ou evitam a clivagem.
Impacto nas mitocôndrias e no metabolismo do hospedeiro
Dentro de células humanas, SnCE1 em comprimento total se concentra no retículo endoplasmático e nos pontos de contato com mitocôndrias, onde coincide com mudanças marcantes na forma mitocondrial. Quer esteja cataliticamente ativa ou não, a expressão de SnCE1 promove a fragmentação da rede mitocondrial normalmente tubular, com o efeito mais forte observado em um mutante monomérico não acetilado que é prontamente processado. Como a dinâmica mitocondrial está fortemente ligada à produção de energia e à sobrevivência celular, esse remodelamento provavelmente influencia o quão hospitaleira a célula é para o crescimento bacteriano. Os autores propõem que o equilíbrio entre acetil‑CoA e NAD+ na célula hospedeira — indicadores químicos do estado metabólico — governa a acetilação, desacetilação e o processamento de SnCE1, regulando assim sua atividade e localização no espaço e no tempo.
Uma nova camada de controle na virulência bacteriana
Em termos práticos, este estudo mostra que Simkania usa a acetilação como um dimmer em uma de suas armas-chave. Quando grupos acetil estão abundantes, SnCE1 torna‑se um monômero estável e ativo que apaga eficientemente marcas de SUMO, ajudando a bactéria a reconfigurar a sinalização do hospedeiro enquanto permanece ligada a membranas. Quando desacetilases do hospedeiro atuam, SnCE1 é aparada e liberada, redistribuindo‑se em direção às mitocôndrias e remodelando ainda mais a paisagem interna da célula. Ao ligar a virulência a pequenas marcas químicas que rastreiam o metabolismo celular, a bactéria pode ajustar o quão agressivamente manipula seu hospedeiro, revelando uma estratégia sofisticada que pode ser compartilhada por outros patógenos intracelulares.
Citação: Schmöker, O., Girbardt, B., Schulze, S. et al. Reprogramming of bacterial virulence by lysine acetylation. Nat Commun 17, 3859 (2026). https://doi.org/10.1038/s41467-026-72244-8
Palavras-chave: regulação da virulência bacteriana, acetilação de proteínas, deconjugação de SUMO, interações hospedeiro–patógeno, dinâmica mitocondrial