Clear Sky Science · zh
一种体外方法,用于模拟肿瘤相关MUC1与正常MUC1在高尔基O-糖基化上的分歧
为什么蛋白质上的糖衣在癌症中很重要
我们的细胞不断在蛋白质上装饰短糖链,形成一种分子“外衣”,影响细胞的生长、通讯以及与免疫系统的相互作用。在许多癌症中,这种糖衣以特征性方式发生改变,尤其是在一种称为MUC1的蛋白上,MUC1在上皮细胞和肿瘤表面大量存在。本研究构建了一个体外模型,模拟细胞如何添加这些糖基,使科学家能够详细观察正常MUC1的糖型如何分化为有助于癌症生长并逃避免疫识别的肿瘤相关形式。
构建可控的细胞“糖厂”模型
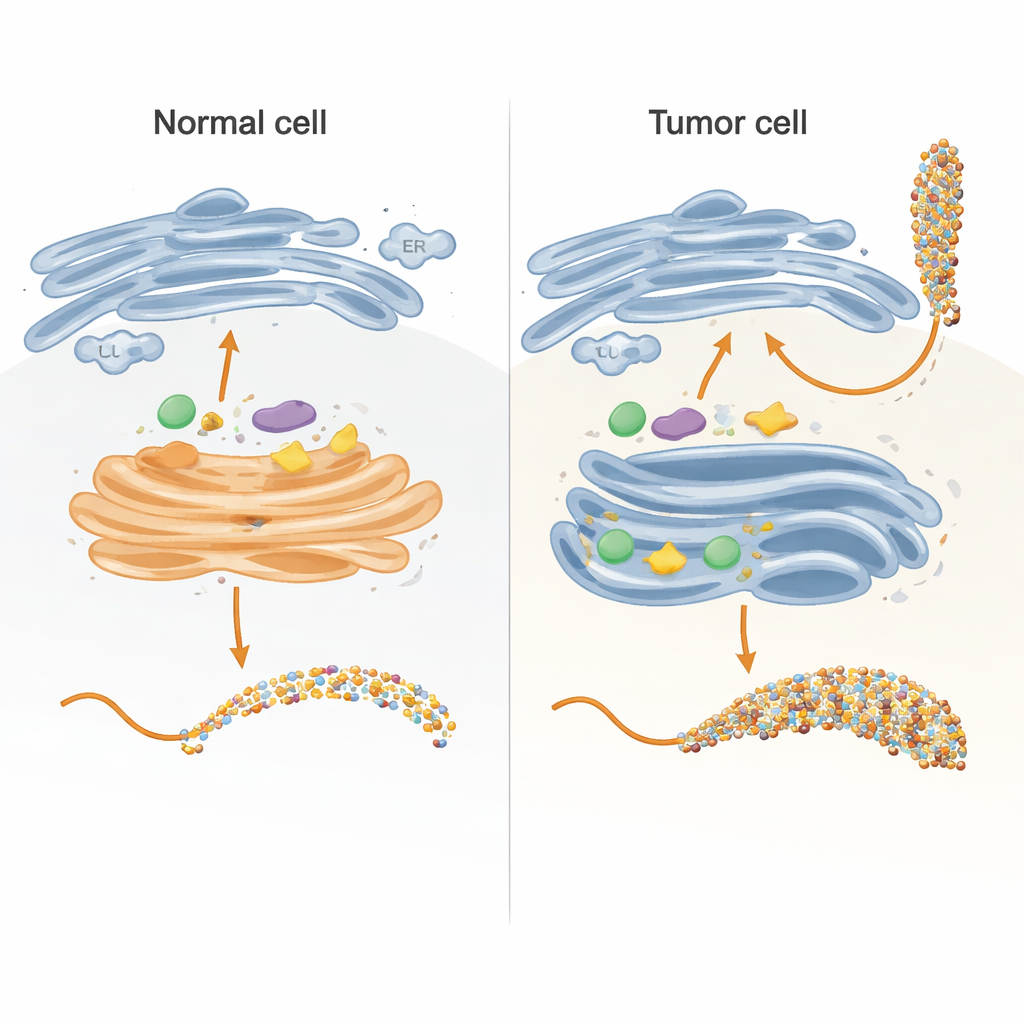
在细胞内,糖链主要在两个区室中被构建:内质网(ER)和高尔基体,它们像一个多步骤的装配线。作者在试管中重建了这条装配线的关键部分,使用一种经过精心设计的MUC1蛋白与载体标签的融合体。他们在细菌中表达该融合蛋白并纯化,然后将其暴露于通常在人体细胞内添加糖基的酶。通过设计MUC1片段,使其五个糖附着位点各自只出现一次且按天然序列排列,他们能够精确追踪每种酶修饰的具体位点及其顺序,并利用敏感的动力学测定和质谱分析进行监测。
正常与肿瘤途径如何分裂
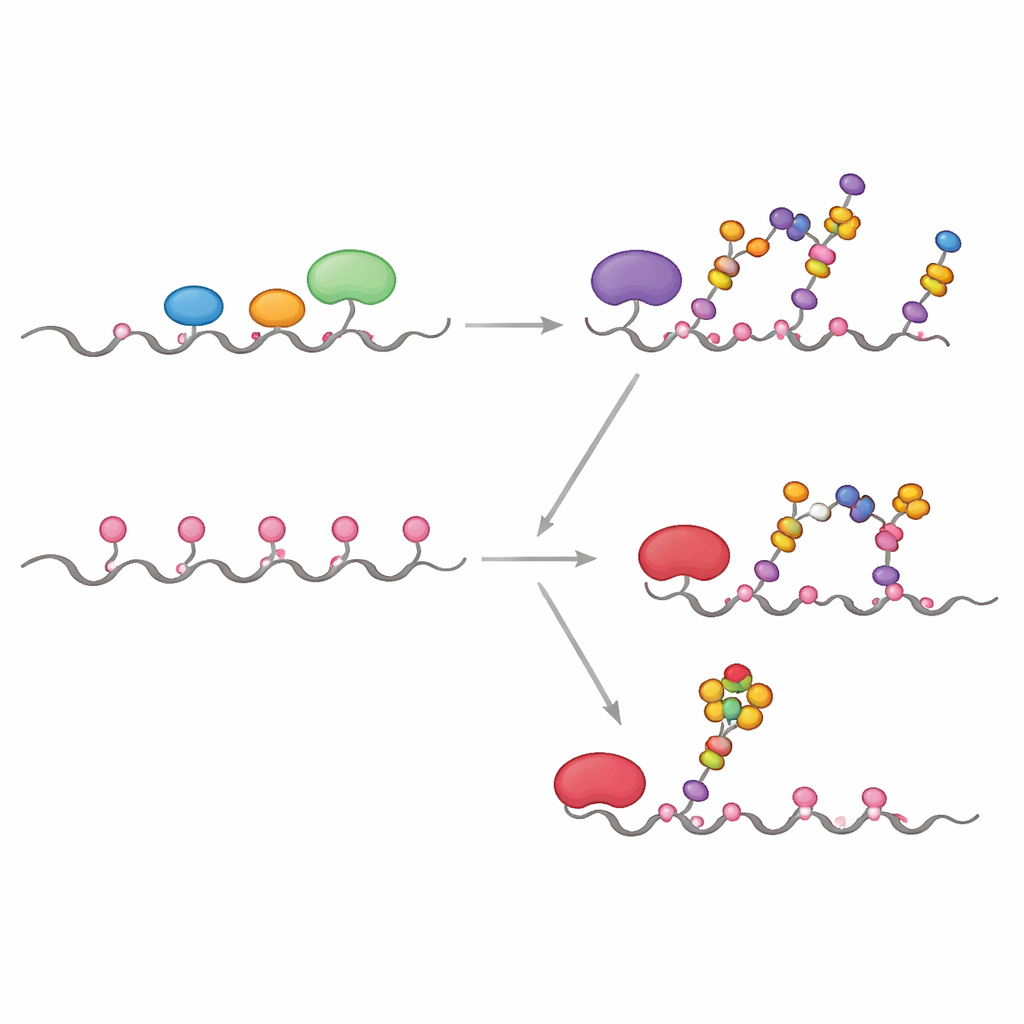
在健康细胞中,过程中的首批酶——称为GALNTs——主要位于高尔基体的早期部分,并与延伸或封端初始糖单元的其他酶并列工作。团队表明,在这些“共定位”的条件下,GALNTs主要修饰MUC1的一部分位点——作者称为直接位点——而两个较慢、依赖凝集素的位点则大多保持未被修饰。一旦在直接位点添加了第一个糖(GalNAc),下游酶如C1GALT1会迅速延伸它们,或ST6GALNAC1和其他唾液酸转移酶添加唾液酸,从而有效阻止GALNTs通过其凝集素机制密集填充剩余位点。结果是更为温和、受控的糖型,典型于正常上皮的MUC1。
模拟类似癌症的酶重排
许多肿瘤表现出GALNT酶从高尔基体逆向重新定位到内质网的显著改变,同时若干糖基化酶的量也发生变化。研究者通过先让GALNTs单独且更长时间地作用,然后再引入下游酶来模拟这种情况。在这些条件下,初始糖逐步从容易的直接位点扩散到较慢的凝集素依赖位点,最终占据MUC1的全部五个位点。只有在这种饱和步骤之后才加入延伸和封端酶。这种类ER情形产生了一种高度装饰的MUC1,类似肿瘤相关的MUC1,富含所谓的Tn和sialyl-Tn(sTn)抗原,而这些抗原已知与癌症进展、免疫逃逸和转移相关。
聚焦单个位点的热点
肿瘤MUC1最具临床重要性的特征之一是sialyl-Tn的存在——一种直接附着于GalNAc并被唾液酸封端的短糖。为准确确定其在MUC1上的出现位置,团队结合了动力学实验、分子对接和混合量子/经典模拟。他们发现酶ST6GALNAC1独自负责在MUC1的Tn和T抗原上以α2-6方式添加唾液酸,并且当所有五个位点都带有GalNAc时,该酶对PDTR区段的一个特定苏氨酸位点(论文中称为T13)表现出强烈偏好。结构模型和反应路径模拟表明,在该位点,糖和催化氨基酸以一种降低反应能垒的几何排列对齐,较邻近位点更有利,这解释了为何sTn首先且最显著地在该位点出现。
这对理解与靶向癌症意味着什么
这些实验与模拟共同表明,正常与肿瘤相关MUC1之间的差异,与其说是由到底存在哪些酶决定的,不如说更多取决于这些酶在细胞中的定位以及在被中断前它们能作用的时间。当GALNTs被限制在与竞争酶共处的高尔基体时,它们主要修饰快速位点,产生典型的core 1糖型并限制唾液酸化。而当它们像许多癌症中那样被重新定位到内质网时,它们有足够时间填充快位点和慢位点,形成高度被GalNAc覆盖的MUC1,这使其成为ST6GALNAC1在T13位点的特别良好底物,显著提高sTn水平。这个系统层面的视角将酶定位、反应时序和分子几何整合到一个框架中,有助于解释细胞“糖厂”中看似微小的变化如何产生强效的肿瘤特异性标志物,并为更精准的诊断、疫苗和以糖链为靶向的癌症疗法提供潜在靶点。
引用: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
关键词: 蛋白质糖基化, MUC1, 癌症生物标志物, 高尔基体, sialyl-Tn 抗原