Clear Sky Science · sv
En in vitro-metod för att simulera divergerande Golgi O-glykosylering av tumörassocierad MUC1 från normal MUC1
Varför sockerskikt på proteiner spelar roll vid cancer
Våra celler förser ständigt sina proteiner med korta sockerkedjor och bildar en slags molekylär ”kappa” som påverkar hur celler växer, kommunicerar och interagerar med immunförsvaret. I många cancerformer förändras denna sockertäckning på karakteristiska sätt, särskilt på ett protein som kallas MUC1 och som finns rikligt på epitelceller och tumörytor. Denna studie bygger en laboratoriemodell som efterliknar hur celler fäster dessa socker, vilket gör det möjligt för forskare att i detalj se hur normala sockerprofiler på MUC1 avviker till tumörassocierade former som hjälper tumörer att växa och undgå upptäckt.
Att bygga en kontrollerbar modell av cellens sockerfabrik
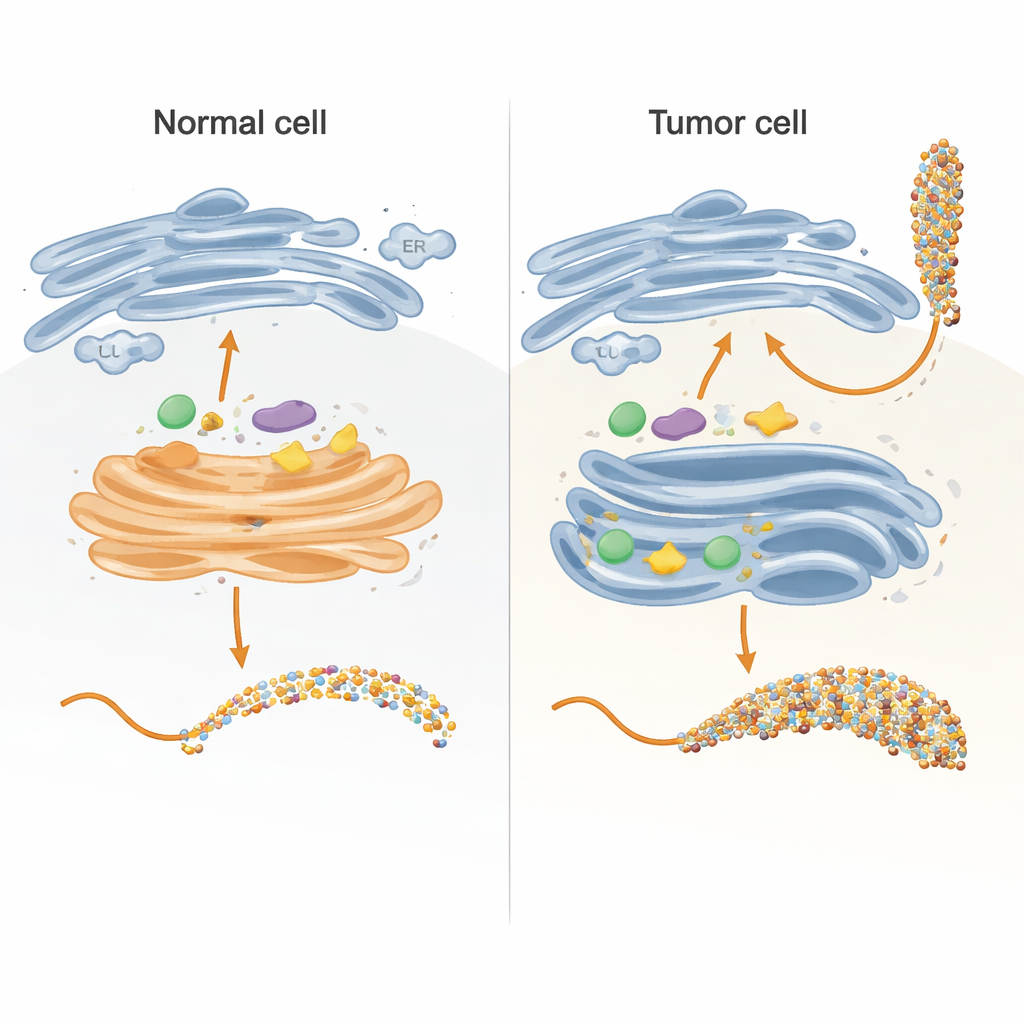
Inuti celler byggs sockerkedjor huvudsakligen i två kompartiment: det endoplasmatiska retikulumet (ER) och Golgiapparaten, som fungerar som en flerstegsmonteringslinje. Författarna återskapade nyckeldelar av denna linje i ett provrör genom att använda en noggrant konstruerad version av MUC1-proteinet fäst vid en bärare. De uttryckte denna fusionsprotein i bakterier, renade den och exponerade den sedan för mänskliga enzymer som normalt tillsätter socker inuti celler. Genom att designa MUC1-fragmentet så att var och en av dess fem sockerbindningsställen framträder endast en gång och i en naturlig sekvens kunde de spåra exakt vilket ställe varje enzym modifierade, och i vilken ordning, med känsliga kinetiska mätningar och masspektrometri.
Hur normala och tumörvägar skiljer sig åt
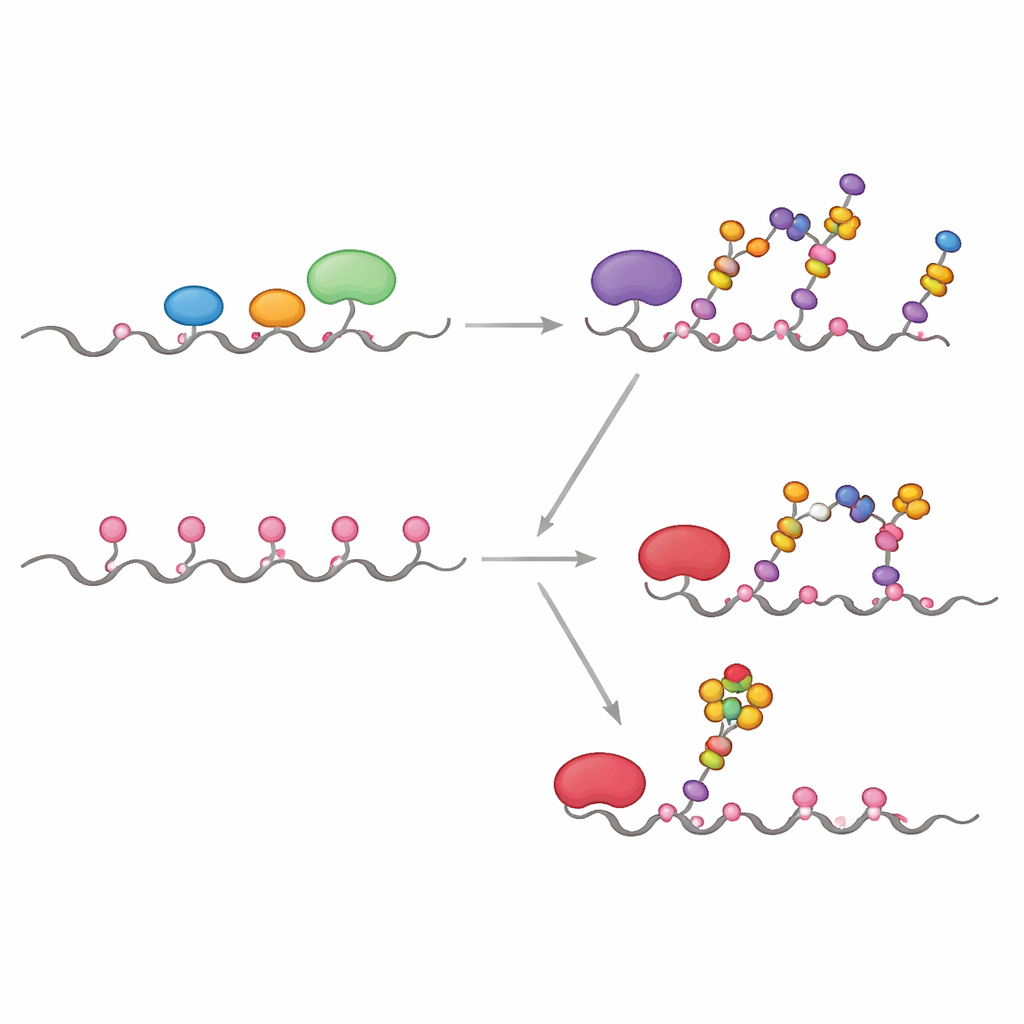
I friska celler finns de första enzymerna i processen, kallade GALNTs, främst i en tidig del av Golgi och arbetar sida vid sida med andra enzymer som förlänger eller kapslar de initiala sockerenheterna. Teamet visade att under dessa ”samexponerade” förhållanden modifierar GALNTs i första hand en undergrupp av ställen på MUC1 — vad författarna kallar direkta ställen — medan två långsammare, lektinberoende ställen förblir mestadels orörda. Så snart det första sockret (GalNAc) har lagts till på de direkta ställena förlänger nedströms enzymer som C1GALT1 dem snabbt, eller så lägger ST6GALNAC1 och andra sialyltransferaser till sialinsyra, vilket i praktiken hindrar GALNTs från att använda sin lektinbaserade mekanism för att täta alla återstående ställen. Resultatet blir ett mer måttfullt, kontrollerat sockermönster typiskt för normal epitelial MUC1.
Att simulera den cancerlika omfördelningen av enzymer
Många tumörer visar en tydlig förflyttning av GALNT-enzymer från Golgi tillbaka till ER, tillsammans med förändringar i nivåerna av flera glykosyleringsenzymer. Forskarna efterliknade detta genom att låta GALNTs verka först, isolerat, under längre tidsperioder innan de introducerade de nedströms enzymerna. Under dessa förhållanden spred sig de inledande sockren gradvis från de lättillgängliga direkta ställena till de långsammare lektinberoende ställena och ockuperade så småningom alla fem positioner på MUC1. Först efter denna mättnadsfas tillsattes förlängnings- och kapslingsenzym. Det här ER-liknande scenariot gav en kraftigt dekorerad MUC1 som liknar tumörassocierad MUC1, rik på så kallade Tn- och sialyl-Tn (sTn)-antigener som är kända för att korrelera med cancerprogression, immunundvikande och metastasering.
Fokusering på en enskild hetpunkt
En av de mest kliniskt viktiga egenskaperna hos tumör-MUC1 är närvaron av sialyl-Tn, en kort sockerstruktur kapslad av sialinsyra och fäst direkt på GalNAc. För att se exakt var detta uppträder på MUC1 kombinerade teamet kinetiska experiment, datorbaserad dockning och hybrida kvant-/klassiska simuleringar. De fann att enzymet ST6GALNAC1 entydigt ansvarar för att lägga till sialinsyra i en α2-6‑bindning till Tn- och T-antigener på MUC1, och att det uppvisar en stark preferens för en särskild treoninposition i PDTR‑regionen (kallad T13 i artikeln) när alla fem ställen bär GalNAc. Strukturella modeller och simulationsstudier av reaktionsvägen visar att vid detta ställe ligger sockret och katalytiska aminosyror i en geometri som sänker energibarriären för reaktionen mer än vid intilliggande ställen, vilket förklarar varför sTn uppträder där först och mest uttalat.
Vad detta betyder för förståelsen och målinriktad behandling av cancer
Tillsammans visar dessa experiment och simuleringar att skillnaden mellan normal och tumörassocierad MUC1 drivs mindre av vilka enzymer som finns närvarande och mer av var de är lokaliserade i cellen och hur länge de kan verka innan de avbryts. När GALNTs är begränsade till Golgi tillsammans med konkurrerande enzymer dekorerar de mestadels bara de snabba ställena, vilket ger upphov till typiska core‑1‑sockerstrukturer och begränsad sialylering. När de förflyttas till ER, som i många cancerformer, får de mer tid att fylla både snabba och långsamma ställen, vilket skapar en tätt GalNAc‑täckt MUC1 som blir ett särskilt bra substrat för ST6GALNAC1 vid T13‑stället, vilket kraftigt ökar sTn‑nivåerna. Detta systemnivåperspektiv kopplar samman enzymlokalisering, reaktionstid och molekylär geometri i en enhetlig ram som hjälper till att förklara hur en till synes subtil förändring i cellens sockerfabrik kan generera potenta tumörspecifika markörer och pekar mot mer precisa mål för diagnostik, vacciner och glykankoncentrerade cancerterapier.
Citering: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Nyckelord: proteinglykosylering, MUC1, cancermarkörer, Golgiapparaten, sialyl-Tn-antigen