Clear Sky Science · es
Un enfoque in vitro para simular la O-glicosilación divergente en el aparato de Golgi de la MUC1 asociada a tumores frente a la MUC1 normal
Por qué importan las “capas” de azúcar en las proteínas en el cáncer
Nuestras células decoran constantemente sus proteínas con pequeñas cadenas de azúcares, formando una especie de “abrigo” molecular que determina cómo crecen las células, se comunican e interactúan con el sistema inmunitario. En muchos cánceres, este recubrimiento azucarado cambia de formas distintivas, sobre todo en una proteína llamada MUC1, abundante en células epiteliales y en las superficies tumorales. Este estudio construye un modelo de laboratorio que imita cómo las células añaden estos azúcares, lo que permite a los científicos observar en detalle cómo los patrones normales de glicosilación de MUC1 divergen hacia formas asociadas a tumores que favorecen el crecimiento tumoral y la evasión inmunitaria.
Construyendo un modelo controlable de la “fábrica” de azúcares celular
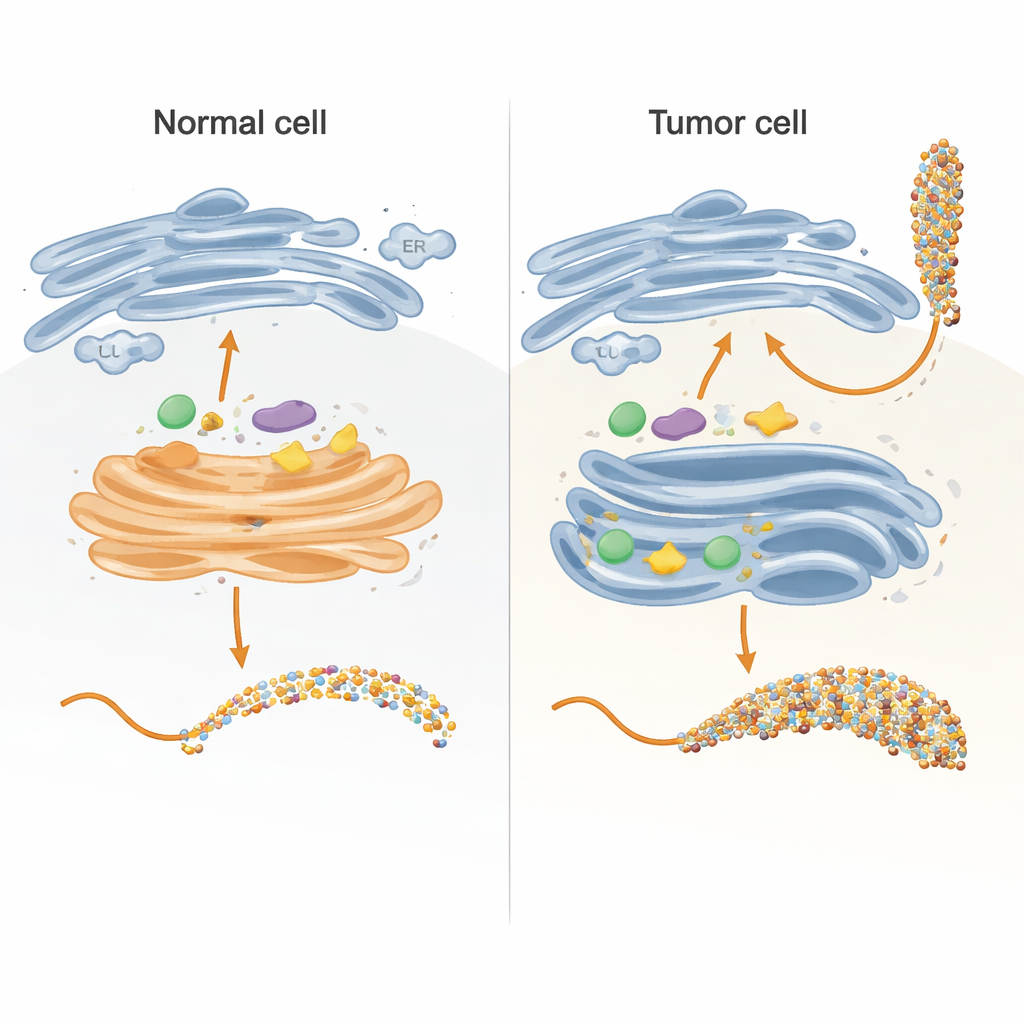
Dentro de las células, las cadenas de azúcar se construyen principalmente en dos compartimentos: el retículo endoplásmico (RE) y el aparato de Golgi, que actúan como una línea de ensamblaje de varios pasos. Los autores recrearon partes clave de esta línea en un tubo de ensayo usando una versión cuidadosamente diseñada de la proteína MUC1 unida a una etiqueta portadora. Expresaron esta proteína de fusión en bacterias, la purificaron y luego la expusieron a enzimas humanas que normalmente añaden azúcares dentro de las células. Al diseñar el fragmento de MUC1 de modo que cada uno de sus cinco sitios de anclaje de azúcar apareciera solo una vez y en la secuencia natural, pudieron rastrear exactamente qué sitio modificaba cada enzima y en qué orden, usando mediciones cinéticas sensibles y espectrometría de masas.
Cómo se separan las vías normal y tumoral
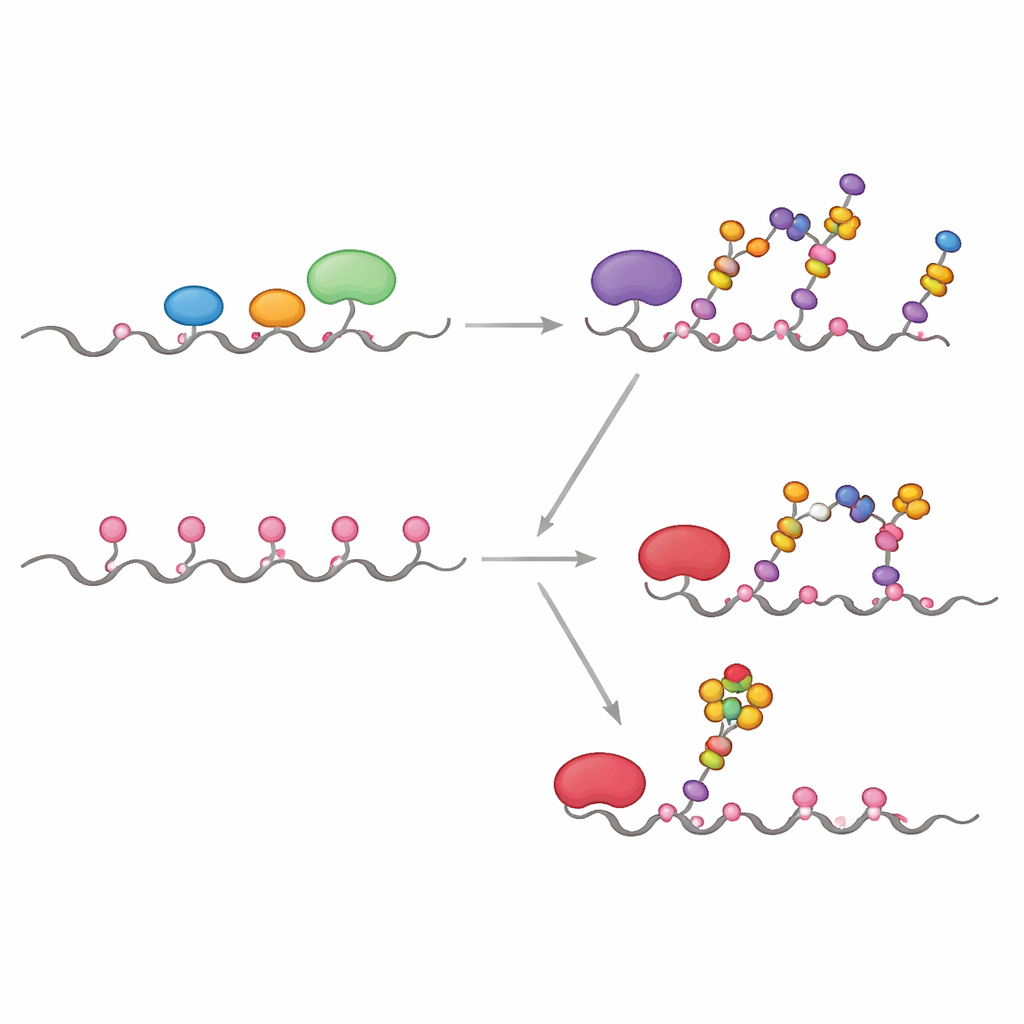
En células sanas, las primeras enzimas del proceso, llamadas GALNTs, residen principalmente en una región temprana del Golgi y actúan junto a otras enzimas que extienden o tapan las unidades de azúcar iniciales. El equipo mostró que bajo estas condiciones "colocalizadas", las GALNTs modifican sobre todo un subconjunto de sitios en MUC1—lo que los autores llaman sitios directos—mientras que dos sitios más lentos, dependientes de lectinas, permanecen mayormente sin tocar. En cuanto se añade la primera azúcar (GalNAc) en los sitios directos, enzimas posteriores como C1GALT1 las extienden rápidamente, o ST6GALNAC1 y otras sialiltransferasas añaden ácido siálico, bloqueando de forma efectiva el mecanismo dependiente de lectinas de las GALNTs para rellenar densamente los sitios restantes. El resultado es un patrón azucarado más moderado y controlado, típico de la MUC1 epitelial normal.
Simulando la reorganización tipo cáncer de las enzimas
Muchos tumores muestran una reubicación llamativa de las GALNTs desde el Golgi de regreso al RE, junto con cambios en los niveles de varias enzimas de glicosilación. Los investigadores imitaron esto permitiendo que las GALNTs actuasen primero, en aislamiento, durante períodos más largos antes de introducir las enzimas posteriores. Bajo estas condiciones, las azúcares iniciales se expandieron gradualmente desde los sitios directos fáciles hacia los sitios más lentos dependientes de lectinas, hasta ocupar las cinco posiciones en MUC1. Solo después de este paso de saturación se añadieron las enzimas de extensión y tapado. Este escenario similar al del RE dio lugar a una MUC1 fuertemente decorada parecida a la asociada a tumores, rica en los llamados antígenos Tn y sialil-Tn (sTn) que se asocian con progresión tumoral, evasión inmune y metástasis.
Focalizando un único punto caliente
Una de las características clínicamente más relevantes de la MUC1 tumoral es la presencia de sialil-Tn, un azúcar corto rematado por ácido siálico unido directamente al GalNAc. Para ver exactamente dónde aparece esto en MUC1, el equipo combinó experimentos cinéticos, acoplamiento por ordenador y simulaciones híbridas cuántico/clásicas. Encontraron que la enzima ST6GALNAC1 es la responsable exclusiva de añadir ácido siálico en una unión α2-6 a los antígenos Tn y T en MUC1, y que muestra una fuerte preferencia por una treonina concreta en la región PDTR (denominada T13 en el artículo) una vez que las cinco posiciones llevan GalNAc. Modelos estructurales y simulaciones del camino de reacción revelan que en este sitio el azúcar y los aminoácidos catalíticos se alinean en una geometría que reduce la barrera energética para la reacción más que en sitios vecinos, lo que explica por qué el sTn aparece allí primero y con mayor intensidad.
Qué implica esto para entender y atacar el cáncer
En conjunto, estos experimentos y simulaciones muestran que la diferencia entre la MUC1 normal y la asociada a tumores está menos determinada por qué enzimas están presentes y más por dónde se localizan en la célula y cuánto tiempo pueden actuar antes de ser interrumpidas. Cuando las GALNTs están confinadas en el Golgi junto a enzimas competidoras, decoran sobre todo los sitios rápidos, dando lugar a azúcares core 1 típicos y a una sialilación limitada. Cuando se reubican en el RE, como en muchos cánceres, disponen de tiempo para rellenar sitios rápidos y lentos, creando una MUC1 densamente cubierta de GalNAc que se convierte en un sustrato especialmente bueno para ST6GALNAC1 en el sitio T13, incrementando drásticamente los niveles de sTn. Esta visión a nivel de sistema vincula la localización enzimática, la sincronización de las reacciones y la geometría molecular en un único marco que ayuda a explicar cómo un cambio aparentemente sutil en la “fábrica” de azúcares celular puede generar marcadores tumorales potentes y sugiere objetivos más precisos para diagnósticos, vacunas y terapias oncológicas centradas en glicanos.
Cita: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Palabras clave: glicosilación de proteínas, MUC1, biomarcadores del cáncer, aparato de Golgi, antígeno sialil-Tn