Clear Sky Science · tr
Tümöre bağlı MUC1’in normal MUC1’den ayrışan Golgi O-glikozilasyonunu simüle etmeye yönelik in vitro bir yaklaşım
Proteinlerin üzerindeki şeker örtülerinin kanserde neden önemli olduğu
Hücrelerimiz proteinlerini küçük şeker zincirleriyle sürekli süsler; bu, hücrelerin büyümesini, iletişimini ve bağışıklık sistemiyle etkileşimini etkileyen bir tür moleküler “örtü” oluşturur. Birçok kanserde bu şeker kaplaması belirgin biçimde değişir; özellikle epitel hücrelerde ve tümör yüzeylerinde bol bulunan MUC1 adlı proteinde. Bu çalışma, hücrelerin bu şekerleri nasıl eklediğini taklit eden bir laboratuvar modeli kurarak, normalde MUC1’de görülen şeker desenlerinin kanserle ilişkili formlara nasıl ayrıştığını ayrıntılı biçimde görmeyi sağlıyor.
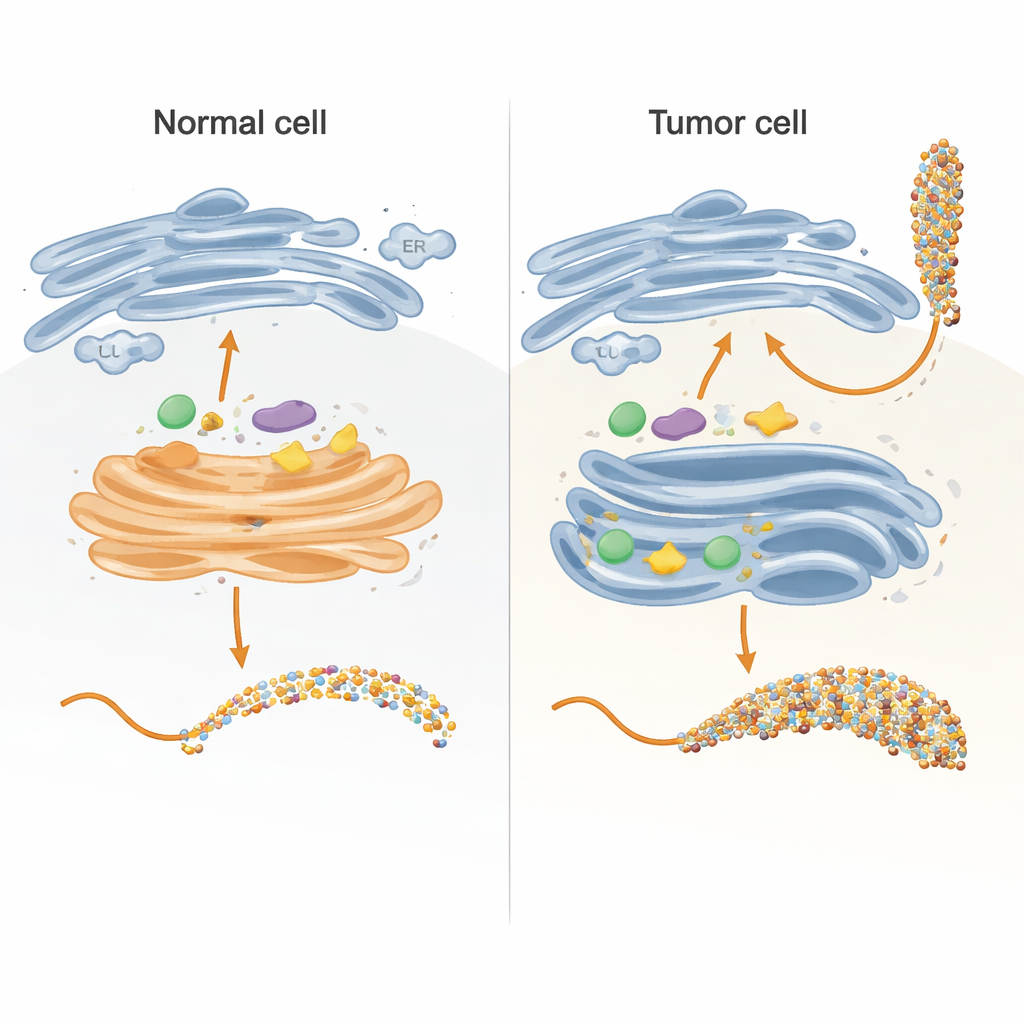
Hücrenin şeker fabrikasını denetlenebilir bir model olarak kurmak
Hücre içinde, şeker zincirleri esas olarak endoplazmik retikulum (ER) ve çok adımlı bir montaj hattı gibi davranan Golgi aygıtında inşa edilir. Yazarlar, bu hattın ana parçalarını test tüpünde, bir taşıyıcı etikete bağlı dikkatle tasarlanmış MUC1 versiyonunu kullanarak yeniden oluşturdular. Bu füzyon proteini bakterilerde ürettiler, saflaştırdılar ve sonra hücre içinde normalde şeker ekleyen insan enzimlerine maruz bıraktılar. MUC1 parçasını beş şeker bağlanma bölgesinin her birinin yalnızca bir kez ve doğal bir dizilimde görünmesini sağlayacak şekilde tasarlayarak, her enzimin hangi bölgeyi, hangi sırayla modifiye ettiğini hassas kinetik ölçümler ve kütle spektrometrisiyle tam olarak izleyebildiler.
Normal ve tümöre özgü yolların nasıl ayrıldığı
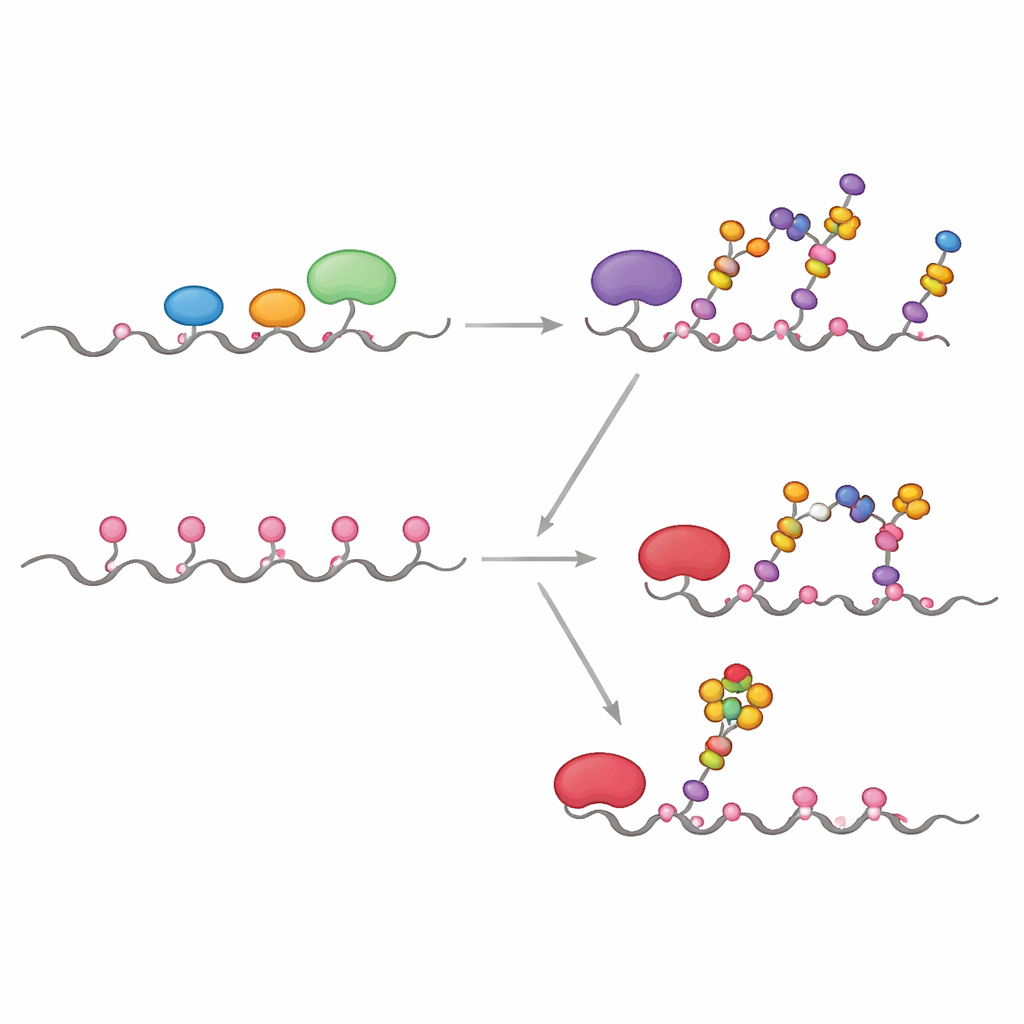
Sağlıklı hücrelerde sürecin ilk enzimleri olan GALNT’ler çoğunlukla Golgi’nin erken bir bölümünde bulunur ve ilk şeker birimlerini uzatan veya kapatan diğer enzimlerle yan yana çalışırlar. Ekip, bu “eş konumlu” koşullar altında GALNT’lerin öncelikle MUC1’in yazarların doğrudan bölgeler dediği bir alt kümesini modifiye ettiğini; iki daha yavaş, lektin-bağımlı bölgenin ise çoğunlukla dokunulmamış kaldığını gösterdi. Doğrudan bölgelere ilk şeker (GalNAc) eklenir eklenmez, C1GALT1 gibi aşağı akış enzimleri bunları hızla uzatıyor veya ST6GALNAC1 ve diğer sialiltransferazlar sialik asit ekleyerek GALNT’lerin lektin tabanlı mekanizmayla kalan tüm bölgeleri yoğun biçimde doldurmasını fiilen engelliyordu. Sonuç, normal epitel MUC1’e tipik olan daha ılımlı, kontrollü bir şeker düzeni oldu.
Kanser benzeri enzim yeniden dağılımını simüle etmek
Birçok tümörde GALNT enzimlerinin Golgi’den ER’ye belirgin bir yer değiştirmesi ve birkaç glikozilasyon enziminin düzeyinde değişiklikler gözlenir. Araştırmacılar bunu, GALNT’lerin aşağı akış enzimleri tanıştırılmadan önce daha uzun süre yalnız başına önce davranmasına izin vererek taklit ettiler. Bu koşullar altında, ilk şekerler zamanla kolay doğrudan bölgelerden daha yavaş lektin-bağımlı bölgelere yayılıp sonunda MUC1’deki beş pozisyonun tamamını işgal etti. Bu doygunluk adımından sonra uzatma ve kapama enzimleri eklendi. Bu ER-benzeri senaryo, Tn ve sialil-Tn (sTn) antijenleriyle zengin, tümöre bağlı MUC1’i andıran yoğun dekore edilmiş bir MUC1 verdi; bu antijenler kanser ilerlemesi, bağışıklıktan kaçış ve metastaz ile ilişkilendiriliyor.
Tek bir sıcak noktaya odaklanmak
Tümör MUC1’in klinik açıdan en önemli özelliklerinden biri, kısaca sialik-asit–kaplı şeker olan sialil-Tn’un doğrudan GalNAc’ye bağlı olarak bulunmasıdır. Bunun MUC1 üzerinde tam olarak nerede ortaya çıktığını görmek için ekip kinetik deneyleri, bilgisayar yerleştirmesi ve hibrit kuantum/klasik simülasyonları bir araya getirdi. ST6GALNAC1 enzimisinin MUC1 üzerindeki Tn ve T antijenlerine α2-6 bağlanmada sialik asit eklemekten eşsiz sorumlu olduğunu ve tüm beş bölge GalNAc taşıdığında PDTR bölgesindeki belirli bir treonin konumuna (makalede T13 olarak adlandırılıyor) güçlü bir tercih gösterdiğini buldular. Yapısal modeller ve reaksiyon-yolu simülasyonları, bu bölgede şeker ve katalitik aminoasitlerin komşu bölgelere göre reaksiyon için enerji bariyerini daha fazla düşürecek şekilde hizalandığını ortaya koyuyor; bu da sTn’un ilk ve en güçlü biçimde orada görülmesini açıklıyor.
Kanseri anlama ve hedefleme açısından önemi
Bu deneyler ve simülasyonlar birlikte gösteriyor ki normal ve tümöre bağlı MUC1 arasındaki fark, hangi enzimlerin mevcut olduğundan çok enzimlerin hücre içinde nerede bulunduğu ve müdahale edilmeden ne kadar süre faaliyet gösterebildiğiyle daha çok belirleniyor. GALNT’ler rekabet eden enzimlerle birlikte Golgi’de sınırlı kaldığında, çoğunlukla yalnızca hızlı bölgeleri süsleyerek tipik core 1 şekerleri ve sınırlı sialilasyon ortaya çıkar. Birçok kanserde olduğu gibi ER’ye taşındıklarında ise hem hızlı hem de yavaş bölgeleri dolduracak zamana kavuşarak yoğun GalNAc kaplı bir MUC1 oluşuyor; bu da T13 bölgesinde ST6GALNAC1 için özellikle iyi bir substrat oluşturarak sTn düzeylerini keskin biçimde artırıyor. Bu sistem düzeyindeki bakış açısı, enzim lokalizasyonu, reaksiyon zamanlaması ve moleküler geometrinin nasıl tek bir çerçevede birleştiğini göstererek hücrenin şeker fabrikasındaki görece ince bir değişikliğin güçlü tümöre özgü belirteçler üretebileceğini açıklıyor ve tanı, aşı ve glikan odaklı kanser tedavileri için daha hassas hedefler öneriyor.
Atıf: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Anahtar kelimeler: protein glikozilasyonu, MUC1, kanser biyobelirteçleri, Golgi aygıtı, sialil-Tn antijeni