Clear Sky Science · pt
Uma abordagem in vitro para simular a divergência da O-glicosilação Golgi de MUC1 associada a tumor a partir da MUC1 normal
Por que as coberturas de açúcar em proteínas importam no câncer
Nossas células constantemente decoram suas proteínas com pequenas cadeias de açúcares, formando uma espécie de “cobertura” molecular que afeta como as células crescem, se comunicam e interagem com o sistema imune. Em muitos cânceres, essa cobertura açucarada muda de maneiras distintas, especialmente em uma proteína chamada MUC1, abundante em células epiteliais e na superfície tumoral. Este estudo constrói um modelo de laboratório que reproduz como as células adicionam esses açúcares, permitindo aos cientistas observar em detalhe como os padrões normais de glicosilação de MUC1 divergem para formas associadas a tumor que ajudam os cânceres a crescer e a escapar da detecção.
Construindo um modelo controlável da “fábrica” de açúcares da célula
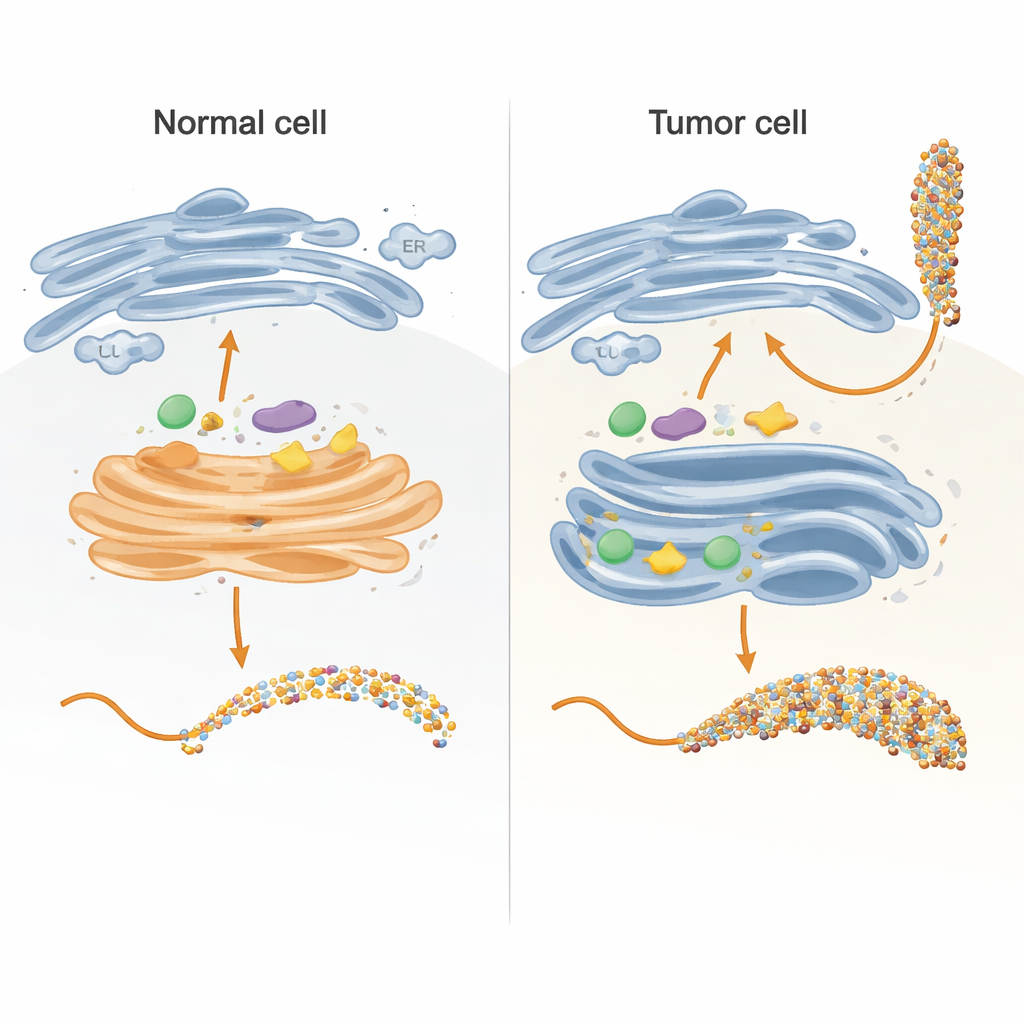
Dentro das células, as cadeias de açúcar são construídas principalmente em dois compartimentos: o retículo endoplasmático (RE) e o aparelho de Golgi, que atuam como uma linha de montagem em múltiplas etapas. Os autores recriaram partes-chave dessa linha em um tubo de ensaio usando uma versão cuidadosamente projetada da proteína MUC1 ligada a uma etiqueta transportadora. Eles expressaram essa proteína de fusão em bactérias, a purificaram e então a expuseram a enzimas humanas que normalmente adicionam açúcares dentro das células. Ao projetar o fragmento de MUC1 de modo que cada um de seus cinco sítios de ligação de açúcares apareça apenas uma vez e em uma sequência natural, puderam rastrear exatamente qual sítio cada enzima modificou, e em que ordem, usando medições cinéticas sensíveis e espectrometria de massa.
Como as vias normais e tumorais se separam
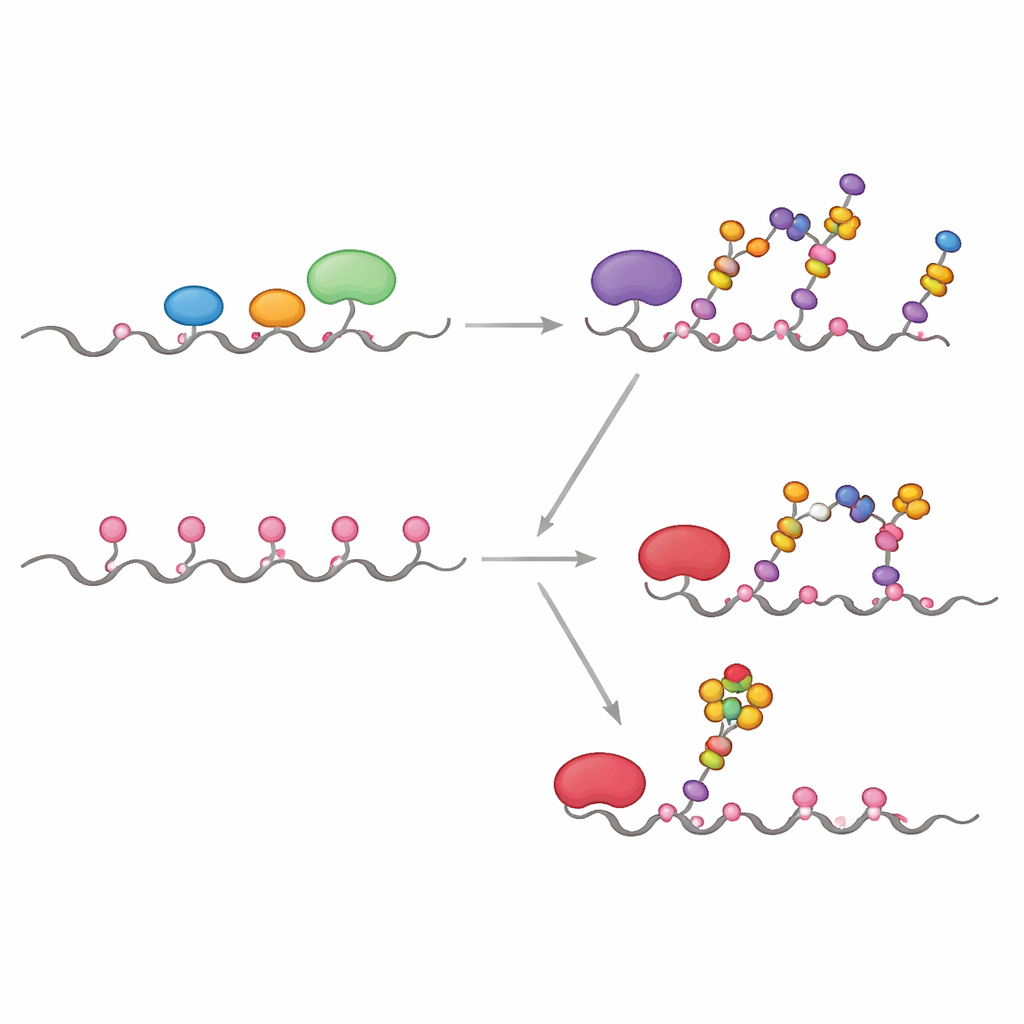
Em células saudáveis, as primeiras enzimas do processo, chamadas GALNTs, residem majoritariamente em uma parte inicial do Golgi e atuam lado a lado com outras enzimas que estendem ou inibem as unidades de açúcar iniciais. A equipe mostrou que, sob essas condições “co-localizadas”, as GALNTs modificam principalmente um subconjunto de sítios em MUC1 — o que os autores chamam de sítios diretos — enquanto dois sítios mais lentos, dependentes de lectinas, permanecem em grande parte intactos. Assim que o primeiro açúcar (GalNAc) é adicionado nos sítios diretos, enzimas a jusante como C1GALT1 rapidamente os estendem, ou ST6GALNAC1 e outras sialiltransferases adicionam ácido siálico, bloqueando efetivamente as GALNTs de usarem seu mecanismo baseado em lectina para preencher densamente os sítios restantes. O resultado é um padrão açucarado mais modesto e controlado, típico da MUC1 epitelial normal.
Simulando a reorganização enzimática semelhante à do câncer
Muitos tumores apresentam uma realocação marcante das enzimas GALNT do Golgi de volta ao RE, juntamente com mudanças nos níveis de várias enzimas de glicosilação. Os pesquisadores imitaram isso permitindo que as GALNTs atuassem primeiro, isoladamente, por períodos mais longos antes de introduzir as enzimas a jusante. Nessas condições, os açúcares iniciais gradualmente se espalharam dos sítios diretos fáceis para os sítios mais lentos dependentes de lectina, eventualmente ocupando todas as cinco posições em MUC1. Somente após essa etapa de saturação as enzimas de extensão e bloqueio foram adicionadas. Esse cenário semelhante ao do RE produziu uma MUC1 altamente decorada, assemelhando-se à MUC1 associada a tumor, rica nos chamados antígenos Tn e sialil-Tn (sTn) — conhecidos por se correlacionarem com progressão do câncer, evasão imune e metástase.
Focando em um único ponto crítico
Uma das características clinicamente mais importantes da MUC1 tumoral é a presença de sialil-Tn, um açúcar curto, bloqueado por ácido siálico e ligado diretamente ao GalNAc. Para ver exatamente onde isso aparece na MUC1, a equipe combinou experimentos cinéticos, docking computacional e simulações híbridas quânticas/clássicas. Eles descobriram que a enzima ST6GALNAC1 é exclusivamente responsável por adicionar ácido siálico em uma ligação α2-6 aos antígenos Tn e T em MUC1, e que ela mostra forte preferência por um sítio específico de treonina na região PDTR (chamado T13 no artigo) assim que os cinco sítios carregam GalNAc. Modelos estruturais e simulações do caminho de reação revelam que, nesse sítio, o açúcar e os aminoácidos catalíticos se alinham em uma geometria que reduz a barreira de energia para a reação mais do que nos sítios vizinhos, explicando por que o sTn aparece ali primeiro e com maior intensidade.
O que isso significa para entender e atacar o câncer
Em conjunto, esses experimentos e simulações mostram que a diferença entre MUC1 normal e MUC1 associada a tumor é guiada menos por quais enzimas estão presentes e mais por onde elas se localizam na célula e por quanto tempo podem agir antes de serem interrompidas. Quando as GALNTs estão confinadas ao Golgi com enzimas concorrentes, elas decoram majoritariamente apenas os sítios rápidos, dando origem a açúcares do core 1 típicos e sialilação limitada. Quando são realocadas para o RE, como em muitos cânceres, ganham tempo para preencher tanto os sítios rápidos quanto os lentos, criando uma MUC1 densamente coberta por GalNAc que se torna um substrato especialmente bom para a ST6GALNAC1 no sítio T13, elevando fortemente os níveis de sTn. Essa visão em nível de sistema conecta localização enzimática, tempo de reação e geometria molecular em um único quadro que ajuda a explicar como uma mudança aparentemente sutil na “fábrica” de açúcares da célula pode gerar marcadores tumorais potentes e sugere alvos mais precisos para diagnósticos, vacinas e terapias anti-câncer focadas em glicanos.
Citação: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Palavras-chave: glicosilação de proteínas, MUC1, biomarcadores do câncer, aparelho de Golgi, antígeno sialil-Tn