Clear Sky Science · ar
نهج مختبري لمحاكاة اختلاف O-جليكوزيلاسيون جولجي لبروتين MUC1 المرتبط بالأورام عن MUC1 الطبيعي
لماذا تهم الأغلفة السكرية على البروتينات في السرطان
تستمر خلايانا في تزيين بروتيناتها بسلاسل صغيرة من السكريات، مكوّنة نوعًا من "الغلاف" الجزيئي الذي يؤثر في كيفية نمو الخلايا وتواصلها وتفاعلها مع جهاز المناعة. في العديد من أنواع السرطان، يتغير هذا الغلاف السكري بطرق مميزة، لا سيما على بروتين يُدعى MUC1 الموجود بكثرة على الخلايا الطلائية وسطوح الأورام. تبني هذه الدراسة نموذجًا مختبريًا يحاكي كيفية إضافة الخلايا لهذه السكريات، مما يسمح للعلماء برؤية تفصيلية لكيفية تباعد أنماط السكر الطبيعية على MUC1 إلى أشكال مرتبطة بالأورام تساعد السرطانات على النمو والتملص من الكشف.
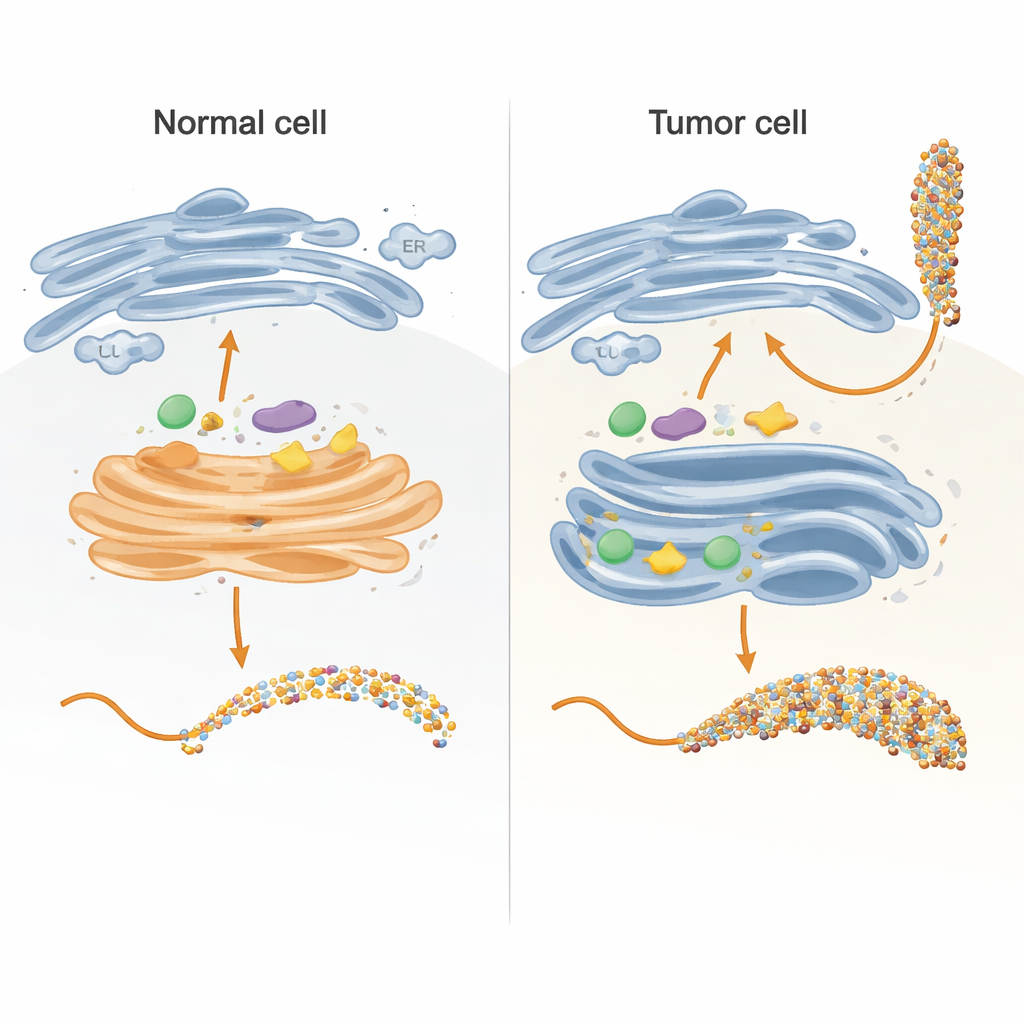
بناء نموذج قابل للتحكم لمصنع السكر داخل الخلية
داخل الخلايا، تُبنى سلاسل السكر بشكل رئيسي في مقطعين: الشبكة الإندوبلازمية وجهاز جولجي، اللذين يعملا كسلسلة تجميع متعددة المراحل. أعاد المؤلفون إنشاء أجزاء رئيسية من هذه السلسلة في أنبوب اختبار باستخدام نسخة معدلة بعناية من بروتين MUC1 مرتبطة بعلامة حاملة. عبروا عن هذا البروتين الموصول في بكتيريا، نظفوه، ثم عرّضوه لإنزيمات بشرية تضيف السكريات عادةً داخل الخلايا. من خلال تصميم قطعة MUC1 بحيث يظهر كل من مواقع ارتباط السكر الخمسة مرة واحدة فقط وفي تسلسل طبيعي، تمكنوا من تتبع بدقة أي موقع عدّله كل إنزيم، وبأي ترتيب، باستخدام قياسات حركية حساسة ومطيافة الكتلة.
كيف تنفصل المسارات الطبيعية ومسارات الورم
في الخلايا السليمة، تقع الإنزيمات الأولى في العملية، المسماة GALNTs، في معظمها في جزء مبكر من جهاز جولجي وتعمل جنبًا إلى جنب مع إنزيمات أخرى تقوم بتمديد أو تغطية وحدات السكر الأولية. أظهر الفريق أنه في ظل هذه الظروف "المترافقة المكان" تُعدّل GALNTs في المقام الأول مجموعة من المواقع على MUC1—ما يسميه المؤلفون المواقع المباشرة—بينما تبقى موقعان بطيئان معتمدان على الليكتين في الغالب غير معدّلين. بمجرد أن يُضاف السكر الأول (GalNAc) في المواقع المباشرة، تقوم الإنزيمات اللاحقة مثل C1GALT1 بسرعة بتمديدها، أو تضيف ST6GALNAC1 وإنزيمات سياتيليترانسفيراز أخرى حمض السياليك، مما يمنع فعليًا GALNTs من استخدام آليتها المعتمدة على الليكتين لملء جميع المواقع المتبقية بكثافة. النتيجة نمط سكري متواضع ومتحكم به نموذجي لـ MUC1 الطلائية الطبيعية.
محاكاة إعادة توزيع الإنزيمات شبيهة بالسرطان
تُظهر العديد من الأورام انتقالًا بارزًا لإنزيمات GALNT من جهاز جولجي إلى الشبكة الإندوبلازمية، إلى جانب تغييرات في مستويات عدة إنزيمات جليكوزيلية. قلّد الباحثون ذلك بالسماح لـ GALNTs بالعمل أولًا، بمعزل، لفترات أطول قبل إدخال الإنزيمات اللاحقة. في ظل هذه الظروف، تنتشر السكريات الأولية تدريجيًا من المواقع المباشرة السهلة إلى المواقع الأبطأ المعتمدة على الليكتين، وتحتل في النهاية جميع المواضع الخمسة على MUC1. لم تُضف إنزيمات التمديد والتغطية إلا بعد هذه خطوة التشبع. أسفرت هذه السيناريو المشابه للشبكة الإندوبلازمية عن MUC1 مزخرف بكثافة يشبه MUC1 المرتبط بالأورام، غنيًا بما يُسمى مستضدات Tn وsialyl-Tn (sTn) المعروفة بارتباطها بتقدم السرطان وتملصه من الجهاز المناعي والانبثاث.
التركيز على موقع ساخن واحد
أحد أهم السمات السريرية لـ MUC1 الورمي هو وجود sialyl-Tn، وهو سكر قصير مغطى بحمض السياليك مرتبط مباشرة بـ GalNAc. لرؤية المكان الدقيق لظهوره على MUC1، جمع الفريق تجارب حركية، ومحاكاة ربط حاسوبي، ومحاكاة هجينة كمية/كلاسيكية. وجدوا أن الإنزيم ST6GALNAC1 هو المسؤول بشكل فريد عن إضافة حمض السياليك بوصلة α2-6 إلى مستضدات Tn وT على MUC1، وأنه يظهر تفضيلًا قويًا لموقع ثريونين محدد في منطقة PDTR (المسمى T13 في الورقة) بمجرد أن تحمل المواقع الخمسة GalNAc كلها. تُظهر النماذج البنيوية ومحاكاة مسار التفاعل أن في هذا الموقع تتراصف السكريات والأحماض الأمينية الحفازة في هندسة تخفض حاجز الطاقة للتفاعل أكثر من المواقع المجاورة، ما يفسر سبب ظهور sTn هناك أولًا وبقوة أكبر.
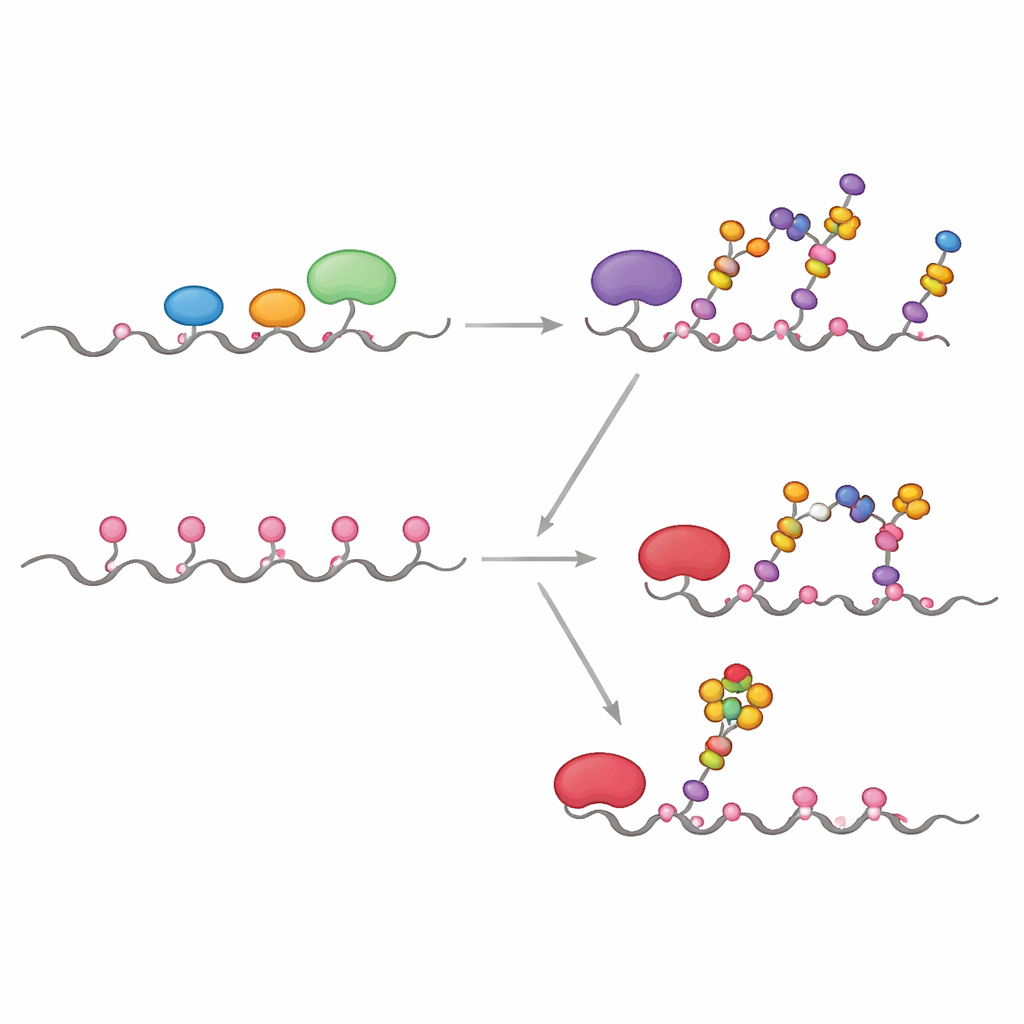
ماذا يعني هذا لفهم واستهداف السرطان
تُظهر هذه التجارب والمحاكاة مجتمعة أن الفرق بين MUC1 الطبيعي وMUC1 المرتبط بالأورام لا يُدفع بالدرجة الأولى بماهية الإنزيمات الموجودة بقدر ما يُحدَّد بمكان تموضعها داخل الخلية ومدة عملها قبل أن تُقاطع. عندما تُحصر GALNTs في جولجي مع إنزيمات متنافسة، فإنها تزيّن في الغالب المواقع السريعة فقط، مما يؤدي إلى سلاسل قالب 1 نموذجية وسيلاتية محدودة. عندما تُنقل إلى الشبكة الإندوبلازمية، كما في العديد من السرطانات، تحصل على وقت لملء المواقع السريعة والبطيئة على حد سواء، مكونة MUC1 مغطى بكثافة بـ GalNAc يصبح ركيزة جيدة جدًا لـ ST6GALNAC1 عند موقع T13، مما يزيد مستويات sTn بشكل حاد. يربط هذا المنظور على مستوى النظام موضع الإنزيم، وتوقيت التفاعل، والهندسة الجزيئية في إطار واحد يساعد على تفسير كيف يمكن لتغيير يبدو طفيفًا في "مصنع السكر" داخل الخلية أن يولد علامات ورمية قوية ويشير إلى أهداف أكثر دقة للتشخيصات واللقاحات والعلاجات المناهضة للسرطان المركزة على الغليكانات.
الاستشهاد: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
الكلمات المفتاحية: جليكوزيلية البروتين, MUC1, مؤشرات حيوية للسرطان, جهاز جولجي, مستضد سياتيلي-Tn