Clear Sky Science · he
שיטה חוץ-תאית המדמה O-גליקוזילציה מתפצלת של MUC1 הקשורה בגידול לעומת MUC1 נורמאלית
מדוע שכבות הסוכר על חלבונים חשובות בסרטן
תאים מקשטים בעקביות את חלבוניהם בשרשראות קצרות של סוכרים, ויוצרים מעין "מעיל" מולקולרי שמשפיע על גדילה, תקשורת ותיפקוד המערכת החיסונית. ברבים ממקרי הסרטן, ציפוי הסוכר משתנה באופן אופייני, במיוחד על חלבון בשם MUC1 השופע בתאים אפיתליאליים ועל פני גידולים. המחקר הזה בונה מודל מעבדה המדמה כיצד תאים מוסיפים סוכרים אלה, ומאפשר למדענים לראות בפרוטרוט כיצד דפוסי הסוכר הרגילים ב‑MUC1 מתפצלים לצורות הקשורות לגידול, שמסייעות להתפתחות הגידול ולהתחמקות מזיהוי.
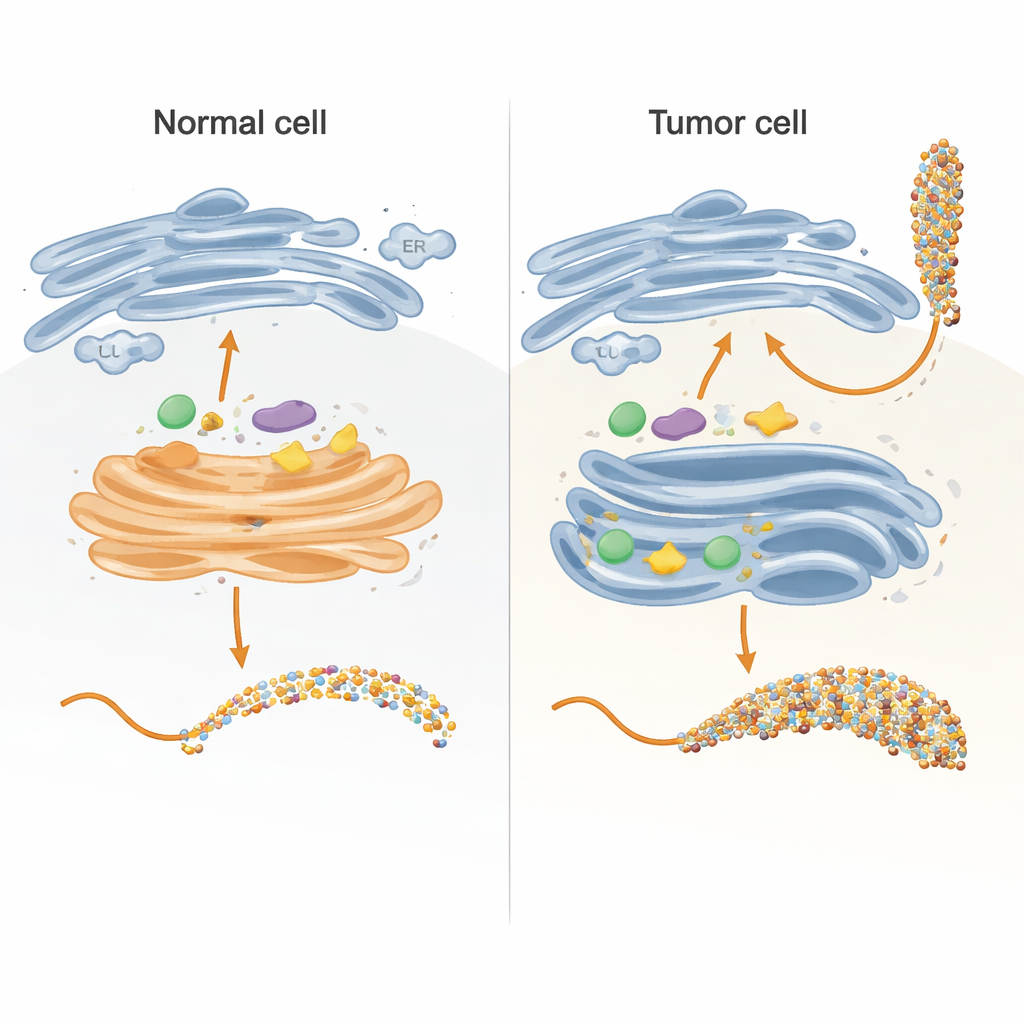
בניית מודל נשלט של "מפעל הסוכרים" התאי
בתוך התא, שרשראות הסוכר נבנות בעיקר בשתי מחלקות: הרשת האנדופלזמית (ER) וגולג'י, הפועלות כמו מסלול הרכבה רב‑שלבי. החוקרים שיחזרו חלקים מרכזיים של מסלול זה במבחנה באמצעות גרסה מהונדסת בקפידה של חלבון MUC1 המחוברת לתג נשא. הם הביטו את החלבון הממוזג בחיידקים, טהרו אותו, ואז חשפו אותו לאנזימים אנושיים שמוסיפים סוכרים בדרך כלל בתוך התאים. על‑ידי עיצוב מקטע ה‑MUC1 כך שכל אחד מחמשת אתרי ההיקשרות לסוכר מופיע פעם אחת בלבד וברצף טבעי, יכלו לעקוב בדיוק איזה אתר כל אנזים שינה ובאיזה סדר, באמצעות מדידות קינטיות רגישות ומסות ספקטרומטריה.
כיצד הדרכים הנורמליות והגידוליות נפרדות
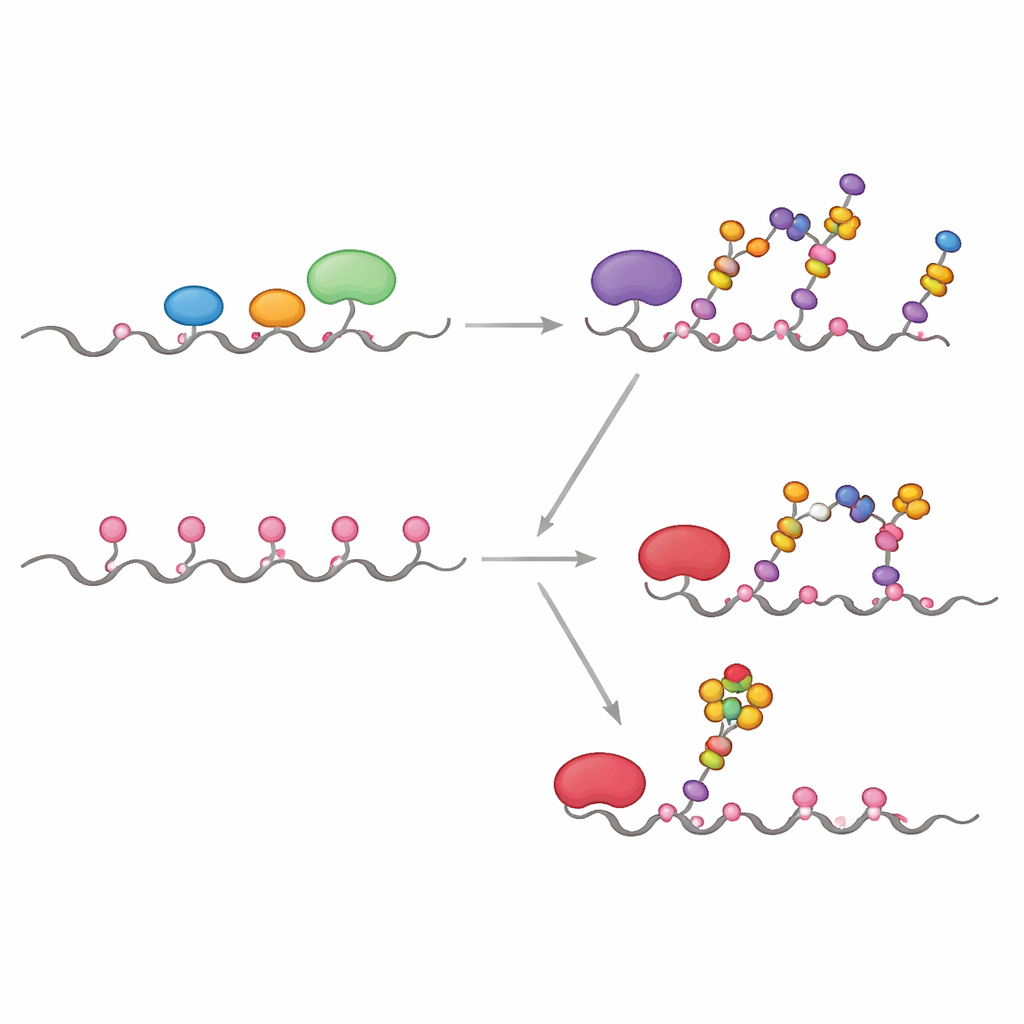
בתאים בריאים, האנזימים הראשונים בתהליך, המכונים GALNTs, ממוקמים בעיקר בחלק מוקדם של הגולג'י ופועלים בסמיכות לאנזימים אחרים שמאריכים או מסכמים את היחידות הסוכריות הראשוניות. הצוות הראה שבתנאי "קוה־לוקליזציה" כאלה, GALNTs מעדיפים בעיקר לשנות תת‑קבוצה של אתרים ב‑MUC1—מה שהמחברים קוראים אתרים ישירים—בעוד שני אתרים איטיים התלויים‑לקטין נשארים בדרך כלל בלתי ממולאים. ברגע שאת הסוכר הראשון (GalNAc) מוסיפים באתרי היעד הישירים, אנזימים יורדים בשרשרת כמו C1GALT1 מאריכים אותם במהירות, או ST6GALNAC1 ואחרים מוסיפים חומצת ניוראמינית (sialic acid), ובכך מונעים מ‑GALNTs להשתמש במנגנון התלוי לקטין כדי למלא בצפיפות את שאר האתרים. התוצאה היא דגם סוכר מתון ומבוקר, אופייני ל‑MUC1 אפיתליאלי נורמלי.
הדמיית העתקת מיקום האנזימים בדומה לסרטן
ברבים מהגידולים נראית תזוזה בולטת של אנזימי GALNT מהגולג'י בחזרה ל‑ER, יחד עם שינויים ברמות של מספר אנזימי גליקוזילציה. החוקרים חיקו זאת בכך שאיפשרו ל‑GALNTs לפעול ראשונים, בבידוד ובמשך זמן ארוך יותר, לפני שהכניסו את האנזימים היורדים. בתנאים אלה, הסוכרים הראשוניים התפשטו בהדרגה מאתרי היעד הקלים לאתרים האיטיים התלויים לקטין, עד שכל חמש העמדות ב‑MUC1 התמלאו. רק לאחר שלב הרוויה הזה הוספו אנזימי הארכה וסיום. התרחיש הדמוי‑ER הניב MUC1 מעוטר בצפיפות המזכיר את ה‑MUC1 הקשור לגידולים, עשיר באנטיגנים מסוג Tn ו‑sialyl‑Tn (sTn) הידועים בקשרם להתקדמות הסרטן, התחמקות חיסונית ומטסטזות.
מיקוד באתר חם יחיד
אחת התכונות הקליניות החשובות של MUC1 הגידולי היא נוכחות ה‑sialyl‑Tn, סוכר קצר המסוכם בחומצת נויראמינית ומחובר ישירות ל‑GalNAc. כדי לזהות בדיוק היכן הוא מופיע ב‑MUC1, שילב הצוות ניסויי קינטיקה, דוקינג ממוחשב וסימולציות היברידיות קוונטיות/קלאסיות. הם מצאו שהאנזים ST6GALNAC1 אחראי באופן ייחודי להוספת חומצת הניוראמינית בקישור α2‑6 לאנטיגנים Tn ו‑T על MUC1, ושיש לו העדפה חזקה לאתר תראונין מסוים באזור PDTR (המכונה T13 במאמר) ברגע שכל חמשת האתרים נושאים GalNAc. מודלים מבניים וסימולציות של מסלול התגובה מגלה שבאתר זה המיקום היחסי של הסוכר וחומצות האמינו הקטליטיות יוצר גאומטריה שמורידה את מחסום האנרגיה של התגובה יותר מאשר באתרים הסמוכים, ומה שמסביר מדוע sTn מופיע שם ראשון ובחוזקה רבה יותר.
השלכות להבנה ולטיפול בסרטן
ביחד, הניסויים והסימולציות הללו מראים שההבחנה בין MUC1 נורמלי ל‑MUC1 הקשור לגידול נשענת פחות על אילו אנזימים נמצאים וכמה על היכן הם ממוקמים בתא וכמה זמן הם יכולים לפעול לפני שנקטעים. כאשר GALNTs מוגבלים לגולג'י עם אנזימים מתחרים, הם מעטרים בעיקר את האתרים המהירים, ומייצרים בעיקר סוכרים מסוג core 1 וסיאלילציה מוגבלת. כשממוקמים ב‑ER, כפי שקורה ברבים מהגידולים, יש להם זמן למלא גם את האתרים המהירים וגם את האיטיים, וליצור MUC1 מצופה בצפיפות ב‑GalNAc שהופך לתשתית מצוינת ל‑ST6GALNAC1 באתר T13, מה שמגביר בצורה חדה את רמות sTn. נקודת מבט מערכתית זו מקשרת בין לוקליזציה של אנזימים, זמני תגובה וגאומטריה מולקולרית למסגרת אחת המסבירה כיצד שינוי לכאורה עדין במפעל הסוכרים התאי יכול לייצר סמנים חזקים וספציפיים לגידול ומציעה מטרות מדויקות יותר לאבחון, חיסון וטיפולים ממוקדי גליקאן בסרטן.
ציטוט: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
מילות מפתח: גליקוזילציה של חלבונים, MUC1, סמנים ביולוגיים של סרטן, גולג'י, נוגד-הציטול sialyl-Tn