Clear Sky Science · fr
Une approche in vitro pour simuler la divergence de l’O-glycosylation Golgi de la MUC1 associée aux tumeurs par rapport à la MUC1 normale
Pourquoi les « habillages » sucrés des protéines comptent en cancérologie
Nos cellules décorent en permanence leurs protéines par de courtes chaînes de sucres, formant une sorte de « revêtement » moléculaire qui influence la croissance cellulaire, la communication et les interactions avec le système immunitaire. Dans de nombreux cancers, ce revêtement sucré change de façon caractéristique, en particulier sur une protéine appelée MUC1, abondante à la surface des cellules épithéliales et des tumeurs. Cette étude met au point un modèle de laboratoire qui reproduit la manière dont les cellules ajoutent ces sucres, permettant aux scientifiques d’observer en détail comment les motifs glycosylés normaux de la MUC1 divergent vers des formes associées aux tumeurs qui favorisent la progression tumorale et l’évasion immunitaire.
Construire un modèle contrôlable de la « fabrique » à sucres de la cellule
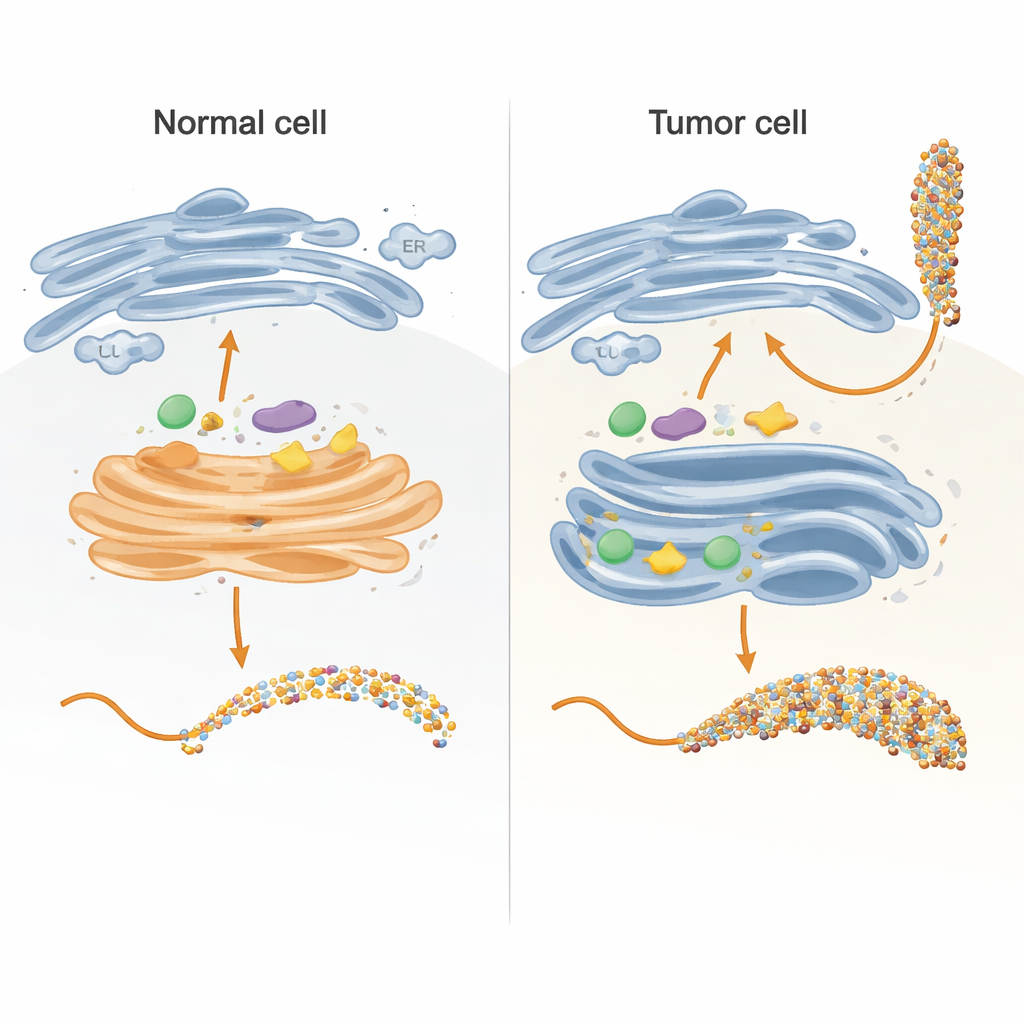
À l’intérieur des cellules, les chaînes de sucres sont principalement assemblées dans deux compartiments : le réticulum endoplasmique (RE) et l’appareil de Golgi, qui fonctionnent comme une chaîne de montage en plusieurs étapes. Les auteurs ont recréé des éléments clés de cette chaîne en éprouvette en utilisant une version ingénieusement conçue de la protéine MUC1 liée à une étiquette porteuse. Ils ont exprimé cette protéine de fusion dans des bactéries, l’ont purifiée, puis l’ont exposée à des enzymes humaines qui ajoutent normalement les sucres in vivo. En concevant le fragment de MUC1 de façon que chacun de ses cinq sites d’attachement de sucre n’apparaisse qu’une fois et dans une séquence naturelle, ils ont pu suivre précisément quel site chaque enzyme modifiait et dans quel ordre, en utilisant des mesures cinétiques sensibles et la spectrométrie de masse.
Comment les voies normale et tumorale se séparent
Dans les cellules saines, les premières enzymes du processus, appelées GALNTs, résident majoritairement dans une région précoce du Golgi et agissent de concert avec d’autres enzymes qui allongent ou terminent les unités sucrées initiales. L’équipe a montré que dans ces conditions « co-localisées », les GALNTs modifient principalement un sous-ensemble de sites sur la MUC1 — ce que les auteurs nomment sites directs — tandis que deux sites plus lents, dépendants de lectines, restent pour l’essentiel non occupés. Dès que le premier sucre (GalNAc) est ajouté aux sites directs, des enzymes en aval comme C1GALT1 les allongent rapidement, ou ST6GALNAC1 et d’autres sialyltransférases ajoutent de l’acide sialique, bloquant de fait le mécanisme lectine-dépendant des GALNTs pour remplir de façon dense les sites restants. Le résultat est un motif glycannique plus modéré et contrôlé, typique de la MUC1 épithéliale normale.
Simuler le remaniement de type tumoral des enzymes
De nombreuses tumeurs présentent une relocalisation marquée des GALNTs du Golgi vers le RE, accompagnée de modifications des niveaux de plusieurs enzymes de glycosylation. Les chercheurs ont imité cela en laissant les GALNTs agir d’abord, isolément, pendant des périodes prolongées avant d’introduire les enzymes en aval. Dans ces conditions, les sucres initiaux se propagent progressivement des sites directs faciles vers les sites plus lents dépendants de lectines, finissant par occuper les cinq positions de la MUC1. Ce n’est qu’après cette étape de saturation que les enzymes d’allongement et de terminaison ont été ajoutées. Ce scénario de type RE a produit une MUC1 fortement décorée, ressemblant à la MUC1 associée aux tumeurs, riche en antigènes Tn et sialyl-Tn (sTn) connus pour être corrélés à la progression tumorale, à l’évasion immunitaire et aux métastases.
Se concentrer sur un seul point chaud
Une des caractéristiques cliniquement les plus importantes de la MUC1 tumorale est la présence de sialyl-Tn, un sucre court, terminé par un acide sialique, attaché directement au GalNAc. Pour déterminer précisément où cela apparaît sur la MUC1, l’équipe a combiné des expériences cinétiques, du docking informatique et des simulations hybrides quantiques/classiques. Ils ont montré que l’enzyme ST6GALNAC1 est spécifiquement responsable de l’ajout d’acide sialique en liaison α2-6 aux antigènes Tn et T sur la MUC1, et qu’elle présente une forte préférence pour un thréonine particulier dans la région PDTR (appelé T13 dans l’article) une fois que les cinq sites portent un GalNAc. Les modèles structuraux et les simulations de trajectoire de réaction révèlent qu’à ce site, le sucre et les acides aminés catalytiques s’alignent dans une géométrie qui abaisse la barrière énergétique de la réaction plus qu’aux sites voisins, ce qui explique pourquoi le sTn y apparaît en premier et de manière prédominante.
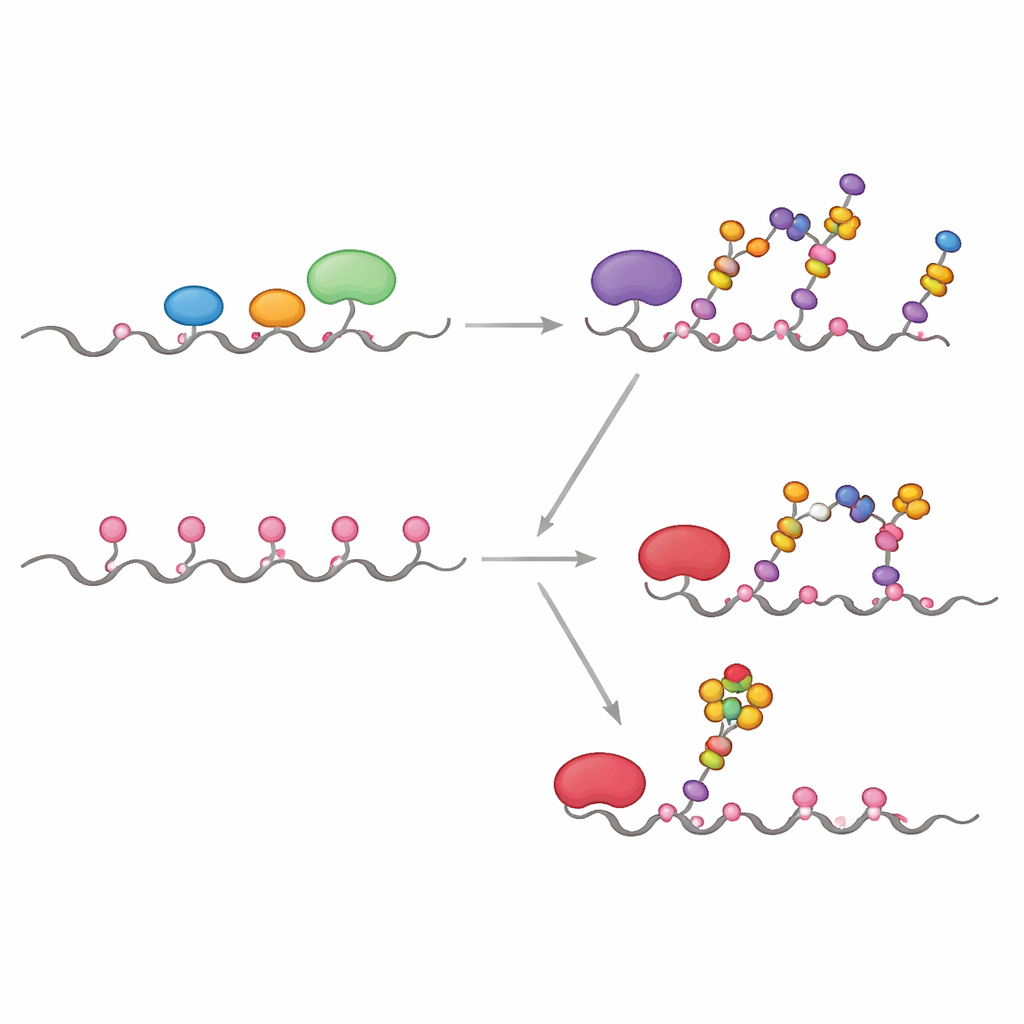
Ce que cela implique pour la compréhension et le ciblage du cancer
Ensemble, ces expériences et simulations montrent que la différence entre la MUC1 normale et la MUC1 associée aux tumeurs est moins déterminée par la présence ou l’absence d’enzymes que par leur localisation dans la cellule et par le temps dont elles disposent pour agir avant d’être interrompues. Lorsque les GALNTs sont confinés au Golgi en présence d’enzymes concurrentes, elles décorent principalement les sites rapides, donnant lieu à des cores 1 typiques et à une sialylation limitée. Lorsqu’elles sont relocalisées au RE, comme dans de nombreux cancers, elles ont le temps de remplir à la fois les sites rapides et lents, produisant une MUC1 densément couverte de GalNAc qui devient un substrat particulièrement favorable pour ST6GALNAC1 au site T13, augmentant fortement les niveaux de sTn. Cette vision à l’échelle du système relie la localisation enzymatique, la chronologie des réactions et la géométrie moléculaire en un cadre unique qui aide à expliquer comment un changement apparemment subtil dans la « fabrique » à sucres de la cellule peut générer des marqueurs tumoraux puissants et suggère des cibles plus précises pour le diagnostic, les vaccins et les thérapies anticancer centrées sur les glycannes.
Citation: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Mots-clés: glycosylation des protéines, MUC1, biomarqueurs du cancer, appareil de Golgi, antigène sialyl-Tn