Clear Sky Science · it
Un approccio in vitro per simulare la divergenza della O-glicosilazione del Golgi di MUC1 associata ai tumori rispetto a MUC1 normale
Perché i rivestimenti zuccherini sulle proteine sono importanti nel cancro
Le nostre cellule decorano costantemente le loro proteine con brevi catene di zuccheri, formando una sorta di “rivestimento” molecolare che influisce su crescita cellulare, comunicazione e interazioni con il sistema immunitario. In molti tumori questo rivestimento zuccherino cambia in modi distintivi, in particolare su una proteina chiamata MUC1, abbondante sulle cellule epiteliali e sulle superfici tumorali. Questo studio costruisce un modello di laboratorio che imita come le cellule aggiungono questi zuccheri, permettendo agli scienziati di osservare nel dettaglio come i pattern zuccherini normali di MUC1 divergano in forme associate ai tumori che favoriscono la crescita tumorale e l’evasione immunitaria.
Costruire un modello controllabile della “fabbrica” degli zuccheri cellulare
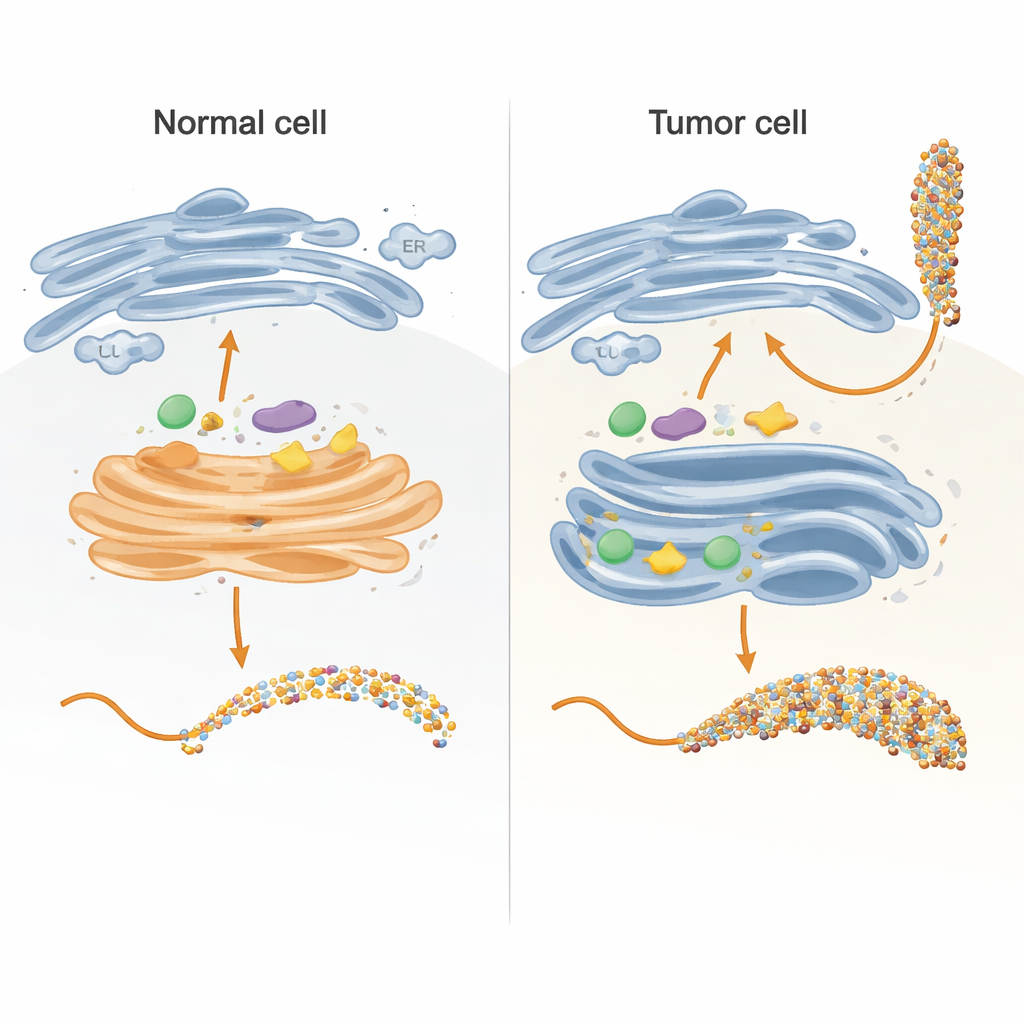
All’interno delle cellule, le catene zuccherine si costruiscono principalmente in due compartimenti: il reticolo endoplasmatico (RE) e l’apparato del Golgi, che funzionano come una linea di montaggio a più tappe. Gli autori hanno ricreato in provetta parti chiave di questa linea usando una versione ingegnerizzata della proteina MUC1 legata a un tag vettore. Hanno espresso questa proteina di fusione nei batteri, l’hanno purificata e poi l’hanno esposta ad enzimi umani che normalmente aggiungono zuccheri all’interno delle cellule. Progettando il frammento di MUC1 in modo che ciascuno dei suoi cinque siti di attacco degli zuccheri appaia una sola volta e in una sequenza naturale, hanno potuto tracciare esattamente quale sito ciascun enzima abbia modificato e in quale ordine, utilizzando misure cinetiche sensibili e spettrometria di massa.
Come i percorsi normali e tumorali si separano
Nelle cellule sane, i primi enzimi del processo, chiamati GALNT, risiedono per lo più in una parte precoce del Golgi e lavorano fianco a fianco con altri enzimi che estendono o cappano le unità zuccherine iniziali. Il gruppo ha dimostrato che in queste condizioni di “co-localizzazione”, i GALNT modificano principalmente un sottoinsieme di siti su MUC1—quelli che gli autori definiscono siti diretti—mentre due siti più lenti e dipendenti da lectine rimangono per lo più intatti. Appena il primo zucchero (GalNAc) viene aggiunto nei siti diretti, enzimi a valle come C1GALT1 li estendono rapidamente, oppure ST6GALNAC1 e altre sialiltransferasi aggiungono acido sialico, bloccando di fatto i GALNT dall’utilizzare il loro meccanismo basato sulle lectine per riempire densamente tutti i siti rimanenti. Il risultato è un pattern zuccherino più contenuto e controllato, tipico della MUC1 epiteliale normale.
Simulare il riposizionamento degli enzimi tipico del cancro
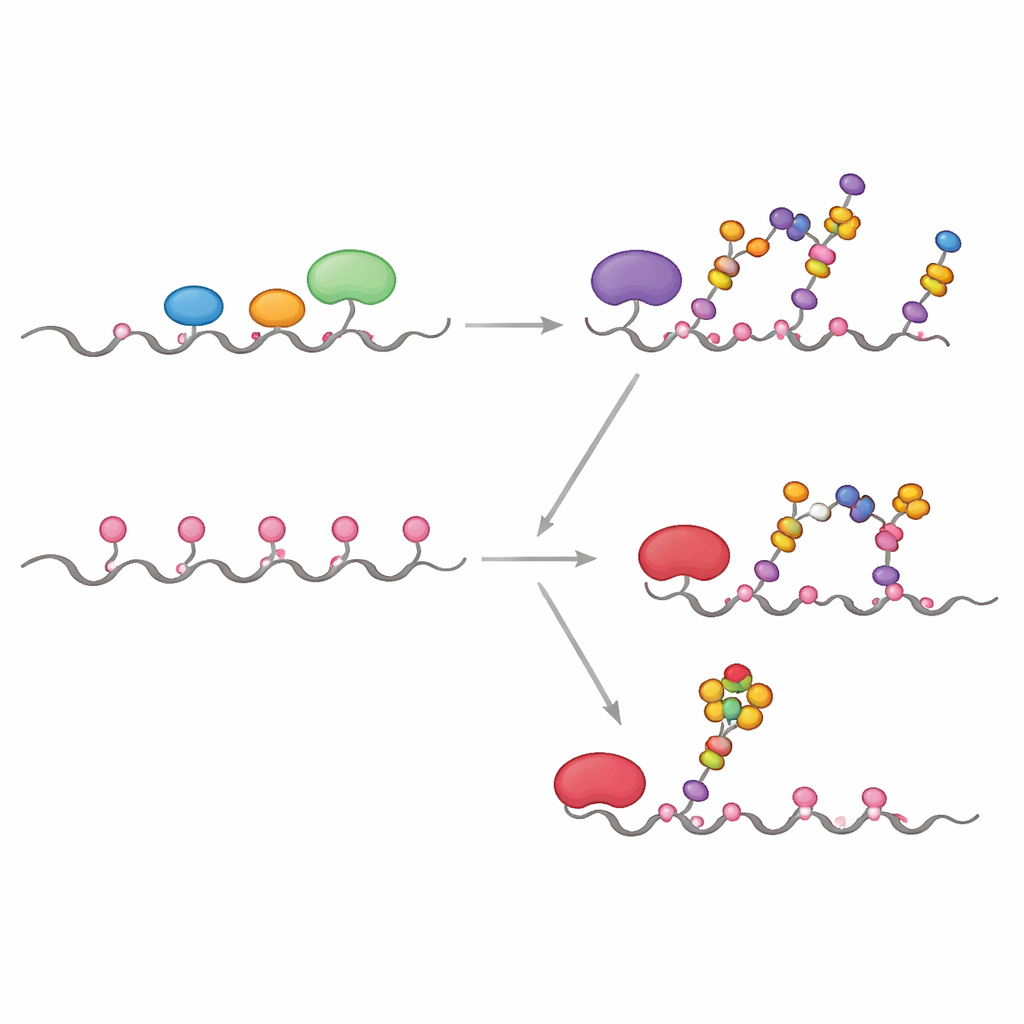
Molti tumori mostrano uno spostamento notevole degli enzimi GALNT dal Golgi al RE, insieme a cambiamenti nei livelli di vari enzimi della glicosilazione. I ricercatori hanno imitato questo lasciando agire i GALNT per primi, in isolamento, per periodi più lunghi prima di introdurre gli enzimi a valle. In queste condizioni, i primi zuccheri si sono gradualmente diffusi dai siti diretti più accessibili ai siti più lenti e dipendenti dalle lectine, occupando infine tutte e cinque le posizioni su MUC1. Solo dopo questa fase di saturazione sono stati aggiunti gli enzimi di estensione e capping. Questo scenario simile al RE ha prodotto una MUC1 intensamente decorata che assomiglia a MUC1 associata a tumori, ricca dei cosiddetti antigeni Tn e sialyl-Tn (sTn) noti per correlare con la progressione tumorale, l’evasione immunitaria e le metastasi.
Concentrare l’attenzione su un singolo punto critico
Una delle caratteristiche clinicamente più rilevanti della MUC1 tumorale è la presenza di sialyl-Tn, uno zucchero corto, cappato con acido sialico e attaccato direttamente al GalNAc. Per determinare esattamente dove questo compare su MUC1, il team ha combinato esperimenti cinetici, docking computazionale e simulazioni ibride quantistiche/classiche. Hanno scoperto che l’enzima ST6GALNAC1 è l’unico responsabile dell’aggiunta di acido sialico in legame α2-6 agli antigeni Tn e T su MUC1, e che mostra una forte preferenza per un particolare sito treonina nella regione PDTR (chiamato T13 nell’articolo) una volta che tutti e cinque i siti portano GalNAc. Modelli strutturali e simulazioni del percorso di reazione rivelano che in questo sito lo zucchero e gli amminoacidi catalitici si allineano in una geometria che abbassa la barriera energetica per la reazione più che nei siti vicini, spiegando perché sTn compare lì prima e con maggiore intensità.
Che cosa significa per comprendere e colpire il cancro
Nel complesso, questi esperimenti e simulazioni mostrano che la differenza tra MUC1 normale e MUC1 associata ai tumori è guidata meno dalla presenza o meno di specifici enzimi e più dalla loro localizzazione nella cellula e dal tempo a disposizione per agire prima di essere interrotti. Quando i GALNT sono confinati nel Golgi insieme a enzimi concorrenti, decorano per lo più solo i siti rapidi, generando zuccheri core 1 tipici e una sialilazione limitata. Quando vengono riposizionati nel RE, come avviene in molti tumori, hanno il tempo di riempire sia i siti veloci che quelli lenti, creando una MUC1 densamente coperta di GalNAc che diventa un substrato particolarmente favorevole per ST6GALNAC1 al sito T13, aumentando bruscamente i livelli di sTn. Questa visione a livello di sistema collega localizzazione enzimatica, tempistica delle reazioni e geometria molecolare in un unico quadro che aiuta a spiegare come un cambiamento apparentemente sottile nella “fabbrica” degli zuccheri cellulari possa generare marcatori tumorali potenti e suggerisce obiettivi più precisi per diagnostica, vaccini e terapie antitumorali focalizzate sui glicani.
Citazione: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Parole chiave: glicosilazione delle proteine, MUC1, biomarcatori del cancro, apparato del Golgi, antigene sialyl-Tn