Clear Sky Science · ru
In vitro-подход для моделирования расходящегося О-гликозилирования Голджи у опухолево-ассоциированного MUC1 и нормального MUC1
Почему сахарная «оболочка» белков важна при раке
Наши клетки постоянно украшают свои белки короткими цепочками сахаров, формируя своего рода молекулярную «оболочку», которая влияет на рост клеток, их общение и взаимодействие с иммунной системой. Во многих раках эта сахарная отделка меняется характерным образом, особенно на белке MUC1, который широко представлен на эпителиальных клетках и поверхности опухолей. В этом исследовании создана лабораторная модель, имитирующая добавление этих сахаров, что позволяет учёным подробно проследить, как нормальные схемы гликозилирования MUC1 расходятся в опухолево-ассоциированные формы, способствующие росту опухолей и уклонению от распознавания.
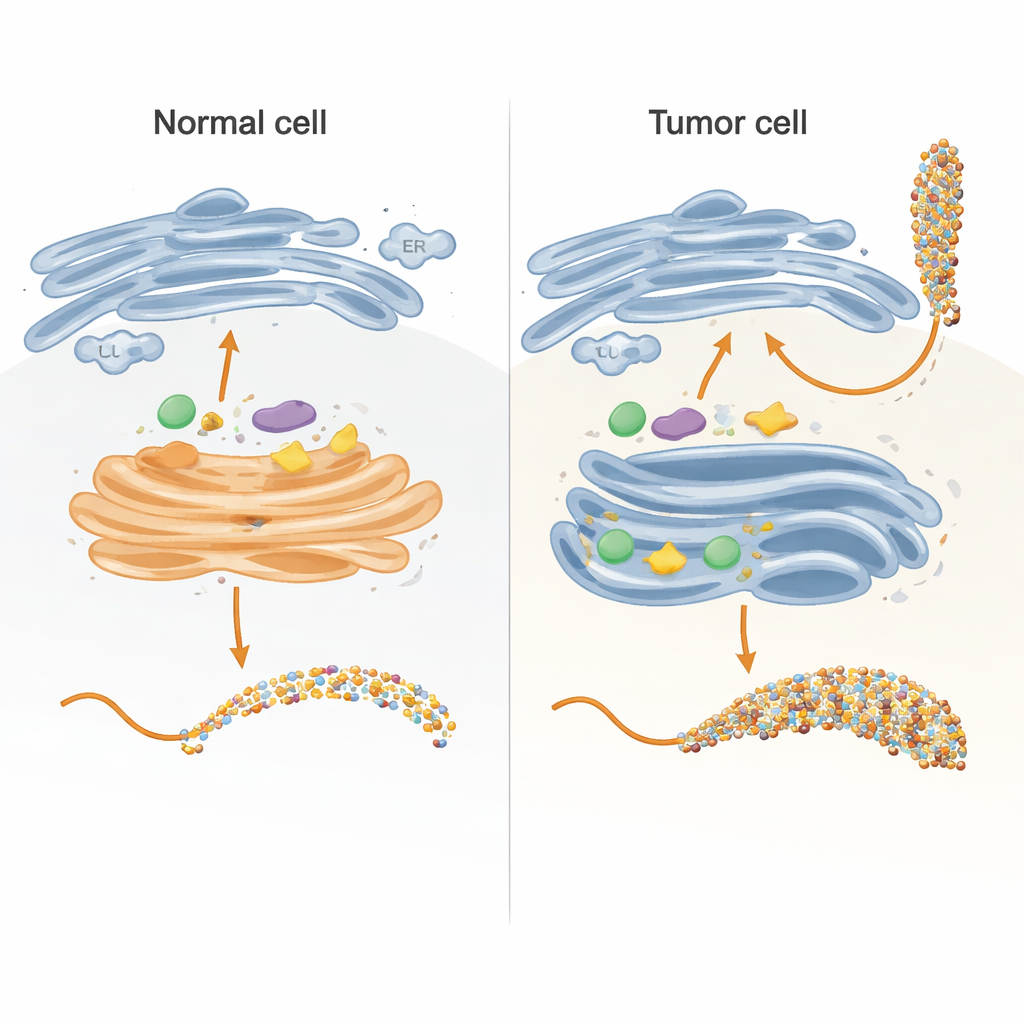
Создание управляемой модели «сахарной фабрики» клетки
Внутри клетки цепочки сахаров формируются главным образом в двух отделах: эндоплазматическом ретикулуме (ЭР) и аппарате Гольджи, которые действуют как многоступенчатая конвейерная линия. Авторы воссоздали ключевые участки этой линии в пробирке, использовав тщательно сконструированную версию белка MUC1, связанную с носителем. Они экспрессировали этот гибридный белок в бактериях, очистили его, а затем подвергли воздействию человеческих ферментов, которые обычно добавляют сахара внутри клетки. Разработав фрагмент MUC1 так, чтобы каждой из его пяти сайтов присоединения сахара соответствовал ровно один последовательный участок в естественной последовательности, исследователи могли точно отслеживать, какой сайт какой фермент модифицировал и в каком порядке, используя чувствительные кинетические измерения и масс-спектрометрию.
Как расходятся нормальный и опухолевый пути
В здоровых клетках первые ферменты процесса, называемые GALNT, главным образом локализуются в ранней части Гольджи и работают наряду с другими ферментами, которые удлиняют или «закрывают» начальные сахарные звенья. Команда показала, что в таких «сосуществующих» условиях GALNT в основном модифицируют подмножество сайтов на MUC1 — то, что авторы обозначают как прямые (direct) сайты — тогда как два более медленных сайта, зависящих от лектинов, остаются в значительной степени нетронутыми. Как только к прямым сайтам присоединяется первый сахар (GalNAc), последующие ферменты, такие как C1GALT1, быстро удлиняют их, либо ST6GALNAC1 и другие сиалилтрансферазы добавляют сиаловую кислоту, фактически блокируя механизм GALNT, основанный на лектинах, и не давая им плотно заполнить все оставшиеся сайты. В результате формируется более умеренный, контролируемый рисунок гликозилирования, типичный для нормального эпителиального MUC1.
Моделирование опухолевого перераспределения ферментов
Во многих опухолях наблюдается заметное перемещение ферментов GALNT из Гольджи обратно в ЭР, а также изменения в уровне нескольких ферментов гликозилирования. Исследователи воспроизвели это, позволив GALNT действовать первыми, в изоляции, на более длительное время, прежде чем вводить последующие ферменты. При таких условиях начальные сахара постепенно распространялись с легко модифицируемых прямых сайтов на более медленные лектино-зависимые сайты, в конечном итоге занимая все пять позиций на MUC1. Только после этой стадии насыщения вводились ферменты удлинения и «закрытия». Такой сценарий, имитирующий ЭР, приводил к сильной декоративной модификации MUC1, напоминающей опухолево-ассоциированный MUC1, богатый так называемыми антигенами Tn и sialyl-Tn (sTn), которые известны своей корреляцией с прогрессированием рака, уклонением от иммунитета и метастазированием.
Фокус на одном «очаговом» сайте
Одной из клинически важных черт опухолевого MUC1 является наличие sialyl-Tn — короткого сахарного остатка, завершающегося сиаловой кислотой и присоединённого непосредственно к GalNAc. Чтобы точно определить, где это появляется на MUC1, команда совместила кинетические эксперименты, компьютерное докирование и гибридные квантово-классические моделирования. Они обнаружили, что фермент ST6GALNAC1 уникально отвечает за добавление сиаловой кислоты в связи α2-6 к антигенам Tn и T на MUC1 и что он демонстрирует сильное предпочтение к одному конкретному треониновому сайту в области PDTR (в статье обозначаемому как T13), когда все пять сайтов несут GalNAc. Структурные модели и моделирование путей реакции показывают, что в этом сайте сахар и катализирующие аминокислоты выстраиваются в геометрию, снижающую энергетический барьер реакции сильнее, чем в соседних сайтах, что объясняет, почему sTn появляется здесь первым и наиболее выраженно.
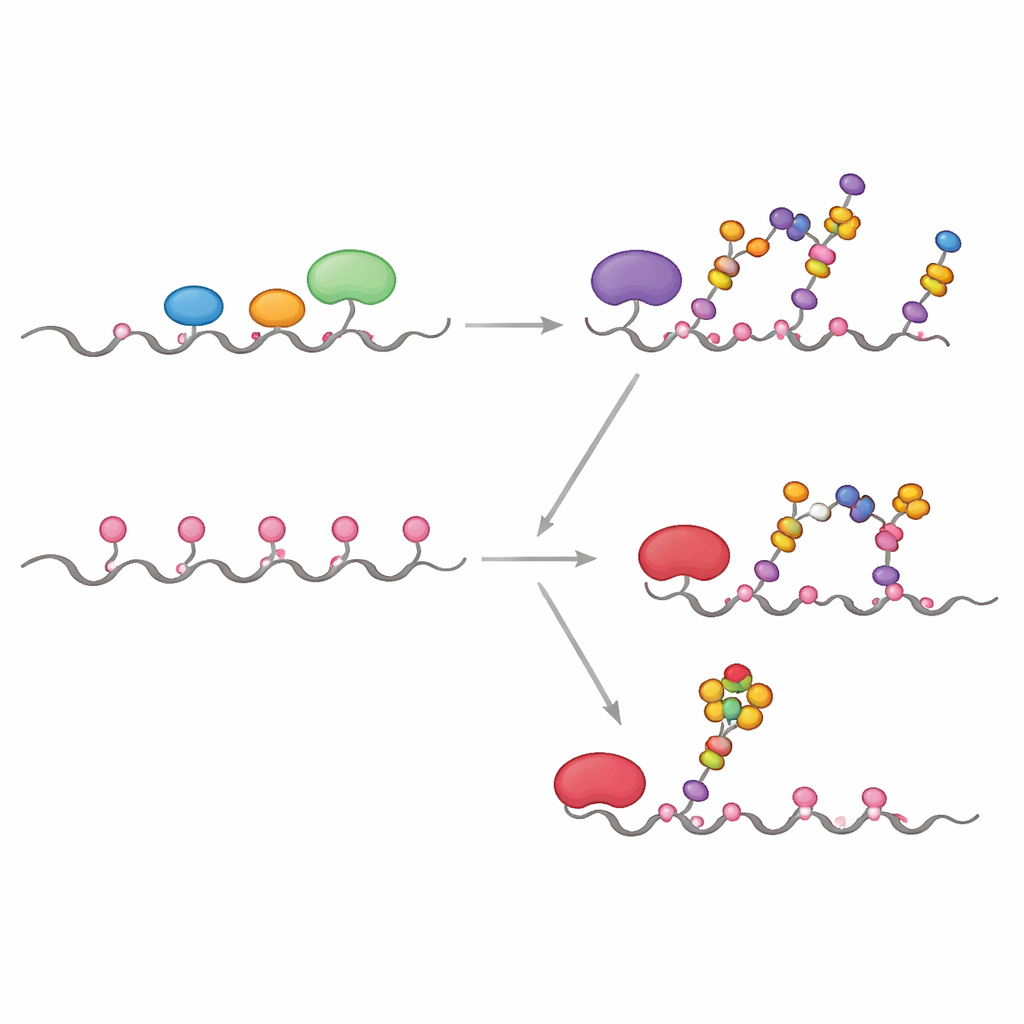
Что это значит для понимания и таргетирования рака
В совокупности эти эксперименты и моделирования показывают, что разница между нормальным и опухолево-ассоциированным MUC1 определяется не столько тем, какие ферменты присутствуют, сколько тем, где они локализованы в клетке и как долго они могут действовать до вмешательства. Когда GALNT ограничены Гольджи и конкурируют с другими ферментами, они в основном модифицируют только быстрые сайты, что приводит к типичным кор-1 сахарам и ограниченной сиализации. Когда же они перемещаются в ЭР, как это происходит во многих раках, у них появляется время заполнить как быстрые, так и медленные сайты, формируя плотно покрытый GalNAc MUC1, который становится особенно хорошим субстратом для ST6GALNAC1 на сайте T13, что резко повышает уровни sTn. Этот системный взгляд связывает локализацию ферментов, временные параметры реакций и молекулярную геометрию в единую схему, которая помогает объяснить, как, казалось бы, тонкое изменение в «сахарной фабрике» клетки может порождать мощные опухолево-специфичные маркеры и указывает на более точные мишени для диагностики, вакцин и терапий, ориентированных на гликаны.
Цитирование: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Ключевые слова: гликозилирование белков, MUC1, онкологические маркеры, аппарат Гольджи, антиген sialyl-Tn