Clear Sky Science · de
Ein in vitro-Ansatz zur Simulation divergenter Golgi-O-Glykosylierung von tumorassoziiertem MUC1 gegenüber normalem MUC1
Warum Zuckerhüllen auf Proteinen bei Krebs wichtig sind
Unsere Zellen verzieren ihre Proteine ständig mit kleinen Zuckerketten und bilden so eine Art molekularen „Mantel“, der beeinflusst, wie Zellen wachsen, kommunizieren und mit dem Immunsystem interagieren. Bei vielen Krebserkrankungen verändert sich diese Zuckerschicht auf charakteristische Weise, insbesondere auf einem Protein namens MUC1, das auf Epithelzellen und Tumoroberflächen reichlich vorkommt. Diese Studie entwickelt ein Labor-Modell, das nachahmt, wie Zellen diese Zucker anfügen, und ermöglicht es Wissenschaftlern, im Detail zu sehen, wie normale Zuckerprofile von MUC1 in tumorassoziierte Formen übergehen, die Krebswachstum unterstützen und die Erkennung erschweren.
Aufbau eines kontrollierbaren Modells der zellulären Zuckerfabrik
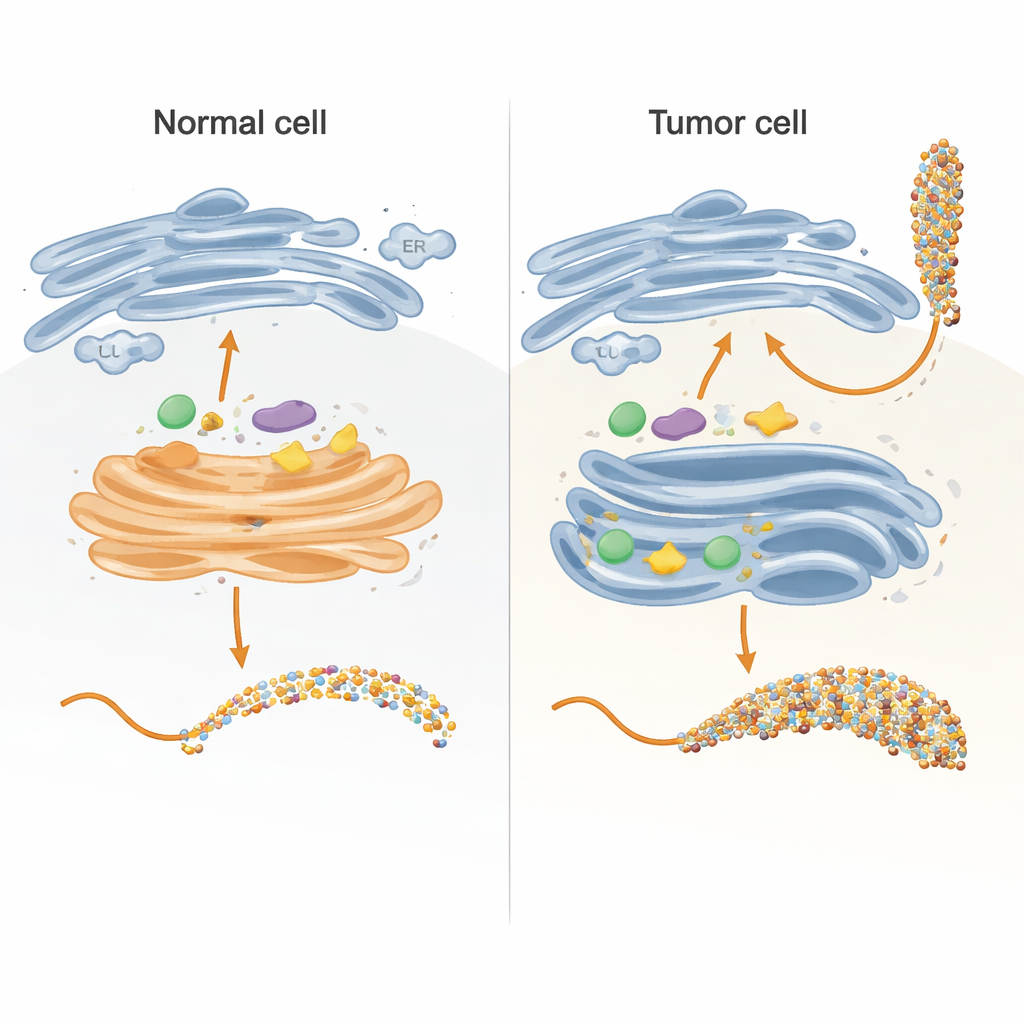
Innerhalb der Zelle werden Zuckerketten hauptsächlich in zwei Kompartimenten aufgebaut: im endoplasmatischen Retikulum (ER) und im Golgi-Apparat, die wie eine mehrstufige Montagelinie funktionieren. Die Autoren rekonstruierten Schlüsselteile dieser Linie im Reagenzglas, indem sie eine sorgfältig konstruierte Version des MUC1-Proteins an ein Trägertag banden. Sie exprimierten dieses Fusionsprotein in Bakterien, reinigten es und setzten es anschließend humanen Enzymen aus, die normalerweise innerhalb der Zelle Zucker anfügen. Indem sie das MUC1-Fragment so gestalteten, dass jede seiner fünf Zuckeransatzstellen nur einmal und in natürlicher Reihenfolge vorkommt, konnten sie genau verfolgen, welche Stelle jedes Enzym modifizierte und in welcher Reihenfolge — mittels empfindlicher kinetischer Messungen und Massenspektrometrie.
Wie sich normale und tumorhafte Wege aufspalten
In gesunden Zellen befinden sich die ersten Enzyme des Prozesses, die sogenannten GALNTs, überwiegend in einem frühen Golgi-Abschnitt und arbeiten dort zusammen mit anderen Enzymen, die die initialen Zucker erweitern oder verschließen. Das Team zeigte, dass unter diesen „ko- lokalisierten“ Bedingungen GALNTs hauptsächlich eine Teilmenge von Stellen auf MUC1 modifizieren — die Autoren bezeichnen sie als direkte Stellen — während zwei langsamere, lectinabhängige Stellen größtenteils unberührt bleiben. Sobald an den direkten Stellen das erste Zucker (GalNAc) hinzugefügt ist, verlängern nachgeschaltete Enzyme wie C1GALT1 sie schnell, oder ST6GALNAC1 und andere Sialyltransferasen fügen Sialinsäure hinzu, wodurch GALNTs effektiv daran gehindert werden, ihren lectinbasierten Mechanismus zu nutzen, um alle verbleibenden Stellen dicht zu füllen. Das Ergebnis ist ein moderateres, kontrolliertes Zuckerprofil, typisch für normales epithelialen MUC1.
Simulation der krebsähnlichen Umverteilung von Enzymen
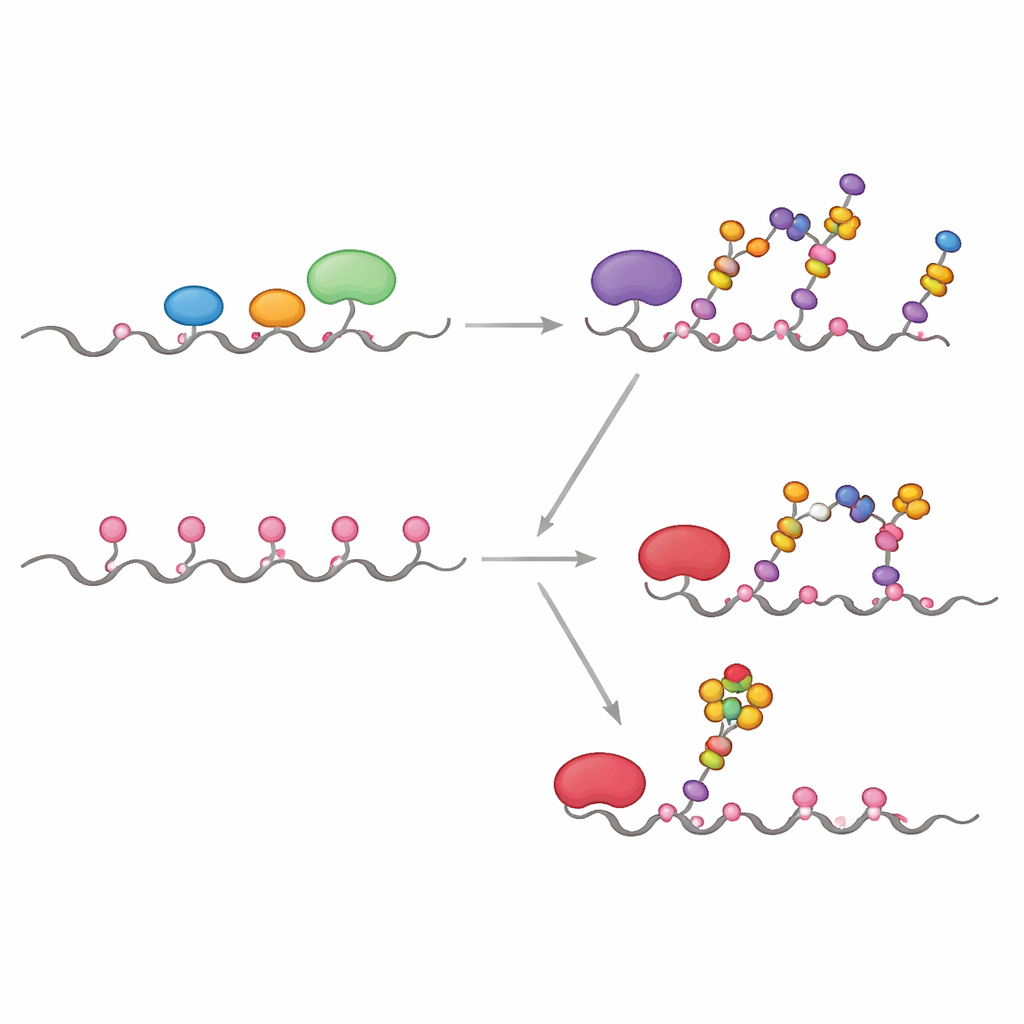
Viele Tumoren zeigen eine markante Verlagerung der GALNT-Enzyme aus dem Golgi zurück in das ER, einhergehend mit Veränderungen der Konzentration mehrerer Glykosylierungsenzyme. Die Forscher ahmten dies nach, indem sie GALNTs längere Zeit zuerst isoliert wirken ließen, bevor sie die nachgeschalteten Enzyme zusetzten. Unter diesen Bedingungen breiteten sich die initialen Zucker allmählich von den leicht zugänglichen direkten Stellen auf die langsameren lectinabhängigen Stellen aus und besetzten schließlich alle fünf Positionen auf MUC1. Erst nach diesem Sättigungsschritt wurden Verlängerungs- und Verschlussenzyme hinzugefügt. Dieses ER-ähnliche Szenario ergab ein stark dekoriertes MUC1, das tumorassoziatem MUC1 ähnelt und reich an den sogenannten Tn- und sialyl-Tn-(sTn)-Antigenen ist, die mit Krebsprogression, Immunevasion und Metastasierung in Verbindung gebracht werden.
Fokussierung auf eine einzelne Hot-Spot-Stelle
Eines der klinisch bedeutendsten Merkmale von tumoralem MUC1 ist das Vorkommen von sialyl-Tn, einem kurzen, mit Sialinsäure gekappten Zucker, der direkt an GalNAc gebunden ist. Um genau zu bestimmen, wo dies auf MUC1 erscheint, kombinierten die Forscher kinetische Experimente, Computer-Docking und hybride Quanten-/klassische Simulationen. Sie fanden heraus, dass das Enzym ST6GALNAC1 einzigartig dafür verantwortlich ist, Sialinsäure in einer α2-6-Bindung an Tn- und T-Antigene auf MUC1 anzuhängen, und dass es eine starke Präferenz für eine bestimmte Threonin-Stelle in der PDTR-Region (im Papier T13 genannt) zeigt, sobald alle fünf Stellen GalNAc tragen. Strukturmodelle und Reaktionsweg-Simulationen zeigen, dass an dieser Stelle Zucker und katalytische Aminosäuren in einer Geometrie ausgerichtet sind, die die Aktivierungsbarriere für die Reaktion stärker senkt als an benachbarten Stellen, was erklärt, warum sTn dort zuerst und am stärksten auftritt.
Was das für das Verständnis und die Bekämpfung von Krebs bedeutet
Zusammen zeigen diese Experimente und Simulationen, dass der Unterschied zwischen normalem und tumorassoziiertem MUC1 weniger davon abhängt, welche Enzyme vorhanden sind, als vielmehr davon, wo sie in der Zelle lokalisiert sind und wie lange sie wirken können, bevor sie unterbrochen werden. Wenn GALNTs im Golgi mit konkurrierenden Enzymen zusammengehalten werden, dekorieren sie überwiegend nur die schnellen Stellen, was zu typischen Core-1-Zuckern und begrenzter Sialylierung führt. Werden sie, wie in vielen Tumoren, ins ER verlagert, gewinnen sie Zeit, sowohl schnelle als auch langsame Stellen zu besetzen, wodurch ein dicht mit GalNAc bedecktes MUC1 entsteht, das ein besonders guter Substrat für ST6GALNAC1 an der T13-Stelle wird und die sTn-Spiegel stark erhöht. Diese Systemsicht verknüpft Enzymlokalisation, Reaktionszeit und molekulare Geometrie zu einem Rahmen, der erklärt, wie eine scheinbar kleine Änderung in der zellulären Zuckerfabrik potente tumor-spezifische Marker erzeugen kann, und deutet auf präzisere Ziele für Diagnostik, Impfstoffe und glykanorientierte Krebstherapien hin.
Zitation: Nashed, A., Dilsook, K., Senapathi, T. et al. An in vitro approach for simulating divergent Golgi O-glycosylation of tumor-associated MUC1 from normal MUC1. Nat Commun 17, 3619 (2026). https://doi.org/10.1038/s41467-026-72151-y
Schlüsselwörter: Protein-Glykosylierung, MUC1, Krebs-Biomarker, Golgi-Apparat, sialyl-Tn-Antigen